Clear Sky Science · fr
L’axe REDD1–NF-κB–miARN–eNOS/SIRT1 médie la sénescence des cellules endothéliales et l’hypertension induites par l’obésité
Pourquoi nos vaisseaux sanguins vieillissent plus vite en cas d’obésité
L’obésité est bien connue pour augmenter le risque d’hypertension, d’infarctus et d’accidents vasculaires cérébraux, mais la manière dont l’excès de graisse vieillit et rigidifie nos vaisseaux est restée obscure. Cette étude met au jour une « conversation » moléculaire au sein de la fine couche cellulaire qui tapisse nos artères, montrant comment le stress métabolique lié à l’obésité peut vieillir prématurément ces cellules, endommager les reins et entraîner de l’hypertension. Comprendre cette chaîne d’événements met en évidence des cibles thérapeutiques très précises susceptibles de protéger les vaisseaux chez les personnes obèses.
La contrainte cachée sur les cellules de la paroi vasculaire
La couche la plus interne des vaisseaux sanguins est constituée d’endothélium, des cellules qui contrôlent le flux sanguin, la relaxation vasculaire et l’inflammation. En cas d’obésité, les taux d’acides gras, de cholestérol, de sucre et de signaux hormonaux augmentent dans le sang. Les auteurs ont nourri des souris avec un régime riche en graisses pour reproduire cet état et ont exposé des cellules endothéliales humaines à des facteurs liés à l’obésité comme l’acide palmitique, les LDL oxydés, une glycémie élevée, la leptine et la résistine. Ces conditions ont induit chez les cellules des signes classiques de sénescence, un état d’arrêt permanent où les cellules cessent de se diviser, accumulent des déchets et libèrent des substances inflammatoires. Chez les souris, l’aorte — l’artère principale sortant du cœur — a développé des zones d’endothélium vieilli et a perdu une partie de sa capacité de relaxation, contribuant à l’élévation de la pression artérielle.
Un capteur de stress qui bascule les cellules vers le vieillissement
L’équipe s’est intéressée à une protéine sensible au stress appelée REDD1, activée par le stress métabolique et oxydatif. Ils ont observé que les facteurs de risque métabolique augmentaient fortement les niveaux de REDD1 dans des cellules endothéliales humaines et murines en culture ainsi que dans les artères de souris obèses. Lorsque REDD1 était surexprimée expérimentalement dans les vaisseaux, les cellules endothéliales devenaient rapidement sénescentes, la production d’oxyde nitrique diminuait et les artères se rigidifiaient, entraînant de l’hypertension. En revanche, une forme mutante de REDD1 incapable de signaler via une voie inflammatoire clé ne provoquait pas ces effets. Les souris privées de REDD1, ou dont REDD1 était supprimée spécifiquement dans les cellules endothéliales, étaient en grande partie protégées : leurs artères montraient moins de cellules sénescentes, des niveaux plus élevés de molécules protectrices, une meilleure relaxation vasculaire et une pression artérielle plus basse malgré l’obésité.
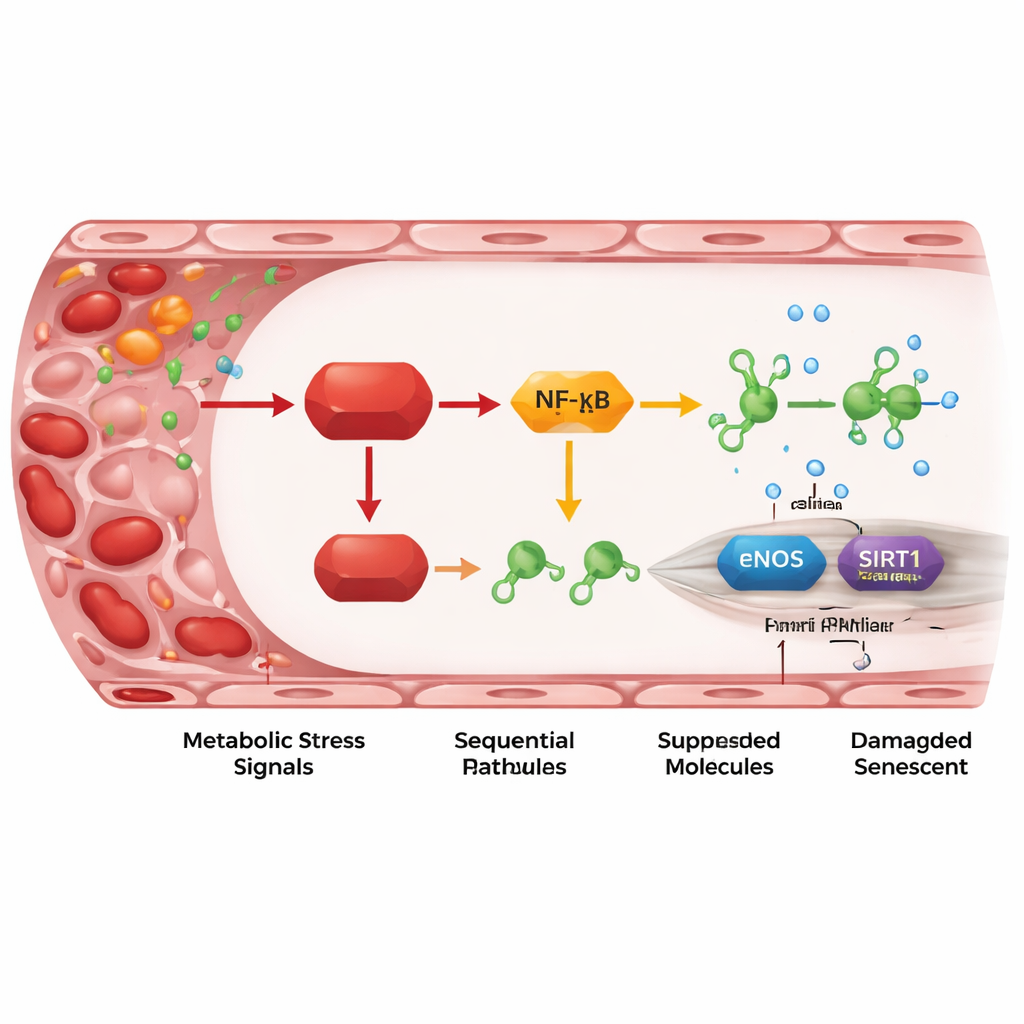
Une transmission inflammatoire de REDD1 vers des gènes protecteurs
En approfondissant, les chercheurs ont cartographié une suite d’étapes moléculaires reliant REDD1 aux lésions vasculaires. REDD1 active une version « atypique » de la voie NF-κB, un régulateur majeur de l’inflammation. Celle-ci augmente à son tour les niveaux de deux petits ARN régulateurs, miR-155-5p et surtout miR-214-3p. Ces microARN agissent comme de minuscules freins sur deux protéines protectrices de l’endothélium : eNOS, qui produit l’oxyde nitrique relaxant les vaisseaux, et SIRT1, qui participe au maintien de la jeunesse cellulaire et de la stabilité de l’ADN. Quand REDD1 est élevé, les microARN augmentent, eNOS et SIRT1 diminuent, la production d’oxyde nitrique chute et les marqueurs de sénescence augmentent. Bloquer ces microARN ou augmenter SIRT1 ou l’oxyde nitrique permettait d’inverser une grande partie des dommages, montrant que cet axe ne se contente pas d’être corrélé au vieillissement vasculaire mais en est un véritable moteur.
Preuves issues de modèles génétiques et effets rénaux
Plusieurs modèles murins ont permis aux auteurs de tester chaque étape de cet axe in vivo. Les souris obèses dépourvues de REDD1, exprimant la forme mutante non signalante de REDD1 ou génétiquement modifiées pour éliminer REDD1 uniquement dans les cellules endothéliales présentaient toutes un vieillissement artériel réduit et une pression artérielle plus basse. Les souris dépourvues de miR-214-3p étaient elles aussi protégées : même si REDD1 augmentait avec l’obésité, eNOS et SIRT1 restaient plus élevés, la signalisation de l’oxyde nitrique était mieux préservée et la sénescence vasculaire et l’hypertension étaient atténuées. La même voie REDD1–microARN affectait les reins, organes cruciaux pour le contrôle à long terme de la pression artérielle. Chez les souris obèses de type sauvage, les reins s’agrandissaient, devenaient fibreux et la créatinine plasmatique augmentait, signes de lésions rénales. Ces signes étaient beaucoup plus faibles chez les souris dépourvues de REDD1, dépourvues de REDD1 endothélial ou dépourvues de miR-214-3p, suggérant que la protection des vaisseaux aide aussi à préserver la fonction rénale.
Implications pour de futurs traitements
Pour un lecteur non spécialiste, ce travail montre que l’obésité n’augmente pas la pression artérielle simplement en ajoutant du poids ; elle reprogramme profondément la biologie de la paroi vasculaire. L’étude identifie une chaîne clé de coupables — REDD1, la signalisation NF-κB atypique et les microARN miR-155-5p et miR-214-3p — qui, ensemble, inhibent eNOS et SIRT1 protecteurs, accélérant le vieillissement des vaisseaux et des reins et élevant la pression artérielle. Parce que chaque maillon de cette chaîne peut être modulé chez la souris pour restaurer des vaisseaux plus sains même après l’apparition de l’obésité, l’axe REDD1–NF-κB–microARN–eNOS/SIRT1 apparaît comme un plan d’action prometteur pour des médicaments visant à prévenir ou traiter l’hypertension liée à l’obésité et ses complications.
Citation: Choi, Y.K., Lee, DK., Park, M. et al. The REDD1–NF-κB–miRNAs–eNOS/SIRT1 axis mediates obesity-induced endothelial cell senescence and hypertension. Nat Commun 17, 3843 (2026). https://doi.org/10.1038/s41467-026-70601-1
Mots-clés: obésité, sénescence endothéliale, hypertension, microARN, oxyde nitrique