Clear Sky Science · nl
De REDD1–NF-κB–miRNA’s–eNOS/SIRT1-as maakt obesitas-geïnduceerde veroudering van endotheelcellen en hypertensie mogelijk
Waarom onze bloedvaten sneller verouderen bij obesitas
Obesitas staat erom bekend dat het het risico op hoge bloeddruk, hartinfarcten en beroertes verhoogt, maar hoe overtollig vet precies onze bloedvaten verouderd en stijf maakt, bleef onduidelijk. Deze studie onthult een moleculair "gesprek" binnen de dunne cellaag die onze slagaders bekleedt, en laat zien hoe metabole stress door obesitas deze cellen voortijdig kan laten verouderen, de nieren kan beschadigen en hypertensie kan aanjagen. Inzicht in deze keten van gebeurtenissen wijst op nieuwe, zeer specifieke doelen voor geneesmiddelen die bloedvaten bij mensen met obesitas zouden kunnen beschermen.
De verborgen belasting van de vaatbekleding
De binnenste bekleding van bloedvaten bestaat uit endotheelcellen, die fungeren als poortwachters voor bloedstroom, vaatontspanning en ontsteking. Bij obesitas stijgen niveaus van vetzuren, cholesterol, suiker en hormoonachtige signalen in de bloedbaan. De auteurs voedden muizen met een vetrijk dieet om deze toestand na te bootsen en behandelden humane endotheelcellen met obesitas-gerelateerde factoren zoals palmitinezuur, geoxideerd LDL, hoge glucose, leptine en resistine. Deze condities leidden ertoe dat de cellen klassieke tekenen van senescentie vertoonden, een toestand van permanente arrestatie waarin cellen stoppen met delen, afval ophopen en ontstekingsbevorderende stoffen afgeven. Bij de muizen ontwikkelde de aorta — de hoofdslagader die het hart verlaat — plekken met verouderde endotheelcellen en verloor ze haar vermogen om goed te ontspannen, wat bijdroeg aan verhoogde bloeddruk.
Een stresssensor die cellen naar ouderdom kantelt
Het team richtte zich op een stress-gevoelig eiwit genaamd REDD1, dat wordt aangeschakeld door metabole en oxidatieve stress. Ze ontdekten dat metabole risicofactoren sterk verhoogde REDD1-niveaus gaven in gekweekte humane en muis-endotheelcellen en in de slagaders van obese muizen. Wanneer REDD1 experimenteel verhoogd werd in bloedvaten, werden endotheelcellen snel senescent, daalde de productie van stikstofoxide en verstijfden de slagaders, waardoor hypertensie ontstond. Daarentegen veroorzaakte een gemuteerde vorm van REDD1 die niet meer via een belangrijke ontstekingsroute kon signaleren deze problemen niet. Muizen die genetisch geen REDD1 hadden, of REDD1 specifiek misten in hun endotheelcellen, waren grotendeels beschermd: hun slagaders toonden minder senescente cellen, hogere niveaus van beschermende moleculen, betere vaatontspanning en lagere bloeddruk ondanks obesitas.
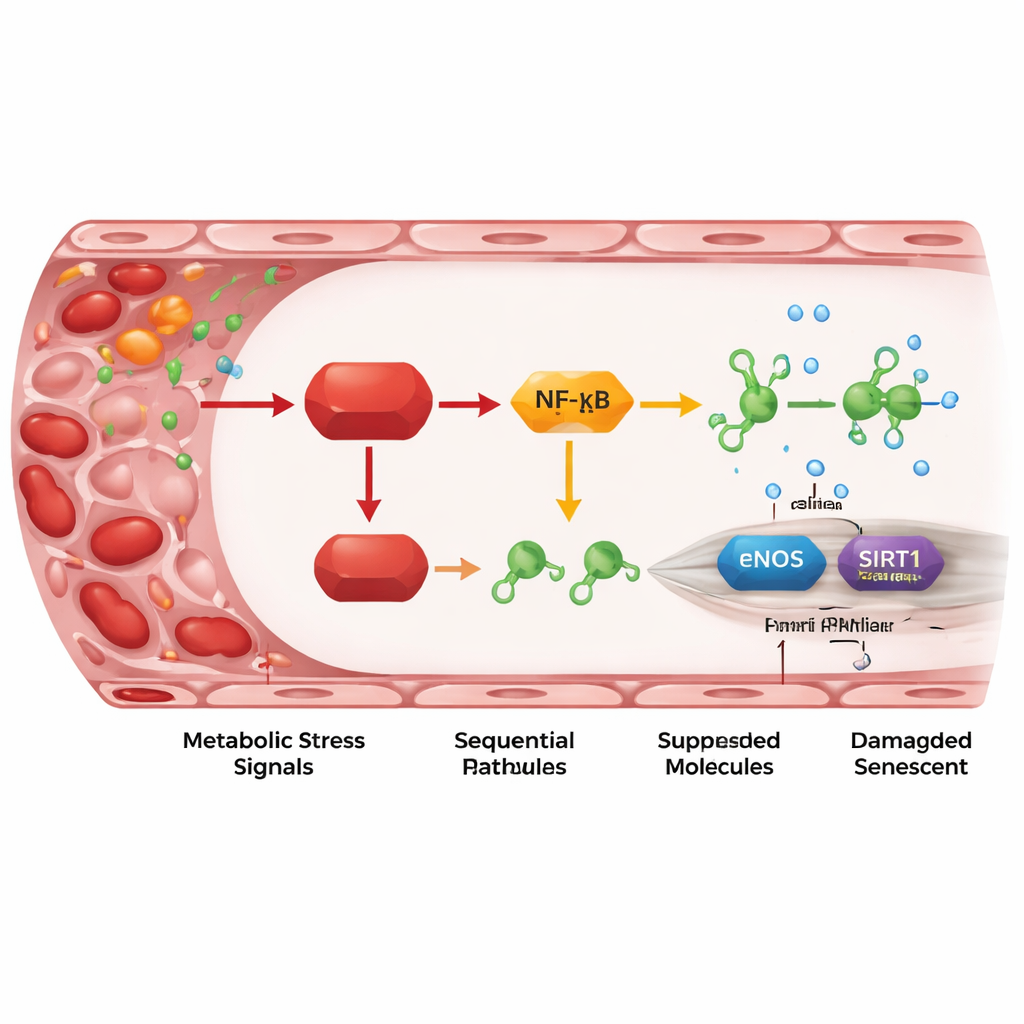
Een ontstekingsrelais van REDD1 naar beschermende genen
Dieper gravend brachten de onderzoekers een relais van moleculaire stappen in kaart die REDD1 koppelt aan vaatschade. REDD1 activeert een "atypische" variant van de NF-κB-route, een hoofdregulator van ontsteking. Dit verhoogt op zijn beurt de niveaus van twee kleine regulatorische RNA’s, miR-155-5p en vooral miR-214-3p. Deze microRNA’s fungeren als kleine remmen op twee beschermende eiwitten in endotheelcellen: eNOS, dat stikstofoxide produceert om vaten te ontspannen, en SIRT1, dat helpt de jeugdigheid van cellen en de stabiliteit van DNA te behouden. Wanneer REDD1 hoog was, stegen de microRNA-niveaus, daalden eNOS- en SIRT1-niveaus, nam de productie van stikstofoxide af en namen de senescentiemarkers toe. Het blokkeren van de microRNA’s of het verhogen van SIRT1 of stikstofoxide kon veel van de schade terugdraaien, wat aantoont dat deze as niet alleen geassocieerd is met, maar daadwerkelijk de veroudering van de vaatwand aandrijft.
Bewijs uit genetische modellen en nier-effecten
Verschillende muismodellen stelden de auteurs in staat elke stap van deze as in levende dieren te testen. Obese muizen zonder REDD1, die de niet-signalerende REDD1-mutant tot expressie brachten, of die zodanig waren gewijzigd dat REDD1 alleen in endotheelcellen werd verwijderd, toonden allemaal verminderde arteriële veroudering en lagere bloeddruk. Muizen die miR-214-3p misten waren vergelijkbaar beschermd: hoewel REDD1 bij obesitas nog steeds toenam, bleven eNOS en SIRT1 hoger, was de stikstofoxidesignalering beter behouden en werden vasculaire senescentie en hypertensie afgezwakt. Dezelfde REDD1–microRNA-route beïnvloedde de nieren, organen die cruciaal zijn voor langetermijnbloeddrukregulatie. Bij obese wildtype-muizen vergrootten de nieren, werden ze fibrotisch en kwam er meer creatinine in het bloed terecht. Deze tekenen van nierschade waren veel milder in muizen zonder REDD1, zonder endotheliaal REDD1 of zonder miR-214-3p, wat suggereert dat het beschermen van bloedvaten ook de nierfunctie hielp veiligstellen.
Wat dit betekent voor toekomstige therapieën
Voor een niet-specialist toont dit werk aan dat obesitas niet simpelweg de bloeddruk verhoogt door extra lichaamsmassa; het herprogrammeert de biologie van de vaatbekleding op diep niveau. De studie identificeert een sleutelketen van daders — REDD1, atypische NF-κB-signaalvoering en microRNA’s miR-155-5p en miR-214-3p — die samen beschermende eNOS en SIRT1 uitschakelen, waardoor bloedvaten en nieren sneller verouderen en de bloeddruk stijgt. Omdat elk schakel in deze keten in muizen wijzigbaar is om gezondere vaten te herstellen, zelfs na het optreden van obesitas, verschijnt de REDD1–NF-κB–microRNA–eNOS/SIRT1-as als een veelbelovend blauwdruk voor geneesmiddelen gericht op het voorkomen of behandelen van obesitas-geassocieerde hypertensie en de complicaties daarvan.
Bronvermelding: Choi, Y.K., Lee, DK., Park, M. et al. The REDD1–NF-κB–miRNAs–eNOS/SIRT1 axis mediates obesity-induced endothelial cell senescence and hypertension. Nat Commun 17, 3843 (2026). https://doi.org/10.1038/s41467-026-70601-1
Trefwoorden: obesitas, endotheliale veroudering, hypertensie, microRNA, stikstofoxide