Clear Sky Science · pl
Oś REDD1–NF-κB–miRNA–eNOS/SIRT1 pośredniczy w starzeniu komórek śródbłonka i nadciśnieniu wywołanym otyłością
Dlaczego naczynia krwionośne szybciej się starzeją przy otyłości
Otyłość jest dobrze znana z podnoszenia ryzyka nadciśnienia, zawałów serca i udarów, ale mechanizmy, dzięki którym nadmiar tkanki tłuszczowej powoduje usztywnienie i przedwczesne starzenie naczyń, pozostawały niejasne. To badanie odkrywa molekularną „rozmowę” w cienkiej warstwie komórek wyściełających tętnice, pokazując, jak stres metaboliczny związany z otyłością może przedwcześnie postarzać te komórki, uszkadzać nerki i prowadzić do nadciśnienia. Zrozumienie tego łańcucha wydarzeń wskazuje nowe, bardzo precyzyjne cele dla leków, które mogłyby chronić naczynia u osób z otyłością.
Ukryte obciążenie komórek wyściełających naczynia
Najbardziej wewnętrzna warstwa naczyń krwionośnych zbudowana jest z komórek śródbłonka, które pełnią rolę strażników przepływu krwi, rozkurczu naczyń i reakcji zapalnej. W otyłości we krwi rośnie poziom kwasów tłuszczowych, cholesterolu, glukozy i sygnałów przypominających hormony. Autorzy karmili myszy dietą wysokotłuszczową, aby naśladować ten stan, i traktowali ludzkie komórki śródbłonka czynnikami związanymi z otyłością, takimi jak kwas palmitynowy, utlenione LDL, wysoka glukoza, leptyna i rezystyna. Te warunki powodowały u komórek klasyczne cechy senescencji — stan trwałego zatrzymania podziałów, gromadzenia odpadów i uwalniania substancji zapalnych. U myszy aorta — główna tętnica wychodząca z serca — rozwijała ogniska postarzałych komórek śródbłonka i traciła zdolność właściwego rozkurczu, co przyczyniało się do wzrostu ciśnienia krwi.
Czujnik stresu, który przesuwa komórki w stronę starości
Zespół skupił się na białku reagującym na stres, zwanym REDD1, aktywowanym przez stres metaboliczny i oksydacyjny. Stwierdzili, że czynniki metaboliczne silnie zwiększały poziom REDD1 w hodowanych ludzkich i mysich komórkach śródbłonka oraz w tętnicach myszy z otyłością. Gdy REDD1 był eksperymentalnie nadmiernie wyrażany w naczyniach, komórki śródbłonka szybko stawały się senescentne, produkcja tlenku azotu spadała, a tętnice usztywniały się, prowadząc do nadciśnienia. Przeciwnie, mutant REDD1 niezdolny do przekazywania sygnału przez kluczową ścieżkę zapalną nie wywoływał tych zaburzeń. Myszy pozbawione REDD1 lub pozbawione REDD1 specyficznie w komórkach śródbłonka były w dużej mierze chronione: ich tętnice miały mniej komórek senescentnych, wyższe poziomy molekuł ochronnych, lepszy rozkurcz naczyń i niższe ciśnienie krwi pomimo otyłości.
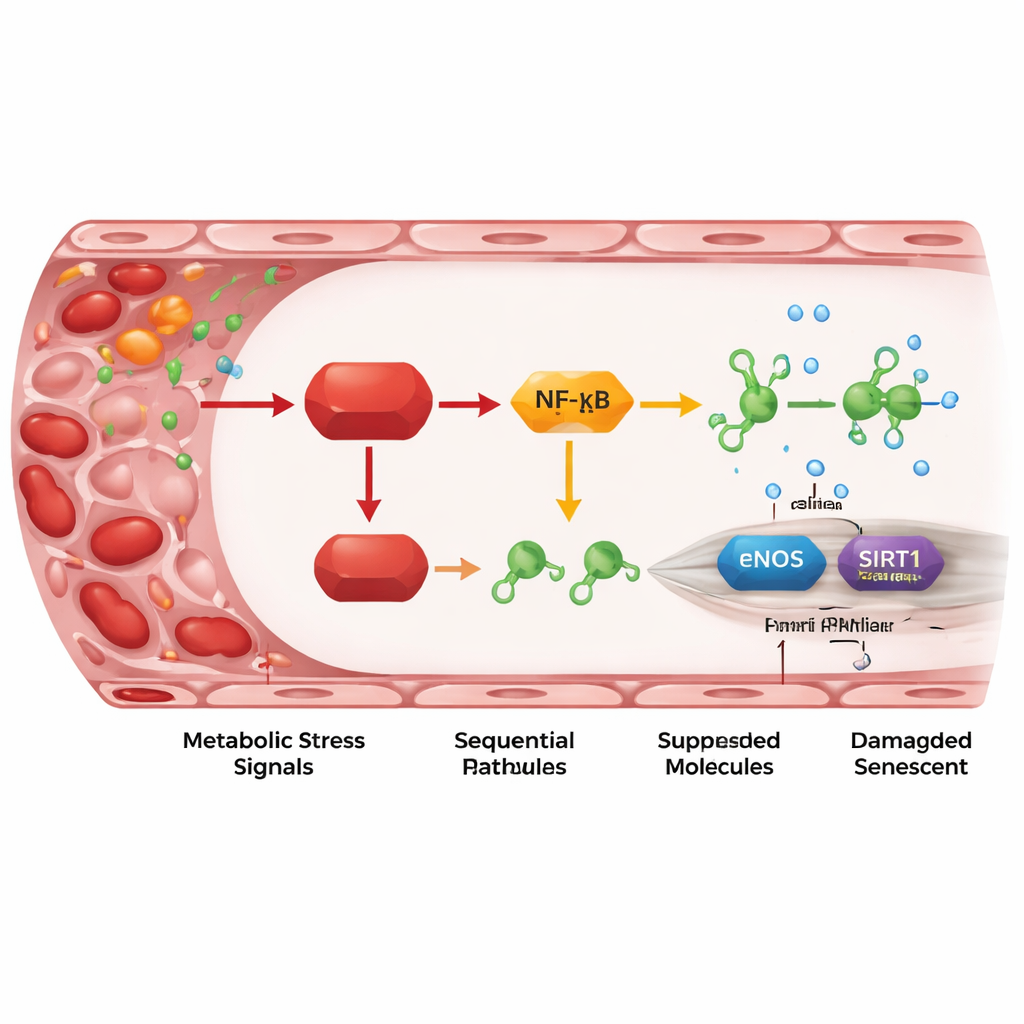
Zapalne przekaźnictwo od REDD1 do genów ochronnych
Pogłębiając analizę, badacze określili kaskadę molekularnych kroków łączących REDD1 z uszkodzeniem naczyń. REDD1 aktywuje „atypową” wersję szlaku NF-κB, głównego regulatora zapalenia. To z kolei podnosi poziomy dwóch małych regulatorowych RNA, miR-155-5p i w szczególności miR-214-3p. Te mikroRNA pełnią rolę małych hamulców dla dwóch ochronnych białek w komórkach śródbłonka: eNOS, które wytwarza tlenek azotu rozkurczający naczynia, oraz SIRT1, które pomaga zachować młodość komórkową i stabilność DNA. Gdy REDD1 był wysoki, poziomy mikroRNA rosły, eNOS i SIRT1 spadały, produkcja tlenku azotu malała, a markery senescencji wzrastały. Blokowanie mikroRNA lub zwiększanie SIRT1 bądź tlenku azotu mogło odwrócić znaczną część uszkodzeń, pokazując, że ta oś nie jest jedynie związana z procesem starzenia, lecz faktycznie go napędza.
Dowody z modeli genetycznych i wpływ na nerki
Kilka modeli mysich pozwoliło autorom przetestować każdy krok tej osi u żywych zwierząt. Myszy otyłe pozbawione REDD1, exprimujące niemogący przekazywać sygnału mutant REDD1 lub zaprojektowane tak, by usuwać REDD1 wyłącznie w komórkach śródbłonka, wykazywały zmniejszone starzenie tętnic i niższe ciśnienie krwi. Myszy pozbawione miR-214-3p były podobnie chronione: choć REDD1 nadal wzrastał przy otyłości, eNOS i SIRT1 pozostawały na wyższych poziomach, sygnalizacja tlenku azotu była lepiej zachowana, a starzenie naczyń i nadciśnienie były osłabione. Ta sama ścieżka REDD1–mikroRNA wpływała na nerki, organy kluczowe dla długoterminowej kontroli ciśnienia. U otyłych myszy typu dzikiego nerki powiększały się, stawały się włókniste i przepuszczały więcej kreatyniny do krwi. Objawy uszkodzenia nerek były znacznie łagodniejsze u myszy pozbawionych REDD1, pozbawionych REDD1 w śródbłonku lub pozbawionych miR-214-3p, co sugeruje, że ochrona naczyń przyczynia się również do zabezpieczenia funkcji nerek.
Co to oznacza dla przyszłych terapii
Dla obserwatora niebędącego specjalistą ta praca pokazuje, że otyłość nie tylko podnosi ciśnienie krwi przez większą masę ciała; przeprogramowuje biologię wyściółki naczyń na głębokim poziomie. Badanie identyfikuje kluczowy łańcuch sprawców — REDD1, atypowe sygnalizowanie NF-κB oraz mikroRNA miR-155-5p i miR-214-3p — które wspólnie wyłączają ochronne eNOS i SIRT1, powodując przyspieszone starzenie naczyń i nerek oraz wzrost ciśnienia krwi. Ponieważ każdy element tej osi można zmienić u myszy, by przywrócić zdrowsze naczynia nawet po rozwoju otyłości, oś REDD1–NF-κB–mikroRNA–eNOS/SIRT1 wyłania się jako obiecujący schemat dla leków mających zapobiegać lub leczyć nadciśnienie związane z otyłością i jej powikłania.
Cytowanie: Choi, Y.K., Lee, DK., Park, M. et al. The REDD1–NF-κB–miRNAs–eNOS/SIRT1 axis mediates obesity-induced endothelial cell senescence and hypertension. Nat Commun 17, 3843 (2026). https://doi.org/10.1038/s41467-026-70601-1
Słowa kluczowe: otyłość, starzenie śródbłonka, nadciśnienie, mikroRNA, tlenek azotu