Clear Sky Science · it
L’asse REDD1–NF-κB–miRNA–eNOS/SIRT1 media la senescenza delle cellule endoteliali e l’ipertensione indotte dall’obesità
Perché i nostri vasi sanguigni invecchiano più rapidamente con l’obesità
L’obesità è nota per aumentare il rischio di ipertensione, infarti e ictus, ma il modo preciso in cui l’eccesso di grasso rende i vasi sanguigni rigidi e “vecchi” è rimasto poco chiaro. Questo studio svela una “conversazione” molecolare all’interno del sottile strato cellulare che riveste le arterie, mostrando come lo stress metabolico dell’obesità possa invecchiare prematuramente queste cellule, danneggiare i reni e promuovere l’ipertensione. Comprendere questa catena di eventi indica nuovi bersagli molto specifici per farmaci che potrebbero proteggere i vasi nelle persone con obesità.
La pressione nascosta sulle cellule del rivestimento vascolare
Il rivestimento più interno dei vasi è formato dalle cellule endoteliali, che regolano il flusso ematico, il rilassamento vascolare e l’infiammazione. Nell’obesità aumentano nel sangue livelli di acidi grassi, colesterolo, zucchero e segnali ormonali. Gli autori hanno nutrito topi con una dieta ricca di grassi per ricreare questo stato e hanno trattato cellule endoteliali umane con fattori correlati all’obesità come acido palmitico, LDL ossidate, elevata glicemia, leptina e resistina. Queste condizioni hanno indotto nelle cellule i segni classici della senescenza, uno stato di arresto permanente in cui le cellule smettono di dividersi, accumulano scarti e rilasciano sostanze infiammatorie. Nei topi, l’aorta — l’arteria principale che esce dal cuore — ha sviluppato aree di cellule endoteliali invecchiate e ha perso la capacità di rilassarsi adeguatamente, contribuendo all’aumento della pressione sanguigna.
Un sensore di stress che spinge le cellule verso l’invecchiamento
Il team si è concentrato su una proteina sensibile allo stress chiamata REDD1, attivata dallo stress metabolico e ossidativo. Hanno osservato che i fattori di rischio metabolici aumentavano fortemente i livelli di REDD1 in cellule endoteliali umane e murine coltivate e nelle arterie di topi obesi. Quando REDD1 veniva aumentato sperimentalmente nei vasi, le cellule endoteliali diventavano rapidamente senescenti, la produzione di ossido nitrico diminuiva e le arterie si irrigidivano, promuovendo l’ipertensione. Al contrario, una forma mutante di REDD1 che non poteva più segnalare attraverso una via infiammatoria chiave non provocava questi effetti. Topi privi di REDD1, o privi di REDD1 specificamente nelle cellule endoteliali, risultavano in gran parte protetti: le loro arterie mostravano meno cellule senescenti, livelli più alti di molecole protettive, migliore rilassamento vascolare e pressione sanguigna inferiore nonostante l’obesità.
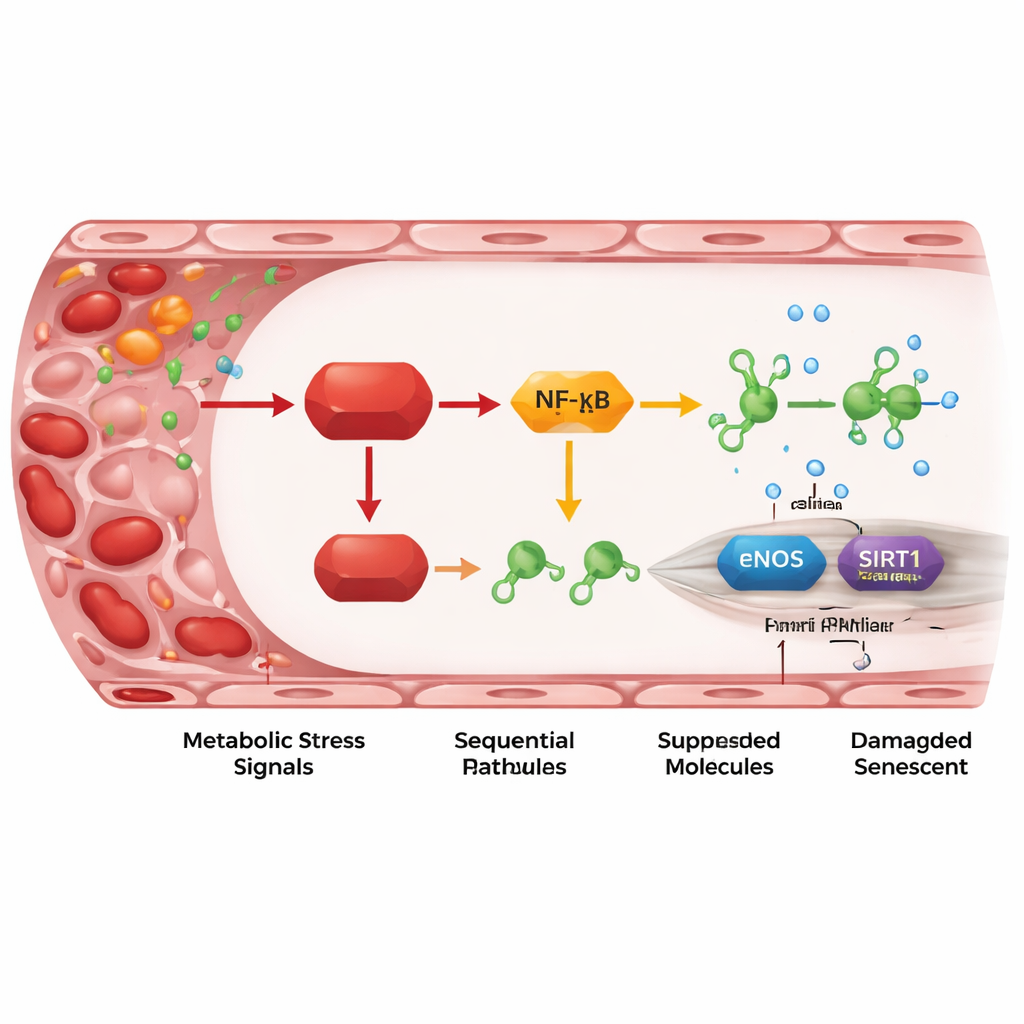
Un rilè infiammatorio da REDD1 ai geni protettivi
Approfondendo, i ricercatori hanno mappato una catena di passaggi molecolari che collegano REDD1 al danno vascolare. REDD1 attiva una versione “atipica” della via NF-κB, un regolatore principale dell’infiammazione. Questa attivazione aumenta a sua volta i livelli di due piccoli RNA regolatori, miR-155-5p e in particolare miR-214-3p. Questi microRNA agiscono come freni su due proteine protettive nelle cellule endoteliali: eNOS, che produce ossido nitrico per il rilassamento vascolare, e SIRT1, che contribuisce a mantenere la giovinezza cellulare e la stabilità del DNA. Quando REDD1 era elevato, aumentavano i microRNA, diminuivano eNOS e SIRT1, calava la produzione di ossido nitrico e aumentavano i marcatori di senescenza. Bloccare i microRNA o potenziare SIRT1 o l’ossido nitrico poteva invertire gran parte del danno, dimostrando che questo asse non è solo associato ma guida effettivamente il processo di invecchiamento nella parete vascolare.
Prove da modelli genetici ed effetti renali
Diversi modelli murini hanno permesso agli autori di testare ogni passaggio di questo asse negli animali vivi. Topi obesi privi di REDD1, che esprimevano il mutante REDD1 non segnalante, o ingegnerizzati per eliminare REDD1 solo nelle cellule endoteliali mostravano tutti ridotto invecchiamento arterioso e pressione più bassa. Topi privi di miR-214-3p erano protetti in modo simile: sebbene REDD1 aumentasse ancora con l’obesità, eNOS e SIRT1 restavano più elevati, la segnalazione dell’ossido nitrico era meglio preservata e la senescenza vascolare e l’ipertensione erano attenuate. Lo stesso asse REDD1–microRNA interessava i reni, organi cruciali per il controllo a lungo termine della pressione arteriosa. Nei topi obesi di tipo selvatico, i reni si ingrossavano, diventavano fibrotici e rilasciavano più creatinina nel sangue. Questi segni di danno renale erano molto più lievi nei topi privi di REDD1, privi di REDD1 endoteliale o privi di miR-214-3p, suggerendo che proteggere i vasi aiutava anche a salvaguardare la funzione renale.
Cosa significa per le terapie future
Per un osservatore non esperto, questo lavoro dimostra che l’obesità non aumenta la pressione solo per l’aumento della massa corporea; essa riprogramma profondamente la biologia del rivestimento vascolare. Lo studio identifica una catena chiave di colpevoli — REDD1, la segnalazione atipica di NF-κB e i microRNA miR-155-5p e miR-214-3p — che insieme spengono eNOS e SIRT1 protettivi, facendo invecchiare più rapidamente vasi e reni e innalzando la pressione arteriosa. Poiché ogni anello di questa catena può essere alterato nei topi per ripristinare vasi più sani anche dopo l’instaurarsi dell’obesità, l’asse REDD1–NF-κB–microRNA–eNOS/SIRT1 emerge come un progetto promettente per farmaci mirati a prevenire o trattare l’ipertensione associata all’obesità e le sue complicanze.
Citazione: Choi, Y.K., Lee, DK., Park, M. et al. The REDD1–NF-κB–miRNAs–eNOS/SIRT1 axis mediates obesity-induced endothelial cell senescence and hypertension. Nat Commun 17, 3843 (2026). https://doi.org/10.1038/s41467-026-70601-1
Parole chiave: obesità, senescenza endoteliale, ipertensione, microRNA, ossido nitrico