Clear Sky Science · es
El eje REDD1–NF-κB–miARNs–eNOS/SIRT1 media la senescencia de las células endoteliales inducida por la obesidad y la hipertensión
Por qué nuestros vasos sanguíneos envejecen más rápido con la obesidad
La obesidad se conoce por aumentar el riesgo de hipertensión, infartos y accidentes cerebrovasculares, pero cómo el exceso de grasa envejece y endurece los vasos sanguíneos no estaba del todo claro. Este estudio revela una "conversación" molecular dentro de la delgada capa celular que recubre las arterias, mostrando cómo el estrés metabólico de la obesidad puede envejecer prematuramente estas células, dañar los riñones y provocar hipertensión. Comprender esta cadena de acontecimientos señala objetivos muy concretos para fármacos que podrían proteger los vasos en personas con obesidad.
La tensión oculta sobre las células del revestimiento vascular
El revestimiento más interno de los vasos sanguíneos está formado por células endoteliales, que funcionan como guardianes del flujo sanguíneo, la relajación vascular y la inflamación. En la obesidad, aumentan en la sangre los niveles de ácidos grasos, colesterol, azúcar y señales hormonales. Los autores alimentaron ratones con una dieta alta en grasas para imitar este estado y trataron células endoteliales humanas con factores relacionados con la obesidad como ácido palmítico, LDL oxidadas, glucosa alta, leptina y resistina. Estas condiciones hicieron que las células mostraran signos clásicos de senescencia, un estado de detención permanente en el que las células dejan de dividirse, acumulan desechos y liberan sustancias inflamatorias. En los ratones, la aorta —la arteria principal que sale del corazón— desarrolló parches de células endoteliales envejecidas y perdió su capacidad de relajarse adecuadamente, contribuyendo al aumento de la presión arterial.
Un sensor de estrés que inclina a las células hacia la vejez
El equipo se centró en una proteína sensible al estrés llamada REDD1, que se activa por estrés metabólico y oxidativo. Encontraron que los factores de riesgo metabólico aumentaban fuertemente los niveles de REDD1 en células endoteliales humanas y murinas cultivadas y en las arterias de ratones obesos. Cuando REDD1 se incrementó experimentalmente en los vasos, las células endoteliales se volvieron rápidamente senescentes, la producción de óxido nítrico cayó y las arterias se endurecieron, lo que impulsó la hipertensión. En contraste, una forma mutante de REDD1 que ya no podía señalizar a través de una vía inflamatoria clave no provocó estos problemas. Los ratones genéticamente privados de REDD1, o sin REDD1 específicamente en sus células endoteliales, estuvieron en gran medida protegidos: sus arterias mostraron menos células senescentes, niveles más altos de moléculas protectoras, mejor relajación vascular y presión arterial más baja a pesar de la obesidad.
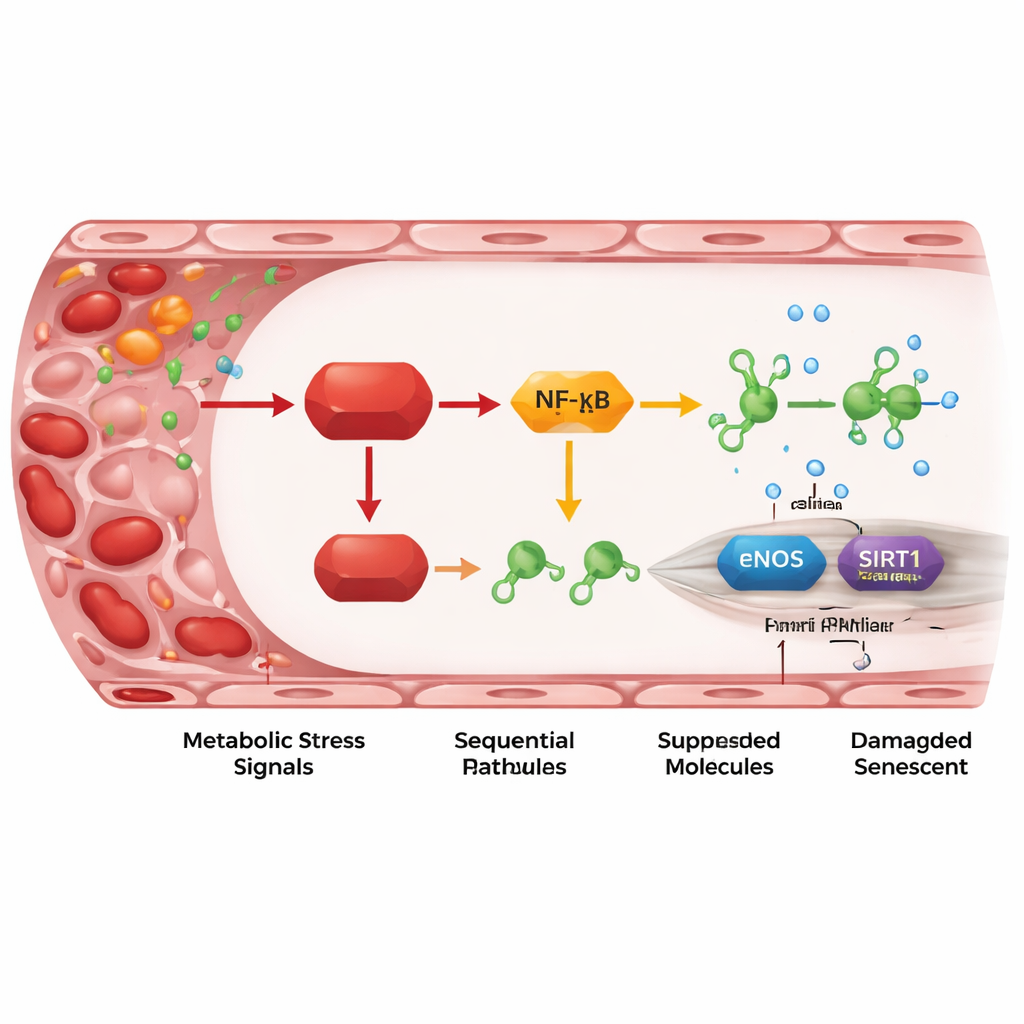
Un relevo inflamatorio de REDD1 hacia genes protectores
Al profundizar, los investigadores delinearon una secuencia de pasos moleculares que conecta REDD1 con el daño vascular. REDD1 activa una versión "atípica" de la vía NF-κB, un regulador maestro de la inflamación. Esto, a su vez, eleva los niveles de dos pequeños ARN regulatorios, miR-155-5p y especialmente miR-214-3p. Estos microARN actúan como frenos diminutos sobre dos proteínas protectoras en las células endoteliales: eNOS, que produce óxido nítrico para relajar los vasos, y SIRT1, que contribuye a mantener la juventud celular y la estabilidad del ADN. Cuando REDD1 era alto, aumentaban los microARN, disminuían eNOS y SIRT1, la producción de óxido nítrico declinaba y aumentaban los marcadores de senescencia. Bloquear los microARN o aumentar SIRT1 u óxido nítrico pudo revertir gran parte del daño, mostrando que este eje no solo está asociado, sino que en realidad impulsa el proceso de envejecimiento en la pared vascular.
Pruebas a partir de modelos genéticos y efectos renales
Varios modelos de ratón permitieron a los autores probar cada paso de este eje en animales vivos. Los ratones obesos que carecían de REDD1, expresaban el mutante REDD1 no señalizador o estaban diseñados para eliminar REDD1 únicamente en células endoteliales mostraron todos un envejecimiento arterial reducido y presión arterial más baja. Los ratones que carecían de miR-214-3p estuvieron protegidos de forma similar: aunque REDD1 seguía elevándose con la obesidad, eNOS y SIRT1 se mantenían más altos, la señalización del óxido nítrico se preservaba mejor y la senescencia vascular y la hipertensión se atenuaban. La misma vía REDD1–microARN afectó a los riñones, órganos cruciales para el control a largo plazo de la presión arterial. En ratones obesos de tipo salvaje, los riñones se agrandaron, se volvieron fibróticos y filtraron más creatinina hacia la sangre. Estos signos de daño renal fueron mucho más leves en ratones sin REDD1, sin REDD1 endotelial o sin miR-214-3p, lo que sugiere que proteger los vasos también ayudó a salvaguardar la función renal.
Qué significa esto para terapias futuras
Para un observador no especializado, este trabajo muestra que la obesidad no solo eleva la presión arterial por el exceso de masa corporal; reprograma la biología del revestimiento vascular a un nivel profundo. El estudio identifica una cadena clave de culpables —REDD1, la señalización atípica de NF-κB y los microARN miR-155-5p y miR-214-3p— que juntos silencian a eNOS y SIRT1 protectores, provocando que vasos y riñones envejezcan más rápido y aumente la presión arterial. Dado que cada eslabón de esta cadena puede alterarse en ratones para restaurar vasos más saludables incluso después de establecida la obesidad, el eje REDD1–NF-κB–microARN–eNOS/SIRT1 emerge como un plano prometedor para fármacos destinados a prevenir o tratar la hipertensión vinculada a la obesidad y sus complicaciones.
Cita: Choi, Y.K., Lee, DK., Park, M. et al. The REDD1–NF-κB–miRNAs–eNOS/SIRT1 axis mediates obesity-induced endothelial cell senescence and hypertension. Nat Commun 17, 3843 (2026). https://doi.org/10.1038/s41467-026-70601-1
Palabras clave: obesidad, senescencia endotelial, hipertensión, microARN, óxido nítrico