Clear Sky Science · de
Die REDD1–NF-κB–miRNAs–eNOS/SIRT1-Achse vermittelt adipositasbedingte Endothelzell-Seneszenz und Bluthochdruck
Warum unsere Blutgefäße bei Adipositas schneller altern
Adipositas ist dafür bekannt, das Risiko für Bluthochdruck, Herzinfarkte und Schlaganfälle zu erhöhen, doch wie überschüssiges Fett die Blutgefäße genau vorzeitig alt und starr macht, blieb bislang unklar. Diese Studie enthüllt eine molekulare "Unterhaltung" innerhalb der dünnen Zellschicht, die unsere Arterien auskleidet, und zeigt, wie metabolischer Stress durch Adipositas diese Zellen vorzeitig altern lassen, die Nieren schädigen und Bluthochdruck verursachen kann. Das Verständnis dieser Ereigniskette weist auf neue, sehr spezifische Angriffspunkte für Medikamente hin, die die Gefäße bei Menschen mit Adipositas schützen könnten.
Die verborgene Belastung der Gefäßinnenhaut
Die innerste Auskleidung der Blutgefäße besteht aus Endothelzellen, die als Torwächter für Blutfluss, Gefäßentspannung und Entzündungsreaktionen fungieren. Bei Adipositas steigen Fettsäuren, Cholesterin, Zucker und hormonähnliche Signale im Blut an. Die Autoren fütterten Mäuse mit einer fettreichen Diät, um diesen Zustand nachzuahmen, und behandelten menschliche Endothelzellen mit adipositasassoziierten Faktoren wie Palmitinsäure, oxidiertem LDL, hohem Glukosegehalt, Leptin und Resistin. Diese Bedingungen führten dazu, dass die Zellen klassische Zeichen der Seneszenz zeigten — einem Zustand permanenter Zellzyklusstillation, in dem Zellen nicht mehr teilen, Abfallstoffe ansammeln und entzündungsfördernde Substanzen freisetzen. Bei den Mäusen bildete die Aorta — die Hauptschlagader des Herzens — herdförmige Bereiche gealterter Endothelzellen und verlor ihre Fähigkeit, sich richtig zu entspannen, was zum Anstieg des Blutdrucks beitrug.
Ein Stresssensor, der Zellen ins Alter kippen lässt
Das Team konzentrierte sich auf ein stressreaktives Protein namens REDD1, das durch metabolischen und oxidativen Stress aktiviert wird. Sie fanden, dass metabolische Risikofaktoren die REDD1-Spiegel in kultivierten menschlichen und murinen Endothelzellen sowie in den Arterien adipöser Mäuse deutlich erhöhten. Wurde REDD1 experimentell in Gefäßen hochreguliert, wurden Endothelzellen schnell seneszent, die Produktion von Stickstoffmonoxid sank und die Arterien versteiften sich, was Bluthochdruck vorantrieb. Im Gegensatz dazu konnte eine mutierte Form von REDD1, die nicht mehr über einen wichtigen Entzündungsweg signalisiert, diese Probleme nicht verursachen. Mäuse, denen REDD1 genetisch fehlte, oder denen REDD1 spezifisch in Endothelzellen fehlte, waren weitgehend geschützt: Ihre Arterien wiesen weniger seneszente Zellen, höhere Spiegel schützender Moleküle, bessere Gefäßentspannung und einen niedrigeren Blutdruck trotz Adipositas auf.
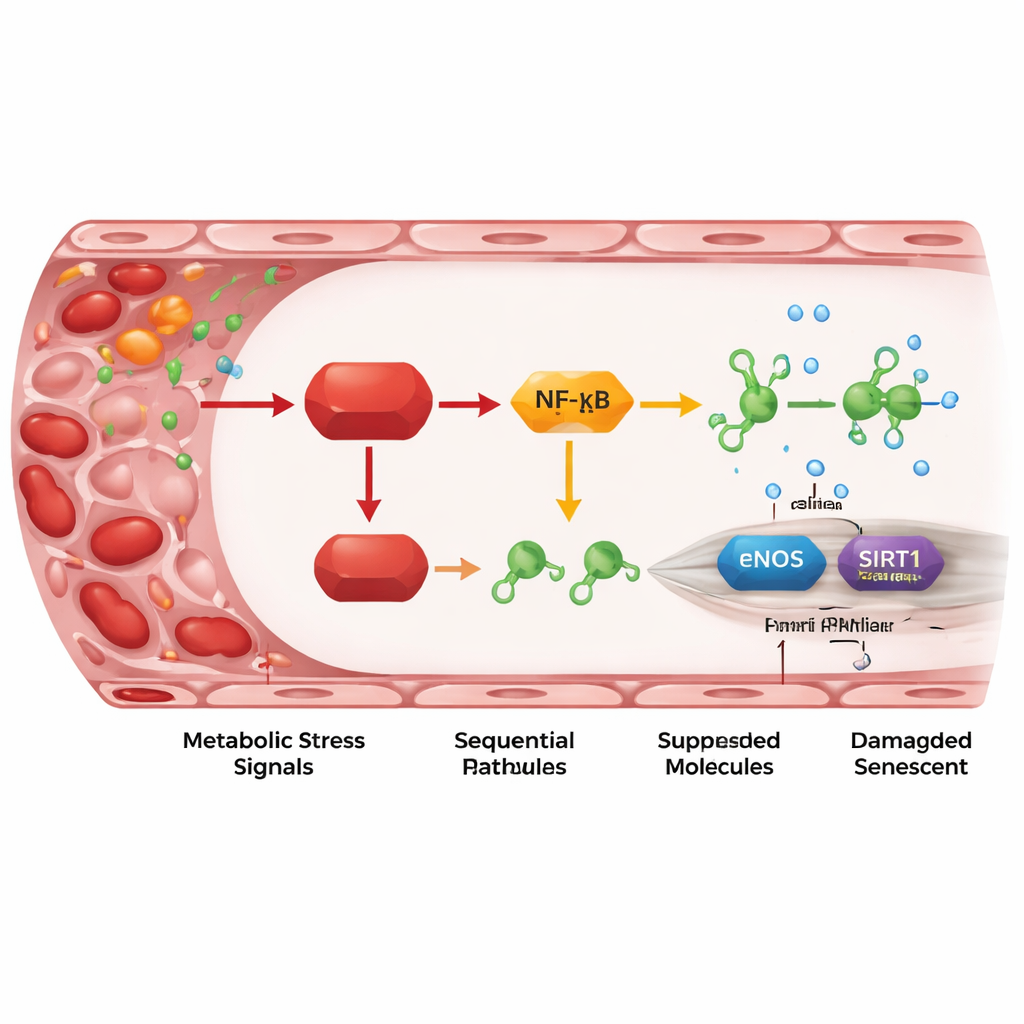
Ein entzündliches Staffelspiel von REDD1 zu schützenden Genen
Bei tieferer Untersuchung kartierten die Forschenden eine Abfolge molekularer Schritte, die REDD1 mit vaskulären Schäden verbindet. REDD1 aktiviert eine "atypische" Variante des NF-κB-Signalwegs, eines Hauptreglers der Entzündung. Dies wiederum erhöht die Spiegel zweier kleiner regulatorischer RNAs, miR-155-5p und insbesondere miR-214-3p. Diese MicroRNAs wirken als winzige Bremsen auf zwei schützende Proteine in Endothelzellen: eNOS, das Stickstoffmonoxid zur Gefäßentspannung produziert, und SIRT1, das zur Erhaltung der zellulären Jugendlichkeit und der DNA-Stabilität beiträgt. Wenn REDD1 erhöht war, stiegen die MicroRNA-Spiegel, eNOS- und SIRT1-Spiegel sanken, die Stickstoffmonoxidproduktion nahm ab und Seneszenzmarker stiegen. Das Blockieren der MicroRNAs oder das Hochregulieren von SIRT1 oder Stickstoffmonoxid konnte viele der Schäden umkehren, was zeigt, dass diese Achse nicht nur korreliert, sondern tatsächlich den Alterungsprozess in der Gefäßwand antreibt.
Belege aus genetischen Modellen und Nierenfolgen
Mehrere Mäusemodelle ermöglichten es den Autoren, jeden Schritt dieser Achse in lebenden Tieren zu prüfen. Adipöse Mäuse ohne REDD1, mit der nicht signalgebenden REDD1-Mutation oder mit gezieltem Endothel-REDD1-Knockout zeigten alle reduzierte arterielle Alterung und niedrigeren Blutdruck. Mäuse, denen miR-214-3p fehlte, waren ähnlich geschützt: Obwohl REDD1 bei Adipositas weiterhin anstieg, blieben eNOS und SIRT1 höher, die Stickstoffmonoxid-Signalgebung war besser erhalten und vaskuläre Seneszenz sowie Hypertonie waren abgeschwächt. Derselbe REDD1–MicroRNA-Weg beeinflusste auch die Nieren, Organe, die für die langfristige Blutdruckregulation entscheidend sind. Bei adipösen Wildtyp-Mäusen vergrößerten sich die Nieren, entwickelten Fibrose und ließen mehr Kreatinin ins Blut übertreten. Diese Anzeichen renaler Schäden waren bei Mäusen, denen REDD1 fehlte, bei Mäusen ohne endotheliales REDD1 oder bei Mäusen ohne miR-214-3p deutlich milder, was darauf hindeutet, dass der Schutz der Gefäße auch die Nierenfunktion bewahrt.
Was das für zukünftige Therapien bedeutet
Für den Laien zeigt diese Arbeit, dass Adipositas den Blutdruck nicht einfach durch zusätzliches Körpergewicht erhöht; sie programmiert die Biologie der Gefäßinnenhaut in einem tiefgreifenden Ausmaß um. Die Studie identifiziert eine Schlüsselreihe von Schuldigen — REDD1, atypische NF-κB-Signalgebung und die MicroRNAs miR-155-5p und miR-214-3p — die gemeinsam schützende eNOS und SIRT1 ausschalten, wodurch Blutgefäße und Nieren schneller altern und der Blutdruck steigt. Da jede Verbindung in dieser Kette bei Mäusen so verändert werden kann, dass gesundere Gefäße selbst nach dem Auftreten von Adipositas wiederhergestellt werden, zeichnet sich die REDD1–NF-κB–MicroRNA–eNOS/SIRT1-Achse als vielversprechende Vorlage für Medikamente ab, die darauf abzielen, adipositasbedingten Bluthochdruck und seine Komplikationen zu verhindern oder zu behandeln.
Zitation: Choi, Y.K., Lee, DK., Park, M. et al. The REDD1–NF-κB–miRNAs–eNOS/SIRT1 axis mediates obesity-induced endothelial cell senescence and hypertension. Nat Commun 17, 3843 (2026). https://doi.org/10.1038/s41467-026-70601-1
Schlüsselwörter: Adipositas, Endotheliale Seneszenz, Hypertonie, MicroRNA, Stickstoffmonoxid