Clear Sky Science · he
ציר REDD1–NF-κB–miRNAs–eNOS/SIRT1 מתווך הזדקנות תאי אנדותל ולחץ דם שנגרמים על ידי השמנת יתר
מדוע כלי הדם שלנו מזדקנים מהר יותר בהשמנה
ידוע שהשמנה מעלה את הסיכון ליתר לחץ דם, התקפי לב ושבץ, אך כיצד עודף שומן מזדקן ומקשיח את כלי הדם נותר עניין מעורפל. המחקר הזה חושף "שיחה" מולקולרית בתוך השכבה הדקה שמצפה את העורקים שלנו, ומראה כיצד עומס מטבולי מהשמנה יכול להזדקן את התאים הללו בטרם עת, לפגוע בכליות ולהניע יתר לחץ דם. הבנת שרשרת האירועים הזו מצביעה על מטרות תרופתיות חדשות ומדויקות שעשויות להגן על כלי הדם אצל אנשים עם השמנת יתר.
העומס החבוי על תאי ציפוי הכלי
השכבה הפנימית של כלי הדם מורכבת מתאים אנדותליים, שפועלים כשומרי סף לזרימת הדם, להרפיית כלי הדם ולדלקת. בהשמנה עולים בדם רמות חומצות שומן, כולסטרול, סוכר ואיתותים הורמונליים. החוקרים האכילו עכברים בדיאטה עתירת שומן כדי לדמות מצב זה וטיפלו בתאי אנדותל אנושיים בגורמים הקשורים להשמנה כמו חומצת פלמיטית, LDL מחומצן, גלוקוז גבוה, לפטין ורזיסטין. תנאים אלה גרמו לתאים להציג תופעות אופייניות של סנציה (senescence), מצב של עצירה קבועה שבו התאים מפסיקים להתחלק, מצטברים פסולת ומשחררים חומרים דלקתיים. בעכברים, האאורטה — העורק הראשי היוצא מהלב — פיתחה אזורים של תאים אנדותליים מזדקנים ואיבדה את היכולת להתרפות כראוי, מה שתרם לעלייה בלחץ הדם.
חיישן מתח שמטה תאים לעבר הזדקנות
הקבוצה התמקדה בחלבון מגיב-מתח שנקרא REDD1, שמופעל על ידי מתח מטבולי וחמצוני. הם גילו שגורמי סיכון מטבוליים הגבירו בעוצמה את רמות REDD1 בתאי אנדותל אנושיים ומאוישים במעבדה ובעורקים של עכברים שמנים. כאשר REDD1 הוגבר ניסויית בכלי הדם, תאי האנדותל הפכו במהירות לסנצנטיים, ייצור החנקן החנקני ירד, והעורקים התקשו — מה שהניע יתר לחץ דם. לעומת זאת, צורת מוטנטית של REDD1 שלא יכלה עוד לאות דרך מסלול דלקתי מפתח לא גרמה לבעיות הללו. עכברים חסרי REDD1 גנטית, או חסרי REDD1 באופן ספציפי בתאי האנדותל שלהם, היו מוגנים באופן ניכר: בעורקיהם נצפו פחות תאים מזדקנים, רמות מולקולות מגן גבוהות יותר, הרפיית כלי הדם השתפרה ולחץ הדם היה נמוך יותר למרות ההשמנה.
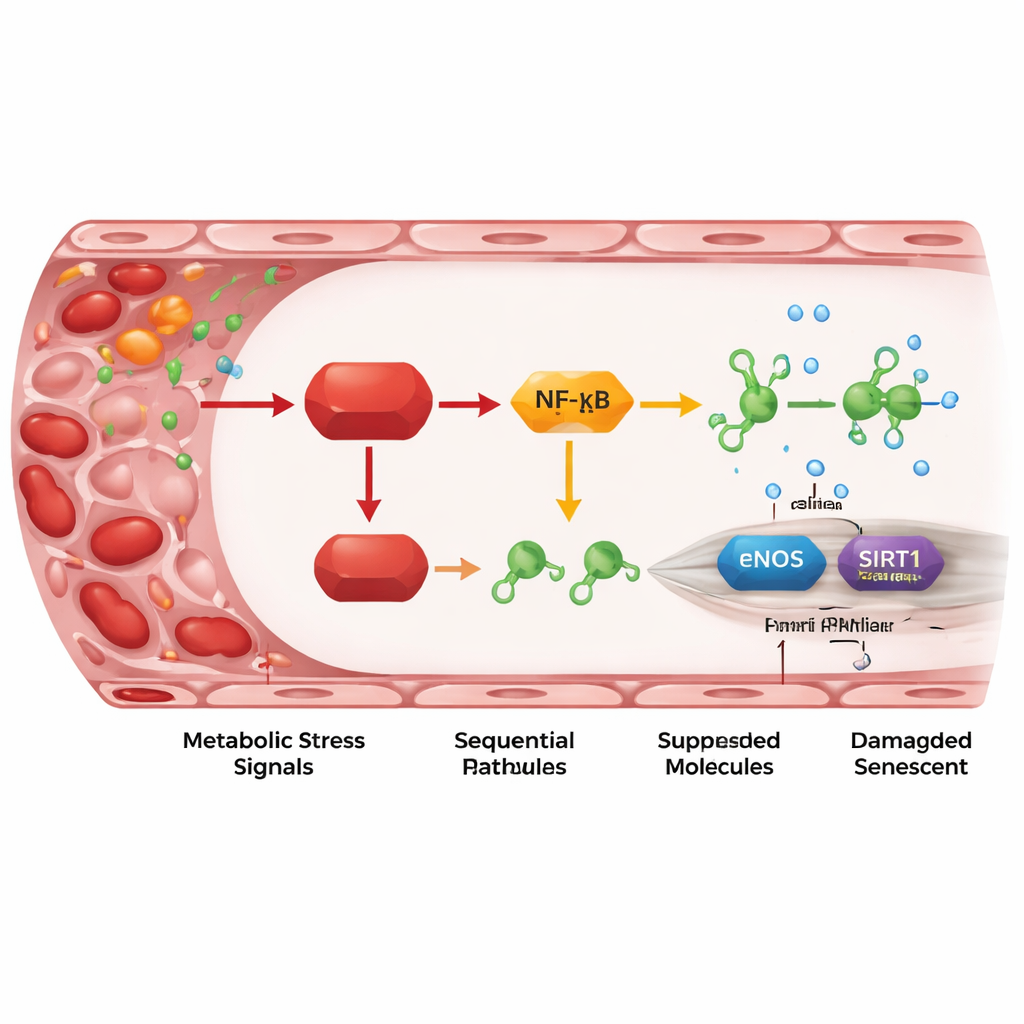
רקע דלקתי משולשל מ-REDD1 לגנים מגן
בחינה מעמיקה יותר חשפה רצף של צעדים מולקולריים שמקשרים את REDD1 לנזק הווסקולרי. REDD1 מפעיל גרסה "א-טיפוסית" של מסלול NF-κB, בקר עיקרי של דלקת. זה, בתורו, מעלה את רמותיהם של שני רנ״א קטנים מבוקרי-גנים, miR-155-5p ובפרט miR-214-3p. המיקרו-רנ״א האלה פועלים כבלמי־זעירים על שני חלבונים מגן בתאי האנדותל: eNOS, שמייצר חנקן חנקני להתרפות כלי הדם, ו-SIRT1, המסייע בשימור נעימות התאים ויציבות ה-DNA. כשה-REDD1 גבוה, רמות המיקרו-רנ״א עולות, רמות eNOS ו-SIRT1 יורדות, ייצור החנקן החנקני מצטמצם וסימני הסנcence עולים. חסימת המיקרו-רנ״א או הגברת SIRT1 או החנקן החנקני יכולה להפוך הרבה מהנזק, מה שמראה שהציר הזה אינו רק מקושר אלא אכן מוביל לתהליך ההזדקנות בדופן הכלי.
הוכחות ממודלים גנטיים והשפעות על הכליות
מספר מודלים של עכברים איפשרו למחברים לבדוק כל שלב בציר הזה בחיות חיות. עכברים שגם היו שמנים וגם חסרי REDD1, שהביעו את המוטנט הבלתי-מאותת של REDD1, או שעוצב בהם מחיקה של REDD1 רק בתאי האנדותל הראו כולם הזדקנות עורקית מופחתת ולחץ דם נמוך יותר. עכברים שחסרו את miR-214-3p הוגנו באופן דומה: אף על פי ש-REDD1 עדיין עלה עם ההשמנה, eNOS ו-SIRT1 נשארו ברמות גבוהות יותר, איתות החנקן החנקני נשמר טוב יותר, וההזדקנות הווסקולרית ויתר הלחץ דם הוקלו. אותו ציר REDD1–מיקרוRNA השפיע גם על הכליות, איברים קריטיים לשליטה ארוכת טווח על לחץ הדם. בעכברים שמנים בעלי רקע פראי, הכליות התנפחה, הפכו לפיברוטיות ודלפו יותר קריאטינין למחזור הדם. סימני נזק כלייתי אלה היו הרבה פחות חמורים בעכברים חסרי REDD1, חסרי REDD1 באנדותל, או חסרי miR-214-3p, מה שמרמז שהגנת כלי הדם גם סייעה לשמירה על תפקוד הכליות.
מה משמעות זה לטיפולים עתידיים
לצופה לא מומחה, עבודה זו מראה שהשמנה לא רק מעלה את לחץ הדם דרך מסת גוף עודפת; היא מתכנתת מחדש את הביולוגיה של שכבת הציפוי של כלי הדם ברמה עמוקה. המחקר מצביע על שרשרת חשודים מרכזית — REDD1, איתות NF-κB א-טיפוסי, והמיקרוRNAים miR-155-5p ו-miR-214-3p — שלבטח סוגרים את eNOS ו-SIRT1 המגנים, גורמים לכלי הדם והכליות להזדקן מהר יותר ומעלים את לחץ הדם. מאחר שכל גשר בשרשרת הזו ניתן לשינוי בעכברים כדי לשחזר כלי דם בריאים יותר אפילו לאחר הופעת ההשמנה, ציר REDD1–NF-κB–מיקרוRNA–eNOS/SIRT1 מתגבש כמתווה מבטיח לפיתוח תרופות שמטרתן למנוע או לטפל ביתר לחץ דם הקשור להשמנת יתר ובסיבוכיה.
ציטוט: Choi, Y.K., Lee, DK., Park, M. et al. The REDD1–NF-κB–miRNAs–eNOS/SIRT1 axis mediates obesity-induced endothelial cell senescence and hypertension. Nat Commun 17, 3843 (2026). https://doi.org/10.1038/s41467-026-70601-1
מילות מפתח: השמנת יתר, הזדקנות אנדותלית, יתר לחץ דם, מיקרוRNA, חמצן חנקני