Clear Sky Science · sv
TIGAR reglerar tarmens slemhinnes barriärintegritet genom att hämma laktylering av G6PD/6PGD vid ulcerös kolit
Varför tarmens slemmiga skydd är viktigt
Insidan av våra tarmar är täckt av ett halaktigt slemlager som håller biljoner mikrober på avstånd. Vid ulcerös kolit, en kronisk sjukdom som orsakar inflammation i tjocktarmen, blir detta skyddande skikt ofta tunnare eller bryts ner, vilket tillåter bakterier och irriterande ämnen att nå tarmväggen. Denna studie undersöker varför slembarriären sviktar, och spårar händelseförloppet från sockeromsättningen i specialiserade slembildande celler hela vägen till skador i tarmen — och lyfter fram en molekyl kallad TIGAR som ett lovande nytt mål för behandling.
En dold försvarare i tarmcellerna
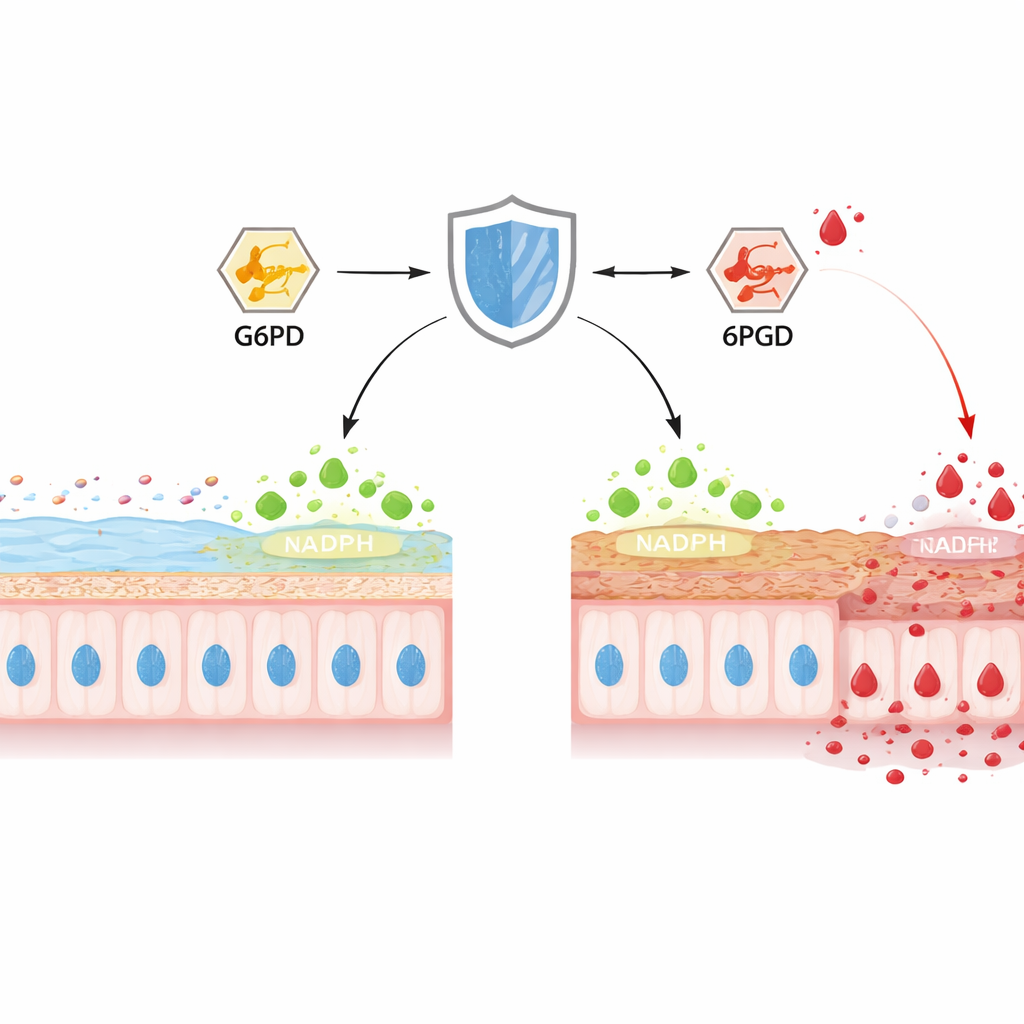
I tjocktarmen producerar gobletceller ständigt MUC2, det huvudsakliga slemproteinet som bildar det inre skyddande gelen. Författarna fokuserade på TIGAR, ett protein tidigare känt för att styra glukos in i en väg som bildar NADPH, en nyckelkomponent i cellens reduktionskraft som håller skadliga oxidationsmedel i schack. Hos möss med kemiskt framkallad kolit sjönk TIGAR-nivåerna i kolon över flera dagar, samtidigt som slemlagret tunnades ut, epitelytan eroderade och bakterier kom närmare vävnaden. När forskarna selektivt tog bort TIGAR enbart i tarmens epitel hos möss började koliten tidigare och blev allvarligare, med missformade kryptor, färre gobletceller och avsevärt mindre mogen MUC2. Mätningar av cellernas kemi visade uttömt NADPH, försvagade antioxidativa system och kraftiga ökningar av reaktiva syrer- och kvävearter, vilket kopplar förlusten av TIGAR till intensiv oxidativ stress och barriärsvikt.
Sockeranvändning omprogrammerad mot slösaktig förbränning
För att förstå hur TIGAR formar metabolismen profilerade teamet hundratals småmolekyler i goblet-liknande cellinjer och i mössens kolonvävnad. Att avlägsna TIGAR förändrade inte hur mycket glukos cellerna importerade eller hur snabbt hela djuren förbrukade syre, men det ändrade kraftigt glukosens öde. Med märkta sockerarter visade de att mindre kolflöde gick genom pentosfosfatvägen — huvudkällan till NADPH — medan mer trycktes in i klassisk glykolys och slutade som laktat. Två metaboliter stack ut: 6‑fosfoglukonat, ett nav i pentosfosfatvägen, ackumulerades kraftigt, och laktatnivåer ökade i celler och vävnader utan TIGAR, särskilt under kolit. Genuttrycksdata antydde att gener för glykolysens enzymer var uppreglerade, medan proteinnivåerna för två nyckelenzymer i pentosfosfatvägen, G6PD och 6PGD, var oförändrade, vilket tyder på att deras aktivitet — inte deras mängd — hämmas.
En kemisk märkning som avväpnar antioxidativa enzymer
Forskarna avslöjade sedan den blockerande mekanismen: laktylering, en kemisk märkning som läggs till proteiner med laktat som donator. I kolitmodeller och i inflammatoriska cellkulturer ökade den övergripande proteinlaktyleringen, och både G6PD och 6PGD bar höga nivåer av denna modifiering. Masspektrometri identifierade specifika lysinpositioner på varje enzym — K432 på G6PD och K38 på 6PGD — som huvudsakliga laktyleringsställen. Strukturell modellering och mutagene tester visade att modifiering av dessa platser stör hur G6PD bildar sin aktiva dimer och hur 6PGD binder sin kofaktor, vilket kraftigt minskar deras förmåga att generera NADPH. Att blockera laktatproduktion eller förhindra laktylering på dessa positioner återställde enzymaktivitet, ökade NADPH, sänkte oxidativ stress och förbättrade MUC2-mognad. I TIGAR‑defekta möss bevarade införande av muterade versioner av G6PD och 6PGD som inte kunde laktyleras slemkakans tjocklek och minskade bakterieintrång i det inre lagret.
Hur redoxobalans ställer till det för slemprocessing
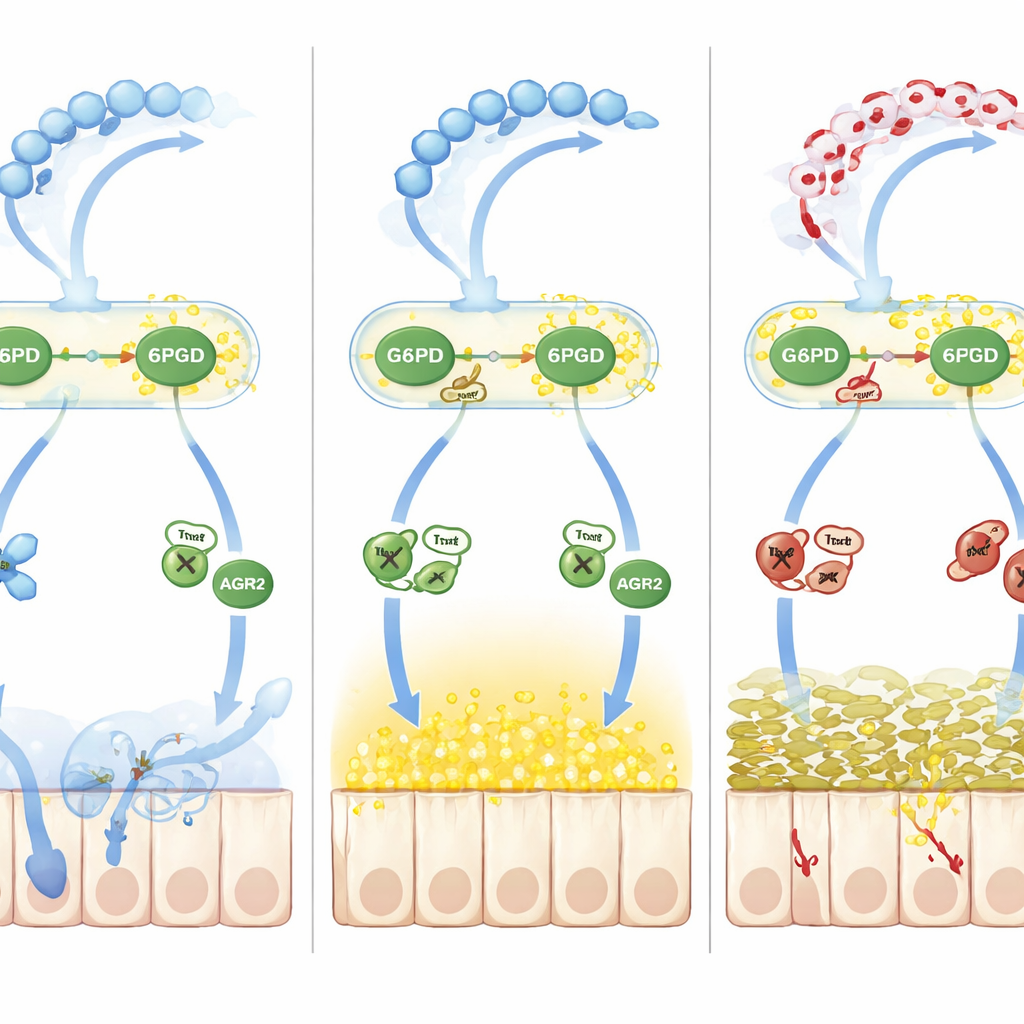
Utöver enkel oxidation spårade teamet en andra våg av skada driven av kväveoxid. Förhöjda nivåer av kväveoxid vid kolit ökade S‑nitrosylation, en annan reversibel kemisk märkning på cysteinrester. Ett veckningshjälpprotein kallat AGR2, viktigt för att omvandla MUC2‑prekursorer till deras mogna form i det endoplasmatiska retiklet, blev kraftigt S‑nitrosylerat vid en kritisk cystein (Cys81). Denna förändring försvagade AGR2:s bindning till MUC2‑prekursorer, vilket ledde till ansamling av felveckade proteiner och ökat endoplasmatiskt retikelstress, vilket ytterligare minskade mängden korrekt bildat slem. Den centrala mellanhanden var thioredoxin‑1 (Trx1), ett redoxkänsligt enzym som antingen kan ta bort eller överföra nitrosylgrupper beroende på sitt eget oxideringstillstånd. När NADPH var knappt eftersom G6PD och 6PGD var laktylerade och långsamma, skiftade Trx1 från ett skyddande denitrosylerande läge till ett skadligt transnitrosylerande läge, och förde nitrosylgrupper över på AGR2 och fördjupade slemdefekten.
Vad detta betyder för personer med kolit
Sammantaget skisserar arbetet en kedjereaktion: kronisk inflammation sänker TIGAR i tarmepitelceller; detta omdirigerar glukos bort från NADPH‑producerande vägar, ökar laktat och laktylerar G6PD och 6PGD; NADPH‑produktionen faller, Trx1 blir överoxiderat, AGR2 överdrivet nitrosylerat och MUC2 misslyckas med att mogna, vilket lämnar slembarriären tunn och läckande. För en lekman är budskapet att en subtil förändring i hur tarmceller förbränner socker kan översättas till ett mycket påtagligt brott i tarmens slemmiga skydd. Genom att skydda TIGAR‑funktionen, förhindra skadlig laktylering av G6PD och 6PGD, eller återbalansera Trx1‑ och AGR2‑kemin kan framtida behandlingar hjälpa till att stärka slembarriären och dämpa inflammationen vid ulcerös kolit.
Citering: Wu, D., Su, S., Zhang, P. et al. TIGAR regulates intestinal mucus barrier integrity by inhibiting lactylation of G6PD/6PGD in ulcerative colitis. Nat Commun 17, 3382 (2026). https://doi.org/10.1038/s41467-026-70263-z
Nyckelord: ulcerös kolit, intestinal slembarriär, TIGAR, oxidativ stress, glukosmetabolism