Clear Sky Science · he
TIGAR מסדיר את שלמות מחסום הריריות המעי על‑ידי עיכוב לקטילציה של G6PD/6PGD בדלקת כיבית של המעי הגס
למה המגן הרירי של המעיים חשוב
רירית המעי מכוסה בשכבת ריר חלקה ששומרת על טריליוני מיקרואורגניזמים במרחק יד. בדלקת כיבית של המעי הגס, מחלה כרונית שמוליכה לדלקת המעי, שכבה מגוננת זו לעיתים דקה או ניזוקה, מה שמאפשר לחיידקים ולחומרים מגרויים להגיע לקיר המעי. מחקר זה בוחן מדוע מחסום הריר נכשל, ועוקב אחרי הסיפור מתחום מטבוליזם הסוכר בתאים מתמחים המפרישים ריר ועד לפגיעה במעי — ומבליט מולקולה בשם TIGAR כמטרה מבטיחה לטיפול.
מגן חבוי בתאי המעי
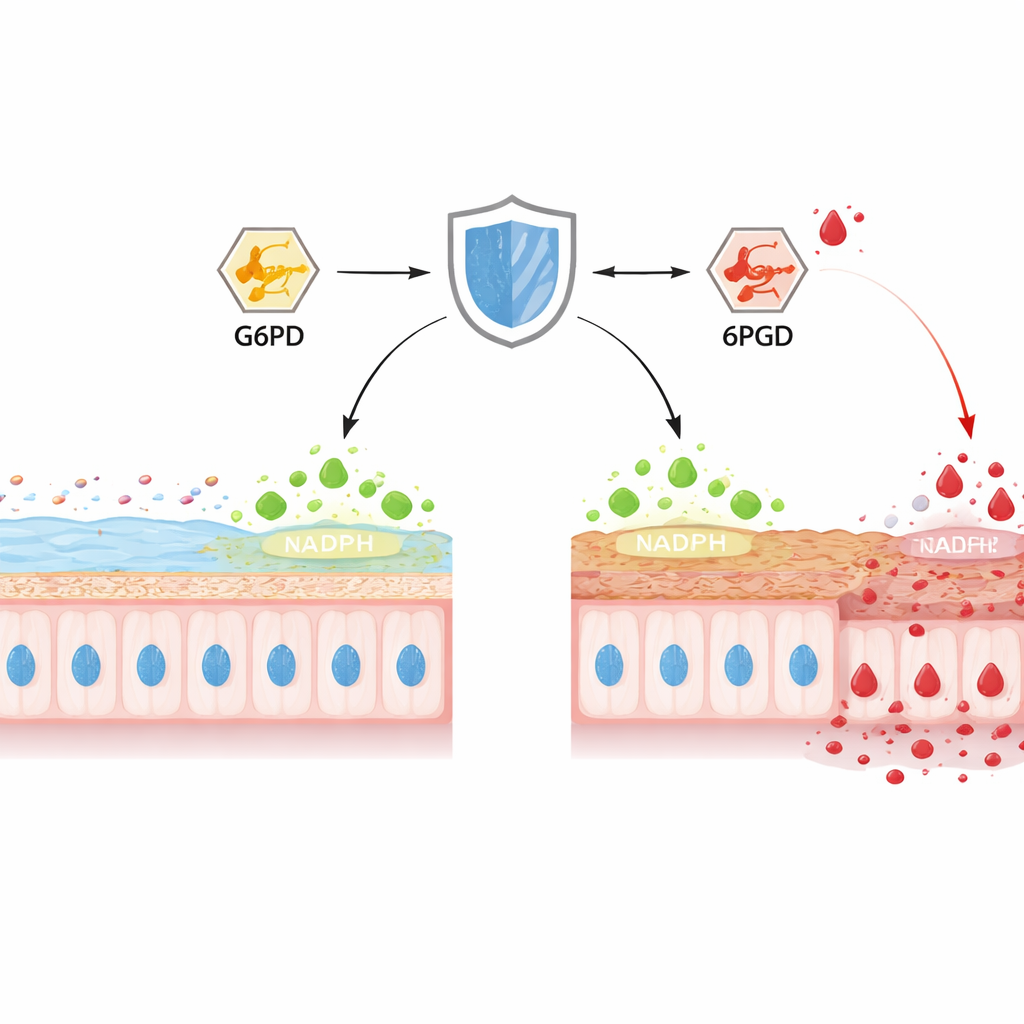
בתוך המעי הגס, תאי גביע מייצרים באופן קבוע את MUC2, חלבון הריר העיקרי שיוצר את הג'ל המגן הפנימי. החוקרים התרכזו ב‑TIGAR, חלבון שידוע כי מונחה להפנות גלוקוז למסלול המייצר NADPH, כוח מיקסון חיוני ששומר על המערכת מפני חמצון מזיק. בעכברים עם קוליטיס כימי, רמות TIGAR במעי הגס ירדו במשך מספר ימים, בדיוק כאשר שכבת הריר הפכה לדקה יותר, פני האפיתל נשחקו והחיידקים התקרבו לרקמה. כאשר החוקרים מחקו באופן סלקטיבי את TIGAR רק ברירית המעי של עכברים, הקוליטיס הופיעה מוקדם יותר והייתה קשה יותר, עם צינורות מעוקלים, פחות תאי גביע ורמות בולטות נמוכות של MUC2 בשלות. מדידות של ביוכימיה תאית חשפו NADPH מותש, מערכות נוגדות חמצון מוחלשות ופרצי זיהום בחמצן ובחנקן פעילים, וקשרו את אובדן ה‑TIGAR ללחץ חמצוני עז וכשל במחסום.
שימוש בסוכר הוסט לשריפה מבזבזת
כדי להבין כיצד TIGAR מעצב את המטבוליזם, הצוות פרופיל מאות מולקולות קטנות בקווי תאים דמויי תאי גביע וברקמת מעי של עכברים. הסרת TIGAR לא שינתה כמה גלוקוז התאים מכניסים פנימה או כמה מהר האורגניזם שורף חמצן, אך שינתה באופן עמוק את גורלו של אותו גלוקוז. באמצעות גלוקוז מסומן הראו שפחות פחמן זרם דרך מסלול הפנטוז‑פוספט — המקור העיקרי ל‑NADPH — בעוד שיותר הוכוּנעו לגלאיקוליזה הקלאסית, שהסתיימה בלקטט. שני מטבוליטים התבלטו: 6‑פוספוגלוקונט, נקודת צומת במסלול הפנטוז‑פוספט, הצטבר בחוזקה, ורמות הלקטט עלו בתאים וברקמות שחסרו TIGAR, במיוחד במהלך קוליטיס. נתוני ביטוי גנים הציעו שגם אנזימי הגליקוליזה הועלו, בעוד שרמות החלבון של שני אנזימי מרכז במסלול הפנטוז‑פוספט, G6PD ו‑6PGD, נשארו ללא שינוי, מה שמרמז כי פעילותם — ולא שפעם — נחסמה.
תג כימי שמנטרל אנזימי נוגדי חמצון
החוקרים גילו אז את מנגנון החסימה: לקטילציה, תג כימי שמתווסף לחלבונים באמצעות לקטט כדונור. במודלים של קוליטיס ובתרביות תאים דלקתיות, לקטילציה כללית של חלבונים עלתה, ושני האנזימים G6PD ו‑6PGD נשאו רמות גבוהות של שינוי זה. ספקטרומטריית מסה זיהתה עמדות ליזין ספציפיות בכל אנזים — K432 ב‑G6PD ו‑K38 ב‑6PGD — כאתרי לקטילציה מרכזיים. מודלים מבניים וניסויי מוטציות הראו ששינוי באתרים אלה מפריע לאופן שבו G6PD יוצר את הדימר הפעיל שלו וכיצד 6PGD קושר את הקו‑פקטור שלו, ובכך מקטין בחדות את יכולתם לייצר NADPH. חסימת ייצור הלקטט או מניעת לקטילציה באתרים אלה שיקמו את פעילות האנזימים, הגדילו NADPH, הורידו את הלחץ החמצוני ושיפרו את הבשלת ה‑MUC2. בעכברים חסרי TIGAR, מסירה של גרסאות מוטנטיות של G6PD ו‑6PGD שלא יכלו לעבור לקטילציה שימרה את עובי הריר וצמצמה חדירת חיידקים לשכבה הפנימית.
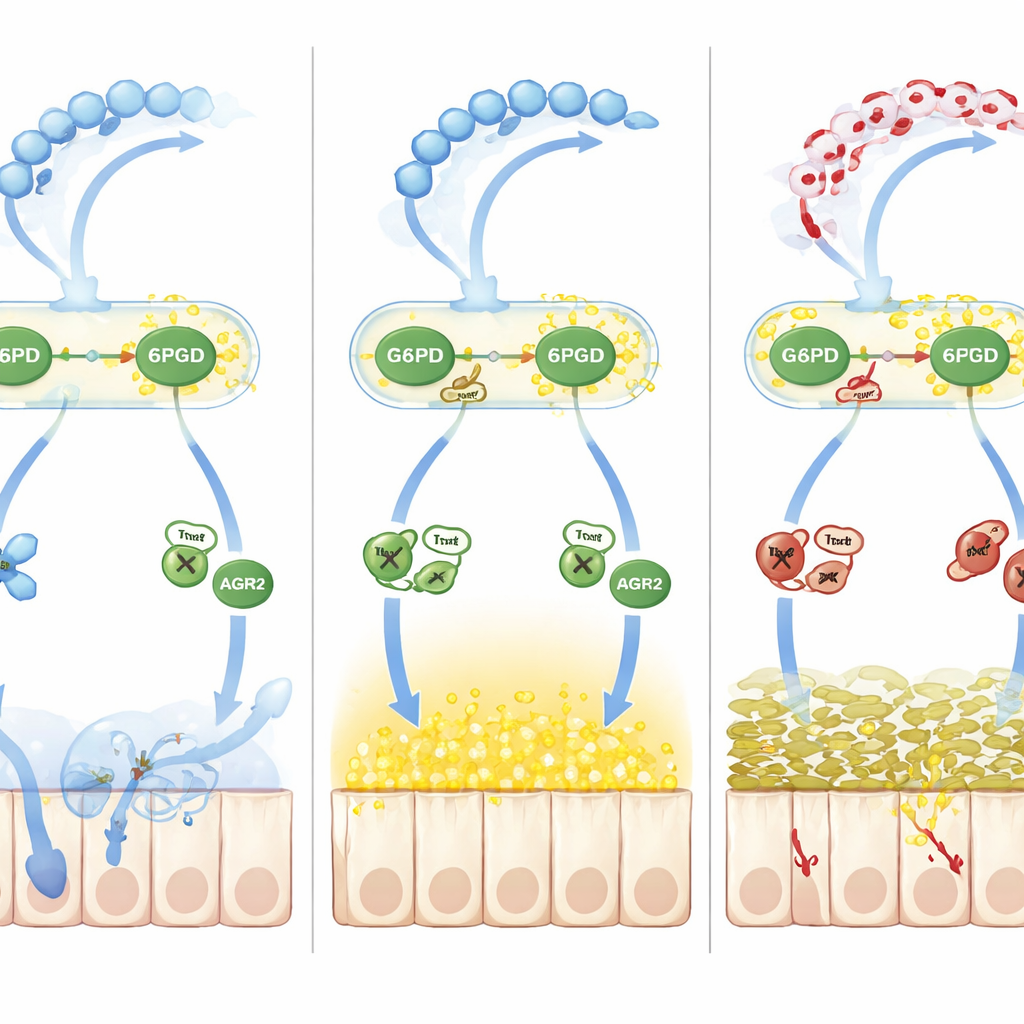
כיצד חוסר איזון רדוקסי מפריע לעיבוד הריר
מעבר לחמצון ישיר, הצוות עקב אחרי גל שני של נזק שמניע חנקן חופשי (חנקתי חמצון). עלייה ברמות חנקן חופשי בקוליטיס הגדילה S‑ניטרוזילציה, תג כימי הפיך נוסף על שיירי ציסטאין. חלבון עזר לקיפול בשם AGR2, החיוני להמרת קדם‑MUC2 לצורתו הבשלת ברשת האנדופלזמטית, הפך כבול ב‑S‑ניטרוזילציה בחומצה אמינית ציסטאין קריטית (Cys81). שינוי זה החליש את אחיזת AGR2 בקדם‑MUC2, מה שגרם להצטברות חלבונים מתקפלים בצורה שגויה ולעליית מתח ברשת האנדופלזמטית, והקטין עוד יותר את מאגר המולקולות הריריות שנוצרו כראוי. התווך המרכזי היה תיאורדוקסין‑1 (Trx1), אנזים רגיש רדוקס שיכול להסיר או להעביר קבוצות ניטרוזיל בהתאם למצב החמצון שלו. כאשר NADPH היה נדיר כי G6PD ו‑6PGD היו לקטילטיים ואיטיים, Trx1 עבר ממצב מפחית ניטרוזילציה מגן למצב שמעביר ניטרוזיל על AGR2, והחמיר את פגימת הריר.
מתי זה חשוב לאנשים עם קוליטיס
העבודה מציעה שרשרת תגובות: דלקת כרונית מורידה את TIGAR בתאי האפיתל המעי; זה מזיז את מסלול השימוש בגלוקוז הרחק ממסלולי יצור NADPH, מגדיל לקטט ומוביל לקטילציה של G6PD ו‑6PGD; ייצור NADPH יורד, Trx1 נהפך יתר‑מחומצע, AGR2 עובר ניטרוזילציה מופרזת ו‑MUC2 נכשלת להתבגר, ומשאירה את המחסום הרירי דק ודולף. לקורא שאיננו מומחה, המסר הוא ששינוי עדין באופן שבו תאי המעי מעבדים סוכר יכול להיתרגם לפגיעה ממשית במגן הרירי של המעי. על‑ידי הגנה על תפקוד TIGAR, מניעת לקטילציה מזיקה של G6PD ו‑6PGD, או איזון מחדש של הכימיה של Trx1 ו‑AGR2, טיפולים עתידיים עשויים לסייע לחזק את מחסום הריר ולרסן את הדלקת בדלקת כיבית של המעי הגס.
ציטוט: Wu, D., Su, S., Zhang, P. et al. TIGAR regulates intestinal mucus barrier integrity by inhibiting lactylation of G6PD/6PGD in ulcerative colitis. Nat Commun 17, 3382 (2026). https://doi.org/10.1038/s41467-026-70263-z
מילות מפתח: דלקת כיבית של המעי הגס, מחסום רירי במעי, TIGAR, לחץ חמצוני, מטבוליזם של גלוקוז