Clear Sky Science · it
TIGAR regola l'integrità della barriera mucosa intestinale inibendo la lattilazione di G6PD/6PGD nella colite ulcerosa
Perché il sottile scudo mucoso dell'intestino è importante
Il rivestimento dei nostri intestini è coperto da uno strato scivoloso di muco che mantiene a distanza trilioni di microbi. Nella colite ulcerosa, una malattia cronica che infiamma il colon, questo mantello protettivo spesso si assottiglia o si rompe, permettendo a batteri e irritanti di raggiungere la parete intestinale. Questo studio indaga perché la barriera mucosa viene meno, seguendo la storia dal metabolismo degli zuccheri all'interno di cellule specializzate nella secrezione di muco fino al danno intestinale—e mette in luce una molecola chiamata TIGAR come promettente nuovo bersaglio terapeutico.
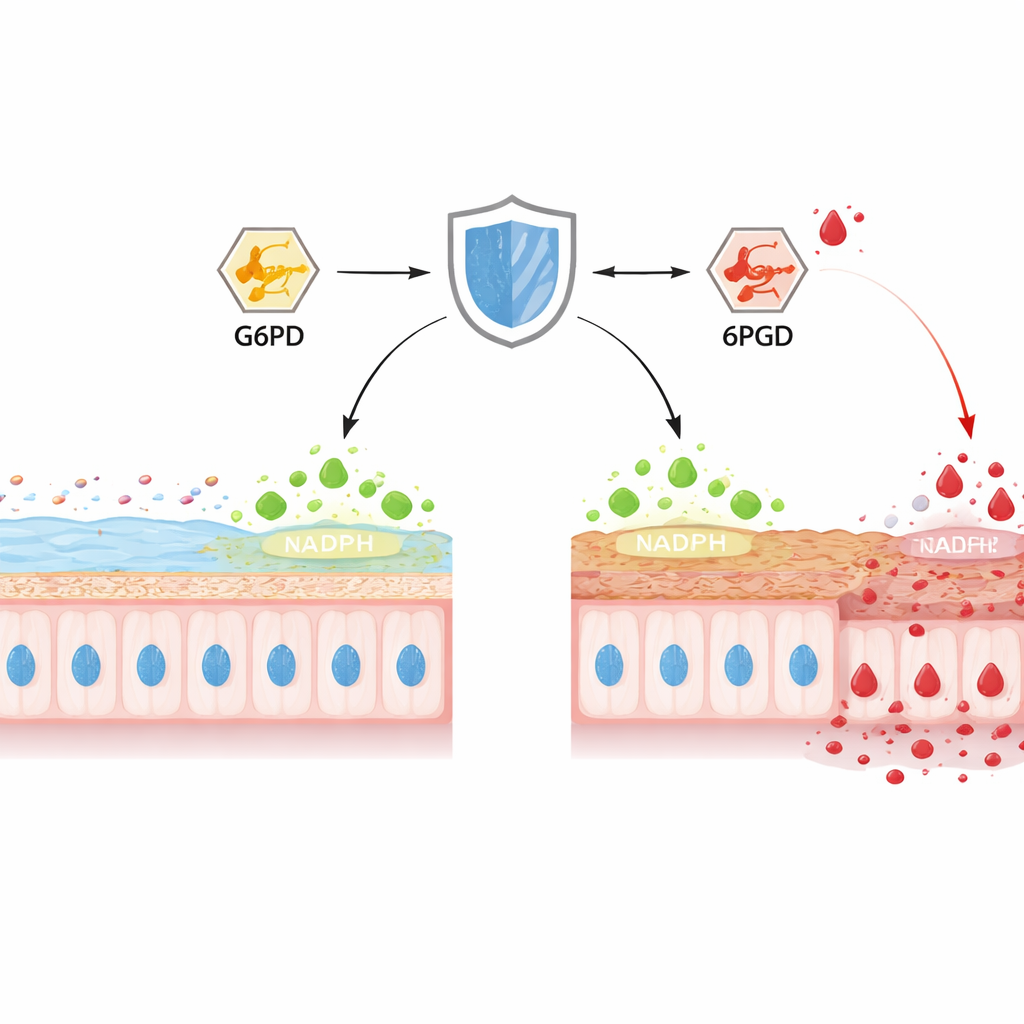
Un difensore nascosto nelle cellule intestinali
Nel colon, le cellule caliciformi producono costantemente MUC2, la principale proteina del muco che forma il gel protettivo interno. Gli autori si sono concentrati su TIGAR, una proteina nota in precedenza per indirizzare il glucosio verso una via che produce NADPH, una «forza riducente» chiave che mantiene sotto controllo gli ossidanti dannosi. Nei topi con colite chimicamente indotta, i livelli di TIGAR nel colon sono diminuiti nell'arco di pochi giorni, proprio mentre lo strato di muco si assottigliava, la superficie epiteliale si erodeva e i batteri si avvicinavano al tessuto. Quando i ricercatori hanno eliminato selettivamente TIGAR solo nell'epitelio intestinale dei topi, la colite è iniziata prima ed è diventata più grave, con cripte distorte, meno cellule caliciformi e una marcata riduzione di MUC2 maturo. Le misure della chimica cellulare hanno rilevato NADPH esaurito, sistemi antiossidanti indeboliti e picchi di specie reattive dell'ossigeno e dell'azoto, collegando la perdita di TIGAR a uno stress ossidativo intenso e al fallimento della barriera.
Il metabolismo dello zucchero riorientato verso la combustione inefficiente
Per capire come TIGAR modella il metabolismo, il team ha profilato centinaia di piccole molecole in linee cellulari simili alle cellule caliciformi e nel tessuto del colon dei topi. La rimozione di TIGAR non ha cambiato la quantità di glucosio importata dalle cellule né la velocità con cui gli animali consumavano ossigeno, ma ha alterato profondamente il destino di quel glucosio. Usando zucchero marcato, hanno mostrato che meno carbonio fluiva attraverso la via delle pentoso‑fosfato—la principale fonte di NADPH—mentre più carbonio veniva spinto nella glicolisi classica, con produzione finale di lattato. Due metaboliti risaltavano: la 6‑fosfogluconato, un crocevia nella via delle pentoso‑fosfato, si accumulava fortemente, e i livelli di lattato aumentavano in cellule e tessuti privi di TIGAR, specialmente durante la colite. I dati di espressione genica suggerivano che gli enzimi della glicolisi erano upregolati, mentre i livelli proteici di due enzimi chiave della via delle pentoso‑fosfato, G6PD e 6PGD, non cambiavano, suggerendo che veniva bloccata la loro attività—non la loro abbondanza.
Un marcatore chimico che disarma gli enzimi antiossidanti
I ricercatori hanno quindi scoperto il meccanismo bloccante: la lattilazione, un marcatore chimico aggiunto alle proteine usando il lattato come donatore. Nei modelli di colite e in colture cellulari infiammatorie, la lattilazione complessiva delle proteine aumentava, e sia G6PD sia 6PGD presentavano alti livelli di questa modifica. La spettrometria di massa ha individuato posizioni specifiche di lisina su ciascun enzima—K432 su G6PD e K38 su 6PGD—come siti principali di lattilazione. La modellizzazione strutturale e i test mutazionali hanno mostrato che modificare questi punti interferisce con il modo in cui G6PD forma il suo dimero attivo e con il modo in cui 6PGD lega il suo cofattore, riducendo nettamente la loro capacità di generare NADPH. Bloccare la produzione di lattato o prevenire la lattilazione in questi siti ha ripristinato l'attività enzimatica, aumentato il NADPH, ridotto lo stress ossidativo e migliorato la maturazione di MUC2. Nei topi carenti di TIGAR, la somministrazione di versioni mutanti di G6PD e 6PGD non soggette a lattilazione ha preservato lo spessore del muco e ridotto l'invasione batterica nello strato interno.
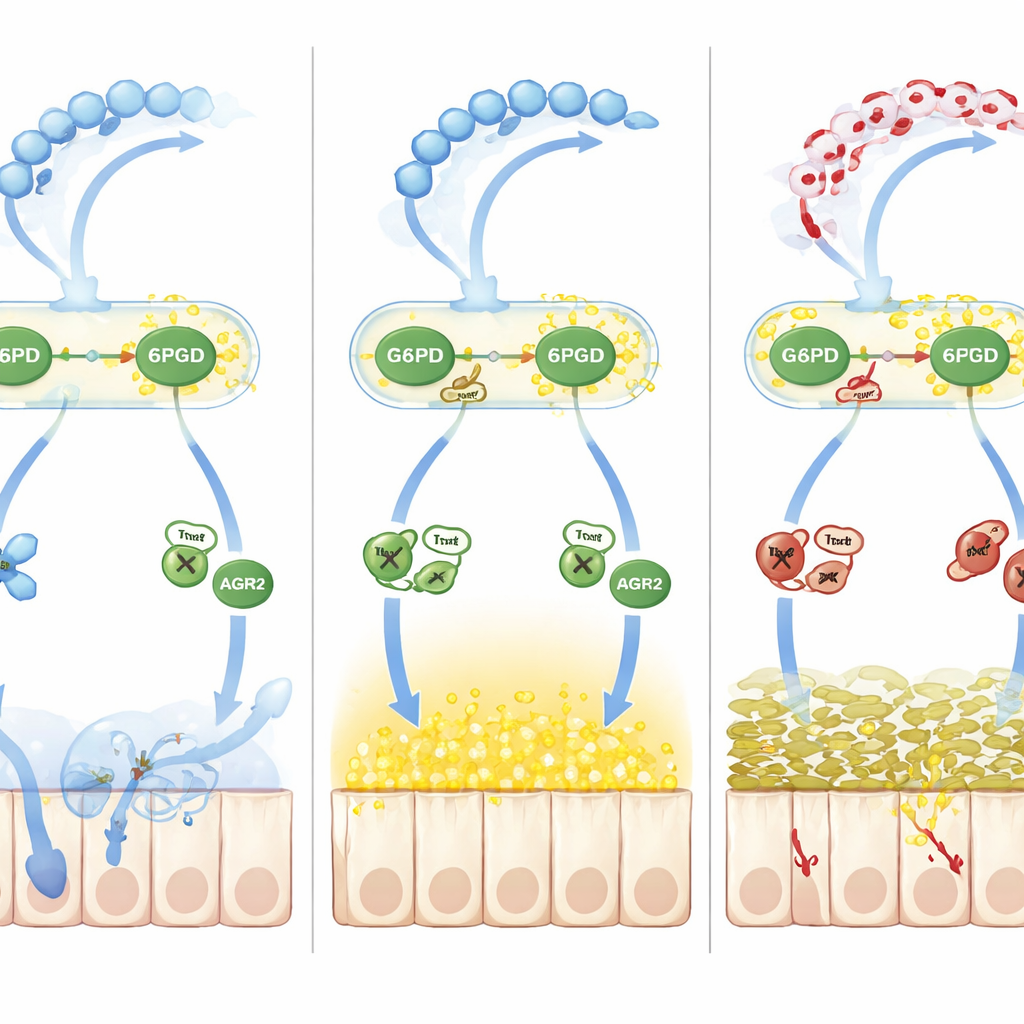
Come lo squilibrio redox deraglia l'elaborazione del muco
Oltre alla semplice ossidazione, il team ha ricostruito una seconda ondata di danno guidata dal monossido di azoto. L'aumento del monossido di azoto nella colite ha incrementato la S‑nitrosilazione, un altro segno chimico reversibile sui residui di cisteina. Una proteina helper per il folding chiamata AGR2, essenziale per convertire i precursori di MUC2 nella loro forma matura nel reticolo endoplasmatico, è diventata fortemente S‑nitrosilata in una cisteina critica (Cys81). Questo cambiamento ha indebolito l'interazione di AGR2 con i precursori di MUC2, causando l'accumulo di proteine non correttamente ripiegate e aumentando lo stress del reticolo endoplasmatico, riducendo ulteriormente la quantità di muco correttamente formato. L'anello di congiunzione chiave è stato la thioredoxina‑1 (Trx1), un enzima sensibile allo stato redox che può rimuovere o trasferire gruppi nitrosili a seconda del suo stato di ossidazione. Quando il NADPH scarseggiava perché G6PD e 6PGD erano lattilate e rallentate, Trx1 passava da una modalità denitrosilante protettiva a una modalità transnitrosilante dannosa, trasferendo gruppi nitrosili su AGR2 e aggravando il difetto del muco.
Cosa significa per le persone con colite
Complessivamente, il lavoro delinea una reazione a catena: l'infiammazione cronica riduce TIGAR nelle cellule epiteliali intestinali; questo devia il glucosio lontano dalle vie produttrici di NADPH, aumenta il lattato e lattila G6PD e 6PGD; la produzione di NADPH cala, Trx1 diventa iper‑ossidato, AGR2 è eccessivamente nitrosilata e MUC2 non matura, lasciando la barriera mucosa sottile e permeabile. Per un lettore non specialistico, il messaggio è che un cambiamento sottile nel modo in cui le cellule intestinali bruciano lo zucchero può tradursi in una rottura molto concreta dello scudo mucoso dell'intestino. Proteggendo la funzione di TIGAR, prevenendo la lattilazione dannosa di G6PD e 6PGD o riequilibrando la chimica di Trx1 e AGR2, trattamenti futuri potrebbero aiutare a rinforzare la barriera mucosa e contenere l'infiammazione nella colite ulcerosa.
Citazione: Wu, D., Su, S., Zhang, P. et al. TIGAR regulates intestinal mucus barrier integrity by inhibiting lactylation of G6PD/6PGD in ulcerative colitis. Nat Commun 17, 3382 (2026). https://doi.org/10.1038/s41467-026-70263-z
Parole chiave: colite ulcerosa, barriera mucosa intestinale, TIGAR, stress ossidativo, metabolismo del glucosio