Clear Sky Science · de
TIGAR reguliert die Integrität der intestinalen Schleimbarriere durch Hemmung der Laktatylierung von G6PD/6PGD bei Colitis ulcerosa
Warum der schleimige Schutz des Darms wichtig ist
Die Auskleidung unseres Darms ist von einer glitschigen Schleimschicht überzogen, die Billionen von Mikroben auf Distanz hält. Bei Colitis ulcerosa, einer chronischen Erkrankung, die den Dickdarm entzündet, wird dieser Schutzmantel häufig dünner oder reißt auf, sodass Bakterien und Reizstoffe die Darmwand erreichen können. Diese Studie untersucht, warum die Schleimbarriere versagt, verfolgt die Geschichte vom Zuckerstoffwechsel in spezialisierten schleimproduzierenden Zellen bis hin zu Schäden im Darm und hebt ein Molekül namens TIGAR als vielversprechendes neues Therapieziel hervor.
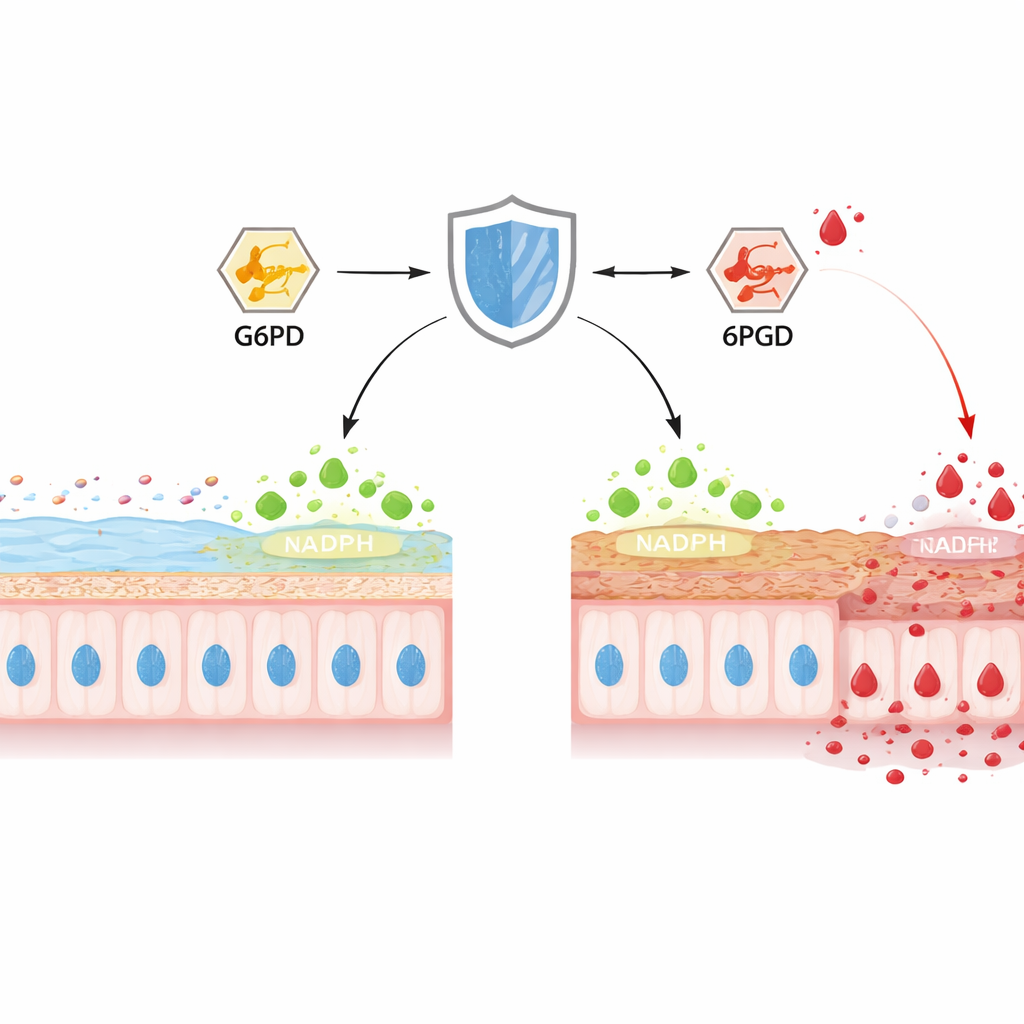
Ein verborgener Verteidiger in Darmzellen
Im Dickdarm stellen Becherzellen ständig MUC2 her, das wichtigste Schleimprotein, das das innere Schutzgel bildet. Die Autoren konzentrierten sich auf TIGAR, ein Protein, das zuvor dafür bekannt war, Glukose in einen Weg zu lenken, der NADPH produziert — eine entscheidende „Reduktionskraft“, die schädliche Oxidantien in Schach hält. Bei Mäusen mit chemisch induzierter Kolitis sanken die TIGAR-Spiegel im Darm über mehrere Tage, parallel dazu wurde die Schleimschicht dünner, die Epitheloberfläche erodierte und Bakterien rückten näher an das Gewebe. Als die Forscher TIGAR selektiv nur in der Darmoberfläche der Mäuse entfernten, begann die Kolitis früher und verlief schwerer, mit deformierten Krypten, weniger Becherzellen und deutlich weniger reifem MUC2. Chemische Messungen auf Zellebene zeigten vermindertes NADPH, geschwächte antioxidative Systeme und starke Anstiege reaktiver Sauerstoff‑ und Stickstoffspezies, was den Verlust von TIGAR mit intensivem oxidativem Stress und Barriereschäden verknüpft.
Zuckergebrauch in Richtung verschwenderischer Verbrennung umprogrammiert
Um zu verstehen, wie TIGAR den Stoffwechsel prägt, analysierte das Team Hunderte kleiner Moleküle in becherzellähnlichen Zelllinien und in Mausdarmpflege. Das Entfernen von TIGAR veränderte nicht die Menge an aufgenommenem Glukose oder wie schnell ganze Tiere Sauerstoff verbrannten, aber es veränderte grundlegend das Schicksal dieser Glukose. Mit markiertem Zucker zeigten sie, dass weniger Kohlenstoff durch den Pentosephosphatweg floss — die Hauptquelle für NADPH — während mehr in die klassische Glykolyse gedrängt wurde, die in Laktat endet. Zwei Metaboliten fielen auf: 6‑Phosphogluconat, ein Knotenpunkt im Pentosephosphatweg, baute sich stark auf, und Laktatspiegel stiegen in Zellen und Geweben ohne TIGAR, besonders während der Kolitis. Genexpressionsdaten deuteten darauf hin, dass Enzyme der Glykolyse hochgefahren wurden, während die Proteinmengen der beiden wichtigen Pentosephosphatenzyme G6PD und 6PGD unverändert blieben, was vermuten ließ, dass ihre Aktivität — nicht ihre Häufigkeit — blockiert wurde.
Ein chemisches Etikett, das antioxidative Enzyme entwaffnet
Die Forscher entdeckten dann den Blockierungsmechanismus: Laktatylierung, ein chemisches Etikett, das Proteinen mittels Laktat als Donor angehängt wird. In Kolitismodellen und in entzündeten Zellkulturen stieg die Gesamtproteinlaktatylierung, und sowohl G6PD als auch 6PGD trugen hohe Mengen dieser Modifikation. Massenspektrometrie identifizierte bestimmte Lysinpositionen auf jedem Enzym — K432 auf G6PD und K38 auf 6PGD — als wichtige Laktatylierungsstellen. Strukturmodellierung und Mutationsversuche zeigten, dass die Modifikation dieser Stellen die Art und Weise stört, wie G6PD sein aktives Dimer bildet und wie 6PGD sein Cofaktor bindet, wodurch ihre Fähigkeit, NADPH zu erzeugen, stark reduziert wird. Das Blockieren der Laktatproduktion oder das Verhindern der Laktatylierung an diesen Stellen stellte die Enzymaktivität wieder her, erhöhte NADPH, senkte den oxidativen Stress und verbesserte die MUC2‑Reifung. In TIGAR‑defizienten Mäusen bewahrte die Übertragung mutierter Versionen von G6PD und 6PGD, die nicht laktatyliert werden konnten, die Schleimstärke und reduzierte das Eindringen von Bakterien in die innere Schicht.
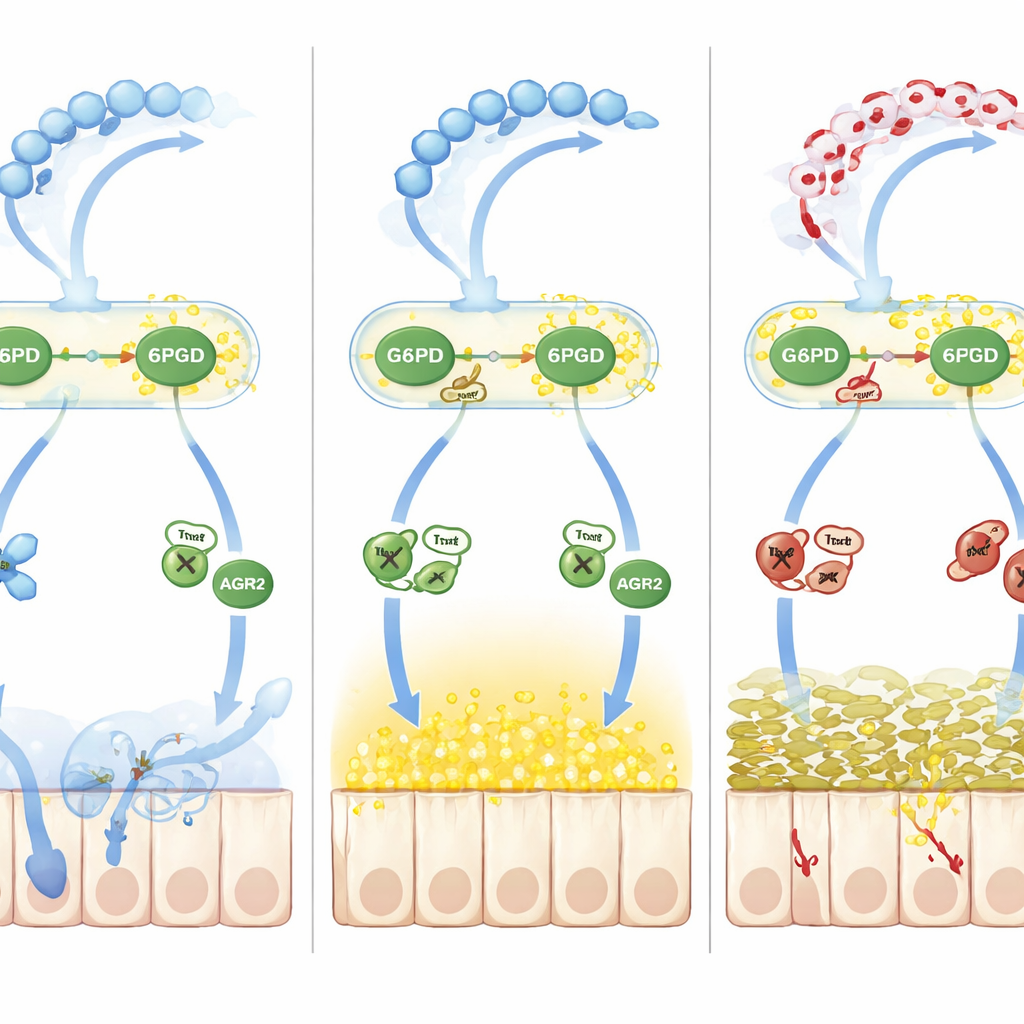
Wie Redoxungleichgewicht die Schleimverarbeitung entgleisen lässt
Über die einfache Oxidation hinaus verfolgte das Team eine zweite Schadenswelle, die vom Stickstoffmonoxid angetrieben wurde. Erhöhtes Stickstoffmonoxid bei Kolitis steigerte die S‑Nitrosylierung, eine weitere reversible chemische Markierung an Cysteinresten. Ein Faltungshelferprotein namens AGR2, das für die Umwandlung von MUC2‑Vormolekülen in ihre reife Form im endoplasmatischen Retikulum essenziell ist, wurde stark an einer kritischen Cysteinstelle (Cys81) S‑nitrosyliert. Diese Veränderung schwächte AGR2s Bindung an MUC2‑Vormoleküle, sodass falsch gefaltete Proteine sich ansammelten und der Stress im endoplasmatischen Retikulum zunahm, was den Anteil korrekt gebildeten Schleims weiter verringerte. Der entscheidende Vermittler war Thioredoxin‑1 (Trx1), ein redox‑sensitives Enzym, das je nach eigenem Oxidationszustand Nitrosylgruppen entfernen oder übertragen kann. Wenn NADPH knapp war, weil G6PD und 6PGD laktatyliert und träge waren, wechselte Trx1 von einem schützenden Denitrosylierungsmodus zu einem schädlichen Transnitrosylierungsmodus, übertrug Nitrosylgruppen auf AGR2 und verschärfte so den Schleimdefekt.
Was das für Menschen mit Colitis bedeutet
Zusammengefasst skizziert die Arbeit eine Kettenreaktion: Chronische Entzündung senkt TIGAR in Darmepithelzellen; dadurch wird Glukose von NADPH‑produzierenden Wegen weggeleitet, Laktat steigt an und laktatyliert G6PD und 6PGD; die NADPH‑Produktion fällt, Trx1 wird überoxidiert, AGR2 wird übermäßig nitrosyliert und MUC2 reift nicht richtig, sodass die Schleimbarriere dünn und durchlässig bleibt. Für Laien ist die Botschaft, dass eine subtile Verschiebung in der Art und Weise, wie Darmzellen Zucker verbrennen, sich in einer sehr greifbaren Lücke im schleimigen Schutz des Darms niederschlagen kann. Durch den Schutz der TIGAR‑Funktion, das Verhindern schädlicher Laktatylierung von G6PD und 6PGD oder das Wiederherstellen des Gleichgewichts von Trx1‑ und AGR2‑Chemie könnten künftige Behandlungen helfen, die Schleimbarriere zu stärken und die Entzündung bei Colitis ulcerosa zu dämpfen.
Zitation: Wu, D., Su, S., Zhang, P. et al. TIGAR regulates intestinal mucus barrier integrity by inhibiting lactylation of G6PD/6PGD in ulcerative colitis. Nat Commun 17, 3382 (2026). https://doi.org/10.1038/s41467-026-70263-z
Schlüsselwörter: Colitis ulcerosa, intestinale Schleimbarriere, TIGAR, oxidativer Stress, Zuckerstoffwechsel