Clear Sky Science · ar
تنظّم TIGAR سلامة حاجز المخاط المعوي عن طريق تثبيط لاكتيلation إنزيمي G6PD/6PGD في التهاب القولون التقرحي
لماذا يهم الدرع المخاطي في الأمعاء
يبطن أمعائنا طبقة مخاطية زلقة تحافظ على تريليونات من الميكروبات على مسافة آمنة. في التهاب القولون التقرحي، وهو مرض مزمن يسبب التهاب القولون، غالبًا ما يضعف هذا الغطاء الواقي أو ينقطع، ما يسمح للبكتيريا والمهيجات بالوصول إلى جدار الأمعاء. تستقصي هذه الدراسة سبب فشل حاجز المخاط، متتبعة القصة من استقلاب السكر داخل الخلايا المتخصّصة في إفراز المخاط وصولًا إلى تلف الأمعاء، ومبرزة جزيئًا يسمى TIGAR كهدف واعد للعلاج.
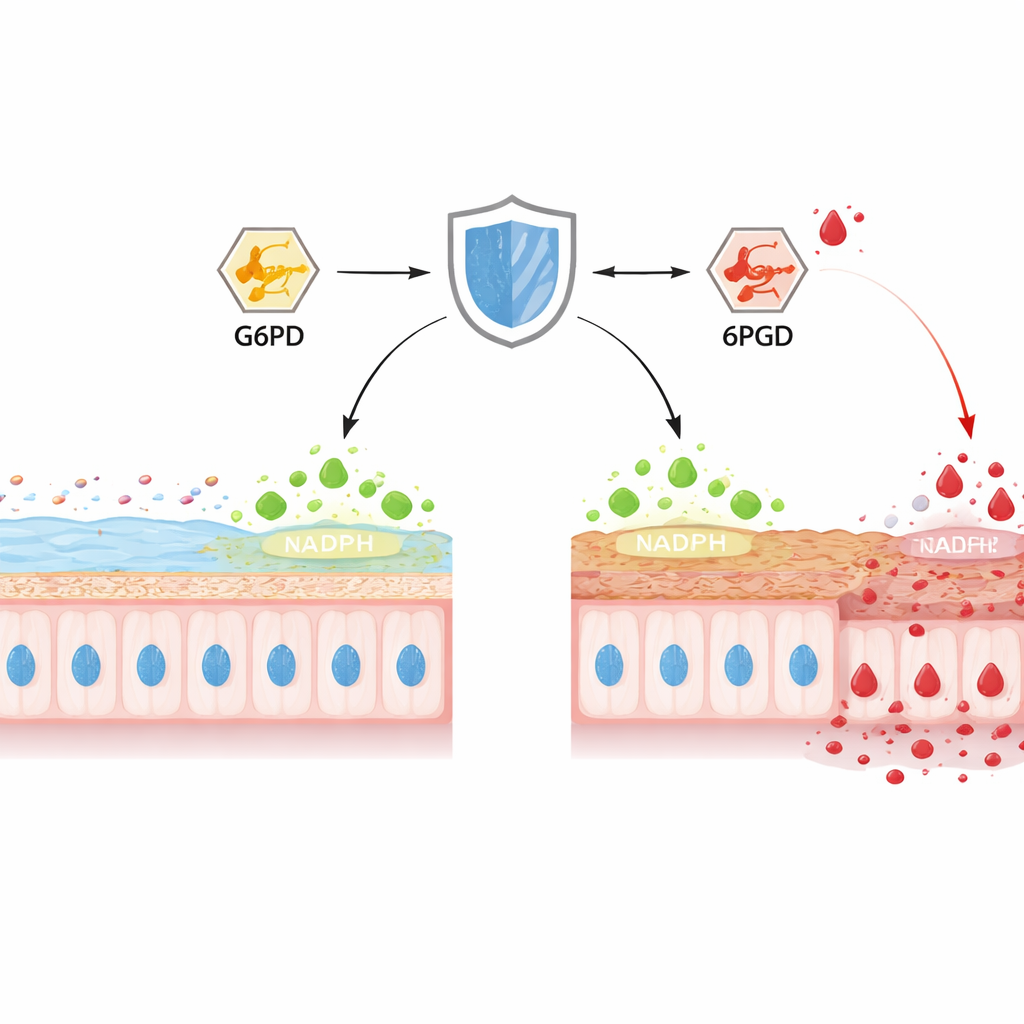
مدافع خفي في خلايا الأمعاء
داخل القولون، تصنّع خلايا الكأس باستمرار MUC2، البروتين المخاطي الرئيسي الذي يشكل الهلام الحامي الداخلي. ركز المؤلفون على TIGAR، بروتين معروف سابقًا بتوجيه الغلوكوز إلى مسار يصنع NADPH، القوة الاختزالية الأساسية التي تكبح المؤكسدات الضارة. في الفئران المصابة بالتهاب القولون المنشأ كيميائيًا، انخفضت مستويات TIGAR في القولون على مدى أيام، تمامًا مع ترقّق طبقة المخاط وتآكل السطح الظهاري واقتراب البكتيريا من النسيج. عندما حذفت الدراسة TIGAR انتقائيًا في بطانة الأمعاء لدى الفئران، بدأ التهاب القولون مبكرًا وشدّته زادت، مع تشوهات في الحُقَن المعوية، نقص خلايا الكأس، وانخفاض واضح في نضوج MUC2. كشفت مقاييس الكيمياء الخلوية عن استنزاف NADPH وتضعف أنظمة مضادات الأكسدة وارتفاعات في أنواع الأكسجين والنيتروجين التفاعلية، رابطًة فقدان TIGAR بالإجهاد التأكسدي الحاد وفشل الحاجز.
إعادة توجيه استخدام السكر نحو الاحتراق المهدِر
لفهم كيف يشكّل TIGAR الاستقلاب، حلّل الفريق مئات الجزيئات الصغيرة في سلاسل خلايا شبيهة بخلايا الكأس ونسيج قولون الفئران. لم يغير حذف TIGAR كمية الغلوكوز التي تستورِدها الخلايا أو سرعة حرق الأكسجين في الحيوان ككل، لكنه بدّل مصير ذلك الغلوكوز بعمق. باستخدام سكر معنّلم، أظهروا أن تدفق الكربون عبر مسار الفوسفات الخماسي—المصدر الرئيسي لـNADPH—انخفض، بينما زاد التوجّه نحو التحلل السكري الكلاسيكي، المنتهي باللاكتات. برز موقِفا استقلابيان: 6‑فوسفوجلوكونات، مركز في مسار الفوسفات الخماسي، تراكم بشدة، وارتفعت مستويات اللاكتات في الخلايا والأنسجة الخالية من TIGAR، خاصة أثناء التهاب القولون. اقترحت بيانات التعبير الجيني رفع نشاط إنزيمات التحلل السكري، بينما بقيت مستويات البروتين لإنزيمين رئيسيين من الفوسفات الخماسي، G6PD و6PGD، دون تغيير، مما يوحي أن نشاطهما—لا كميتهما—هو ما يتعطّل.
شارة كيميائية تعطل إنزيمات مضادات الأكسدة
كشف الباحثون بعد ذلك آلية التعطيل: اللاكتيلation، شارة كيميائية تُضاف إلى البروتينات باستخدام اللاكتات كمانح. في نماذج التهاب القولون وفي ثقافات خلوية ملتهبة، ارتفعت لاكتيلation البروتينات بشكل عام، وحملا كل من G6PD و6PGD مستويات عالية من هذا التعديل. حدّد التحليل الطيفي الكتلي مواقع ليزين محددة في كل إنزيم—K432 في G6PD وK38 في 6PGD—كمواقع لاكتيلation رئيسية. أظهرت النمذجة البنيوية والاختبارات الطفيرية أن تعديل هذه المواقع يتداخل مع طريقة تكوين G6PD للثنائيات الفعّالة وكيفية ارتباط 6PGD وعاءه المساعد، مما يقلل بشدة من قدرتهما على توليد NADPH. عَملت موانع إنتاج اللاكتات أو منع اللاكتيلation عند هذه المواقع على استعادة نشاط الإنزيمات، وزيادة NADPH، وخفض الإجهاد التأكسدي، وتحسين نضوج MUC2. في فئران ناقصة TIGAR، أدّى إيصال نسخ طفيرية من G6PD و6PGD غير قابلة للاكتيلation إلى الحفاظ على سمك المخاط وتقليل تغلغل البكتيريا في الطبقة الداخلية.
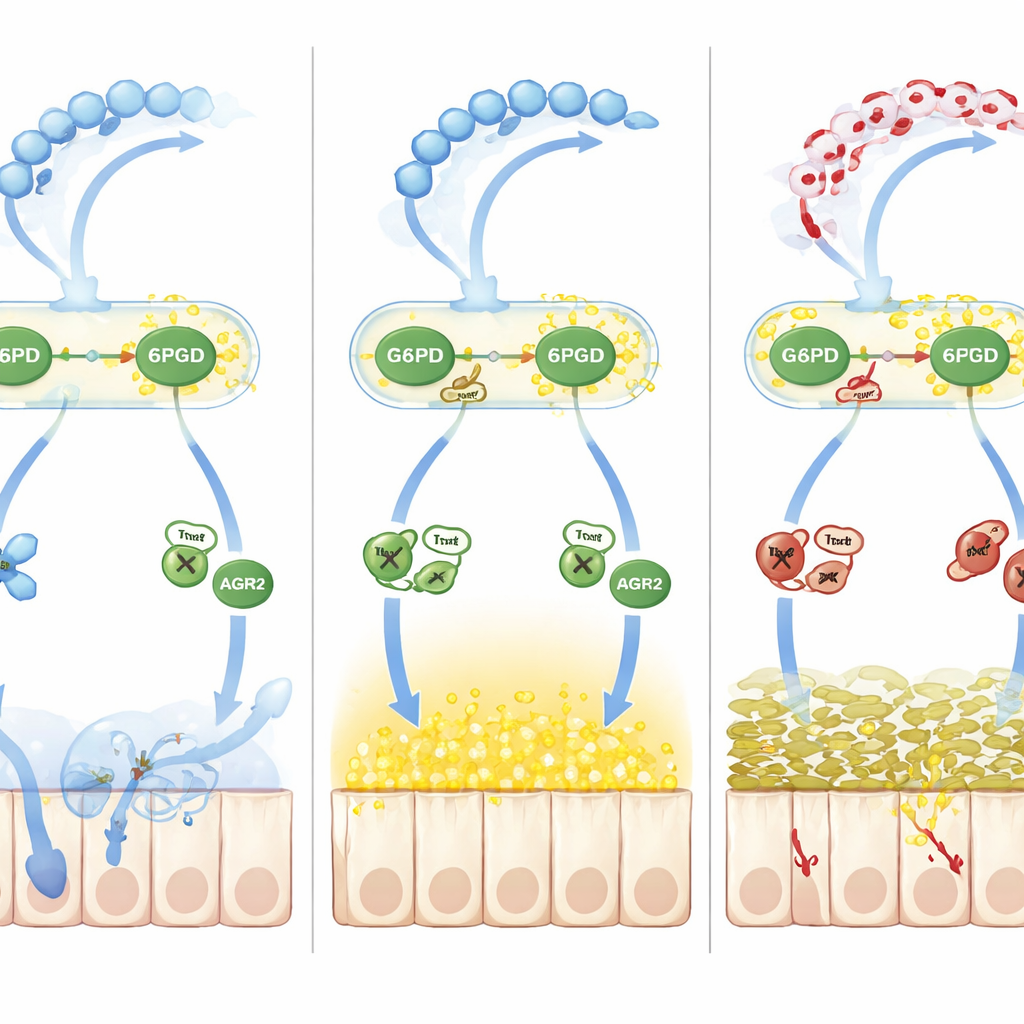
كيف يقوّض الخلل التأكسدي معالجة المخاط
بعيدًا عن الأكسدة البسيطة، تعقّب الفريق موجة ثانية من التلف يقودها أكسيد النيتريك. زيادات أكسيد النيتريك في التهاب القولون رفعت مستوى S‑nitrosylation، علامة كيميائية عكسية أخرى على بقايا السيستين. أصبح بروتين مساعِد الطيّ AGR2، الضروري لتحويل مجهرات MUC2 إلى شكلها الناضج في الشبكة الإندوبلازمية، مُشبَعًا بـS‑nitrosylation على سيستين حرج (Cys81). أضعف هذا التغيير قدرة AGR2 على الإمساك بمسبّقات MUC2، مما تسبب في تراكم بروتينات غير مطوية وارتفاع إجهاد الشبكة الإندوبلازمية، وهو ما قلّل أكثر من حوض المخاط المشكلة بشكل صحيح. كانت الوسيط الرئيسي ثيورِدوكسين‑1 (Trx1)، إنزيم حساس للتوازن الاختزالي يمكنه إما إزالة مجموعات النيتروزيل أو نقلها تبعًا لحالته التأكسدية. عندما نَفَد NADPH لأن G6PD و6PGD أُصِيبَا باللاكتيلation وأصبحا بطيئين، تحوّل Trx1 من وضع نزع النيتروزيل الحامي إلى وضع نقل النيتروزيل الضار، ناقلاً مجموعات النيتروزيل إلى AGR2 ومفاقمًا عيب المخاط.
ماذا يعني هذا للأشخاص المصابين بالتهاب القولون
معًا، تبيّن هذه النتائج سلسلة تفاعلات: يقلل الالتهاب المزمن TIGAR في خلايا الظهارة المعوية؛ هذا يحوّل الغلوكوز بعيدًا عن مسارات إنتاج NADPH، يزيد اللاكتات، ولاكتيلates G6PD و6PGD؛ ينخفض إنتاج NADPH، ويصبح Trx1 مفرط الأكسدة، ويُصاب AGR2 بقدر زائد من النيتروزيلة، ويفشل MUC2 في النضوج، تاركًا حاجز المخاط رقيقًا ومتسرّبًا. للقارئ العام، الرسالة أن تغييرًا دقيقًا في كيفية استهلاك خلايا الأمعاء للسكر يمكن أن يتحول إلى اختراق مادي واضح في الدرع المخاطي للأمعاء. بحماية وظيفة TIGAR، أو منع اللاكتيلation الضار لـG6PD و6PGD، أو إعادة توازن كيمياء Trx1 وAGR2، قد تساعد العلاجات المستقبلية في تعزيز حاجز المخاط وكبح الالتهاب في التهاب القولون التقرحي.
الاستشهاد: Wu, D., Su, S., Zhang, P. et al. TIGAR regulates intestinal mucus barrier integrity by inhibiting lactylation of G6PD/6PGD in ulcerative colitis. Nat Commun 17, 3382 (2026). https://doi.org/10.1038/s41467-026-70263-z
الكلمات المفتاحية: التهاب القولون التقرحي, حاجز مخاطي معوي, TIGAR, الإجهاد التأكسدي, تمثيل الغلوكوز