Clear Sky Science · pt
TIGAR regula a integridade da barreira de muco intestinal ao inibir a lactilação de G6PD/6PGD na colite ulcerativa
Por que o escudo viscoso do intestino importa
O revestimento do nosso intestino é coberto por uma camada escorregadia de muco que mantém trilhões de microrganismos à distância. Na colite ulcerativa, uma doença crônica que inflama o cólon, esse manto protetor frequentemente afina ou se rompe, permitindo que bactérias e irritantes alcancem a parede intestinal. Este estudo investiga por que essa barreira de muco falha, traçando a história desde o metabolismo da glicose dentro de células especializadas em secretar muco até o dano no intestino — e destacando uma molécula chamada TIGAR como um novo alvo promissor para terapia.
Um defensor discreto nas células intestinais
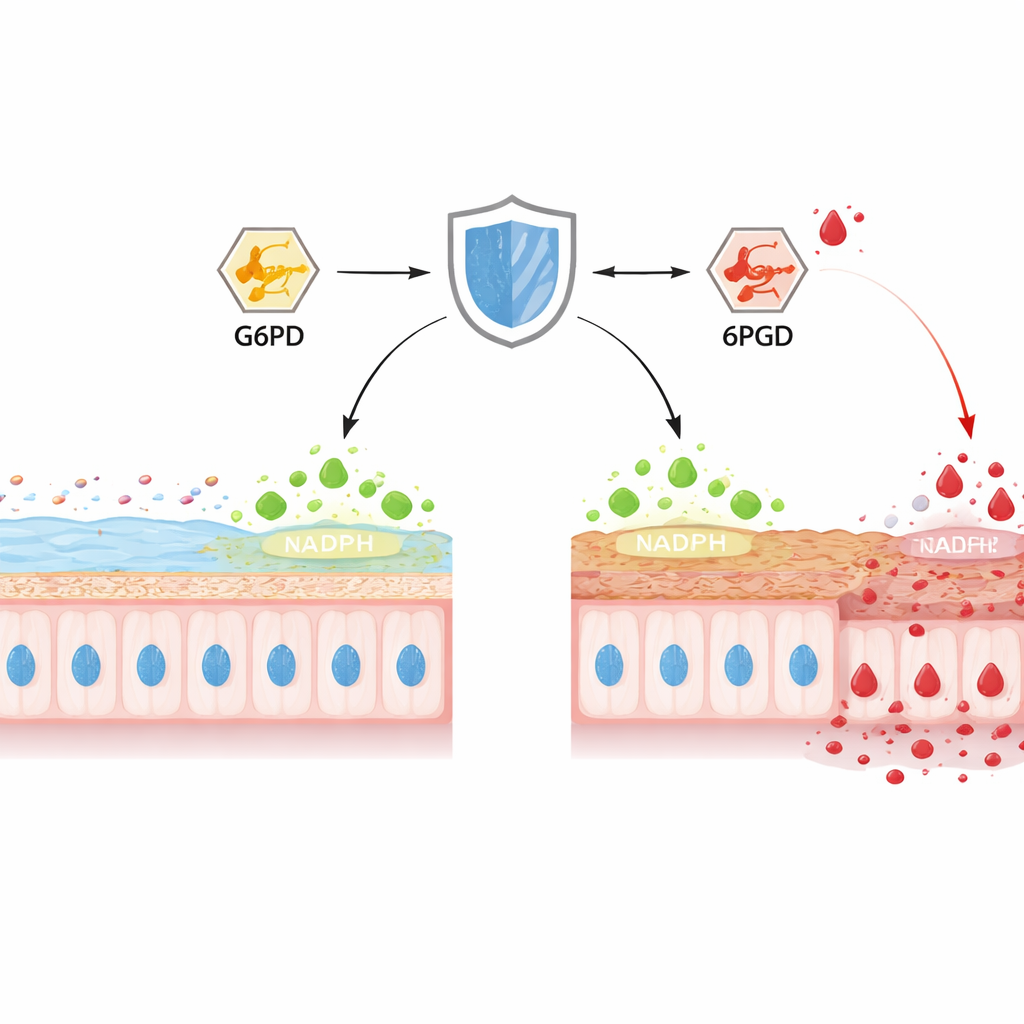
No cólon, as células caliciformes fabricam continuamente MUC2, a principal proteína do muco que forma o gel protetor interno. Os autores se concentraram no TIGAR, uma proteína previamente conhecida por direcionar a glicose para uma via que produz NADPH, um “poder redutor” essencial que mantém oxidantes nocivos sob controle. Em camundongos com colite induzida quimicamente, os níveis de TIGAR no cólon caíram ao longo de vários dias, justamente quando a camada de muco afinou, a superfície epitelial se erodiu e as bactérias se aproximaram mais do tecido. Quando os pesquisadores deletaram seletivamente o TIGAR apenas no revestimento intestinal dos camundongos, a colite começou mais cedo e se tornou mais grave, com criptas distorcidas, menos células caliciformes e muito menos MUC2 maduro. Medidas da bioquímica celular revelaram NADPH esgotado, sistemas antioxidantes enfraquecidos e surtos de espécies reativas de oxigênio e nitrogênio, ligando a perda de TIGAR a intenso estresse oxidativo e à falha da barreira.
Uso de açúcar reprogramado para queima inútil
Para entender como o TIGAR molda o metabolismo, a equipe perfilou centenas de pequenas moléculas em linhagens de células semelhantes a caliciformes e em tecido de cólon de camundongo. Remover o TIGAR não alterou quanto glicose as células importavam nem a rapidez com que os animais consumiam oxigênio, mas mudou profundamente o destino dessa glicose. Usando açúcar marcado, mostraram que menos carbono fluía pela via das pentoses fosfato — a principal fonte de NADPH — enquanto mais era empurrado para a glicólise clássica, terminando em lactato. Dois metabólitos se destacaram: 6‑fosfogluconato, um ponto central na via das pentoses fosfato, acumulou‑se fortemente, e os níveis de lactato aumentaram em células e tecidos sem TIGAR, especialmente durante a colite. Dados de expressão gênica sugeriram que enzimas da glicólise foram aumentadas, enquanto os níveis das proteínas de duas enzimas-chave da via das pentoses fosfato, G6PD e 6PGD, permaneceram inalterados, indicando que sua atividade — não sua abundância — estava sendo bloqueada.
Uma etiqueta química que desarma enzimas antioxidantes
Os pesquisadores então descobriram o mecanismo de bloqueio: a lactilação, uma marca química adicionada a proteínas usando o lactato como doador. Em modelos de colite e em culturas celulares inflamatórias, a lactilação total de proteínas aumentou, e tanto G6PD quanto 6PGD exibiram altos níveis dessa modificação. Espectrometria de massa identificou posições específicas de lisina em cada enzima — K432 na G6PD e K38 na 6PGD — como sítios principais de lactilação. Modelagem estrutural e testes mutacionais mostraram que modificar esses pontos interfere na forma como a G6PD forma seu dímero ativo e como a 6PGD se liga ao cofator, reduzindo fortemente sua capacidade de gerar NADPH. Bloquear a produção de lactato ou impedir a lactilação nesses sítios restaurou a atividade enzimática, aumentou o NADPH, diminuiu o estresse oxidativo e melhorou a maturação do MUC2. Em camundongos deficientes em TIGAR, a entrega de versões mutantes de G6PD e 6PGD que não podiam ser lactiladas preservou a espessura do muco e reduziu a intrusão bacteriana na camada interna.
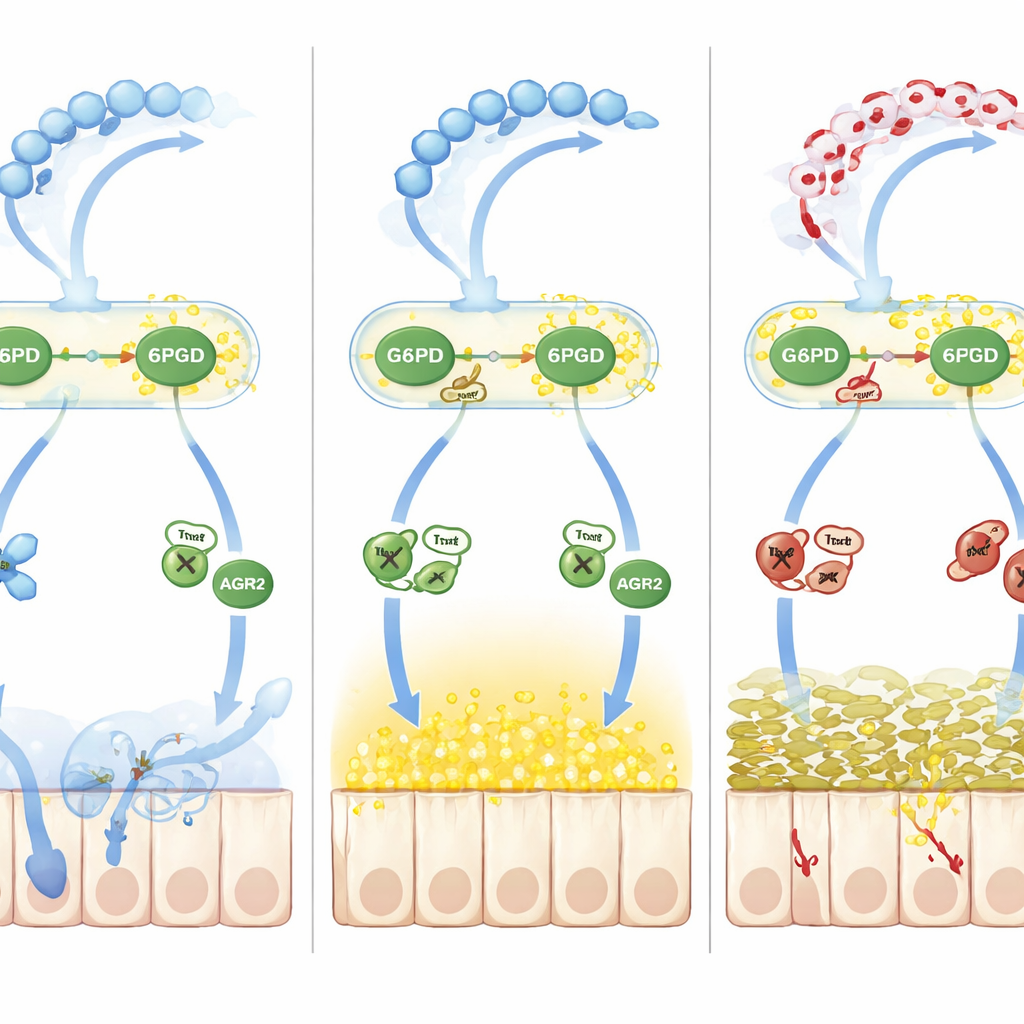
Como o desequilíbrio redox atrapalha o processamento do muco
Além da oxidação simples, a equipe rastreou uma segunda onda de dano impulsionada pelo óxido nítrico. Níveis elevados de óxido nítrico na colite aumentaram a S‑nitrosilação, outra marca química reversível em resíduos de cisteína. Uma proteína auxiliar de dobramento chamada AGR2, essencial para converter os precursores de MUC2 em sua forma madura no retículo endoplasmático, tornou‑se fortemente S‑nitrosilada em uma cisteína crítica (Cys81). Essa alteração enfraqueceu a interação da AGR2 com os precursores de MUC2, causando acúmulo de proteínas mal dobradas e aumentando o estresse do retículo endoplasmático, reduzindo ainda mais o conjunto de muco corretamente formado. O intermediário chave foi a tioredoxina‑1 (Trx1), uma enzima sensível ao estado redox que pode remover ou transferir grupos nitrosila dependendo de seu próprio estado de oxidação. Quando o NADPH estava escasso porque G6PD e 6PGD estavam lactiladas e lentas, a Trx1 mudou de um modo protetor de desnitosilação para um modo prejudicial de transmetilação de nitrosila, transferindo grupos nitrosila para a AGR2 e aprofundando o defeito do muco.
O que isso significa para pessoas com colite
Em conjunto, o trabalho delineia uma reação em cadeia: inflamação crônica reduz o TIGAR nas células epiteliais intestinais; isso desvia a glicose das rotas produtoras de NADPH, aumenta o lactato e provoca a lactilação de G6PD e 6PGD; a produção de NADPH cai, a Trx1 fica hiperoxidada, a AGR2 é excessivamente nitrosilada e o MUC2 deixa de maturar, deixando a barreira de muco fina e permeável. Para o leitor leigo, a mensagem é que uma mudança sutil em como as células intestinais queimam açúcar pode se traduzir em uma ruptura muito física no escudo viscoso do intestino. Protegendo a função do TIGAR, prevenindo a lactilação prejudicial de G6PD e 6PGD ou reequilibrando a química de Trx1 e AGR2, tratamentos futuros podem ajudar a reforçar a barreira de muco e a controlar a inflamação na colite ulcerativa.
Citação: Wu, D., Su, S., Zhang, P. et al. TIGAR regulates intestinal mucus barrier integrity by inhibiting lactylation of G6PD/6PGD in ulcerative colitis. Nat Commun 17, 3382 (2026). https://doi.org/10.1038/s41467-026-70263-z
Palavras-chave: colite ulcerativa, barreira de muco intestinal, TIGAR, estresse oxidativo, metabolismo da glicose