Clear Sky Science · ru
TIGAR регулирует целостность защитного слизистого барьера кишечника, ингибируя лактиляцию G6PD/6PGD при язвенном колите
Почему важен слизистый щит кишечника
Поверхность кишечника покрыта скользким слоем слизи, который удерживает триллионы микробов на расстоянии. При язвенном колите — хроническом воспалительном заболевании толстой кишки — эта защитная оболочка часто истончается или нарушается, позволяя бактериям и раздражителям достигать стенки кишки. В этом исследовании анализируют, почему рушится слизистый барьер: путь простирается от обмена сахаров в специализированных слизистых клетках до повреждения кишечной ткани — и выделяет молекулу TIGAR как перспективную мишень для терапии.
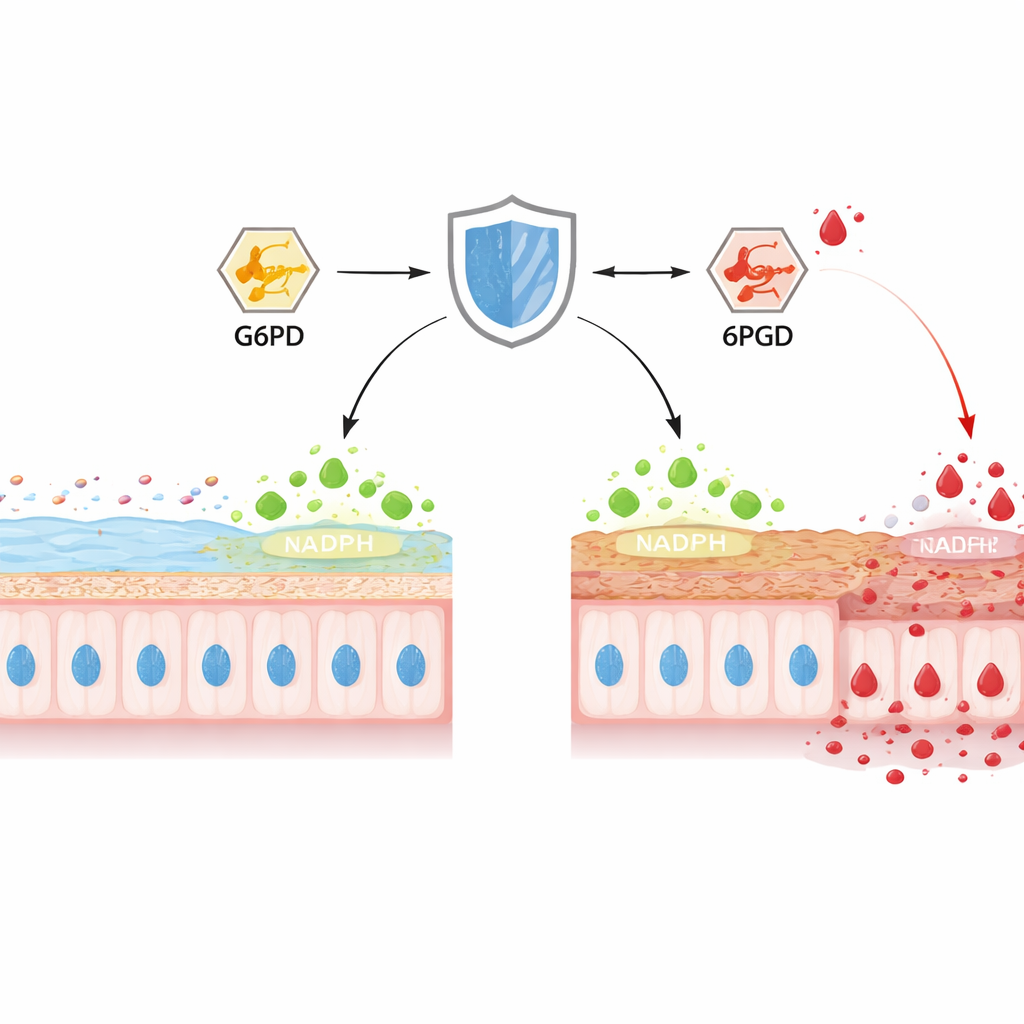
Скрытый защитник в клетках кишечника
В толстой кишке бокаловидные клетки постоянно синтезируют MUC2 — основной белок слизи, формирующий внутренний защитный гель. Авторы сосредоточились на TIGAR, белке, ранее известном тем, что направляет глюкозу в путь, синтезирующий NADPH — ключевую «восстановительную силу», которая сдерживает вредные окислители. У мышей с химически вызванным колитом уровень TIGAR в толстой кишке снижался в течение нескольких дней, одновременно истончался слой слизи, эродировалась эпителиальная поверхность и бактерии приближались к ткани. При селективном удалении TIGAR только в кишечном эпителии у мышей колит начинался раньше и протекал тяжелее: наблюдались деформированные крипты, меньше бокаловидных клеток и заметно сниженное содержание зрелого MUC2. Биохимические замеры выявили истощение NADPH, ослабление антиоксидантных систем и всплески реактивных форм кислорода и азота, связывая потерю TIGAR с выраженным оксидативным стрессом и нарушением барьера.
Перенастройка использования сахара в сторону бесполезного горения
Чтобы понять, как TIGAR формирует метаболизм, команда профилировала сотни малых молекул в линиях клеток, напоминающих бокаловидные клетки, и в тканях толстой кишки мышей. Удаление TIGAR не изменило объема поступающей в клетки глюкозы и не повлияло на скорость потребления кислорода у животных, но существенно изменило судьбу этой глюкозы. С помощью меченого сахара они показали, что меньше углерода шло по пентозофосфатному пути — основному источнику NADPH — тогда как больше направлялось в классическую гликолизу с образованием лактата. Выделялись два метаболита: 6‑фосфоглюконат, узел в пентозофосфатном пути, значительно накапливался, а уровни лактата повышались в клетках и тканях без TIGAR, особенно при колите. Данные об экспрессии генов указывали на усиление ферментов гликолиза, тогда как уровни белка двух ключевых ферментов пентозофосфатного пути, G6PD и 6PGD, оставались неизменными, что наводило на мысль: блокируется их активность, а не уменьшается количество.
Химическая метка, которая нейтрализует антиоксидантные ферменты
Исследователи выявили механизм блокировки: лактиляция — химическая метка, добавляемая к белкам с использованием лактата в качестве донора. В моделях колита и в культурах воспаленных клеток общая лактиляция белков возрастала, и как G6PD, так и 6PGD несли высокие уровни этой модификации. Масс‑спектрометрия точно определила отдельные лизиновые позиции в каждом ферменте — K432 в G6PD и K38 в 6PGD — как основные сайты лактиляции. Моделирование структуры и мутационные тесты показали, что модификация этих участков мешает формированию активного димера G6PD и связыванию кофактора 6PGD, резко снижая их способность генерировать NADPH. Блокирование образования лактата или предотвращение лактиляции в этих сайтах восстанавливало активность ферментов, увеличивало NADPH, снижало оксидативный стресс и улучшало созревание MUC2. У мышей, лишенных TIGAR, доставка мутантных версий G6PD и 6PGD, не способных к лактиляции, сохраняла толщину слизи и уменьшала проникновение бактерий во внутренний слой.
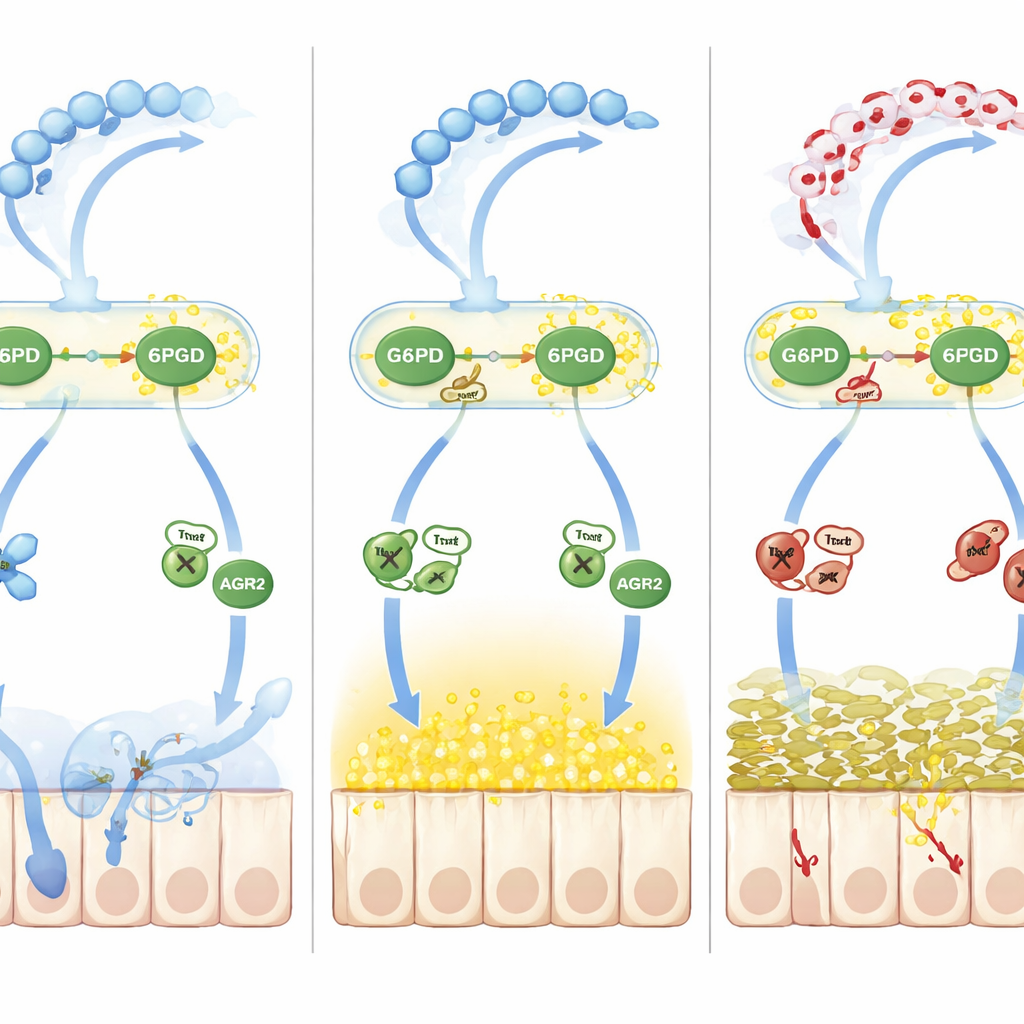
Как дисбаланс редокс‑статуса нарушает обработку слизи
Помимо простой окислительной нагрузки, команда проследила вторую волну повреждений, обусловленную оксидом азота. Повышенный уровень оксида азота при колите усиливал S‑нитрозилирование — еще одну обратимую химическую метку на остатках цистеина. Шаперон AGR2, необходимый для превращения предшественников MUC2 в зрелую форму в эндоплазматическом ретикулуме, оказался сильно S‑нитрозилированным в критическом цистеине (Cys81). Это ослабляло его взаимодействие с предшественниками MUC2, приводя к накоплению неправильно свернутых белков и усилению стресса эндоплазматического ретикулума, что дополнительно уменьшало пул правильно сформированной слизи. Ключевым посредником оказался тиоредоксин‑1 (Trx1) — редокс‑чувствительный фермент, который может либо удалять, либо переносить нитрозильные группы в зависимости от собственного состояния окисления. Когда NADPH был в дефиците из‑за лактиляции и торможения G6PD и 6PGD, Trx1 переключался с защитного режима денитрозилирования на вредоносный режим транзнитрозилирования, перенося нитрозильные группы на AGR2 и усугубляя дефект слизи.
Что это значит для пациентов с колитом
В совокупности работа описывает цепную реакцию: хроническое воспаление снижает TIGAR в эпителиальных клетках кишечника; это отводит глюкозу от путей, производящих NADPH, повышает уровень лактата и приводит к лактиляции G6PD и 6PGD; производство NADPH падает, Trx1 переокисляется, AGR2 чрезмерно нитрозилируется, и MUC2 не созревает, оставляя слизистый барьер тонким и проницаемым. Для непрофессионального читателя основной вывод таков: даже тонкое смещение в том, как клетки кишечника используют сахар, может вылиться в физическое нарушение их слизистого щита. Защита функции TIGAR, предотвращение вредной лактиляции G6PD и 6PGD или восстановление баланса в химии Trx1 и AGR2 могут стать путями для будущих терапий, которые укрепят слизистый барьер и смягчат воспаление при язвенном колите.
Цитирование: Wu, D., Su, S., Zhang, P. et al. TIGAR regulates intestinal mucus barrier integrity by inhibiting lactylation of G6PD/6PGD in ulcerative colitis. Nat Commun 17, 3382 (2026). https://doi.org/10.1038/s41467-026-70263-z
Ключевые слова: язвенный колит, слизистый барьер кишечника, TIGAR, оксидативный стресс, углеводный обмен