Clear Sky Science · es
TIGAR regula la integridad de la barrera mucosa intestinal inhibiendo la lactilación de G6PD/6PGD en la colitis ulcerosa
Por qué importa el escudo viscoso del intestino
El revestimiento de nuestros intestinos está cubierto por una capa resbaladiza de moco que mantiene a raya a trillones de microbios. En la colitis ulcerosa, una enfermedad crónica que inflama el colon, este manto protector con frecuencia se adelgaza o rompe, permitiendo que bacterias e irritantes lleguen a la pared intestinal. Este estudio explora por qué falla esa barrera mucosa, trazando la historia desde el metabolismo de la glucosa dentro de células especializadas en secretar moco hasta el daño en el intestino, y destacando a una molécula llamada TIGAR como un prometedor nuevo objetivo terapéutico.
Un defensor oculto en las células intestinales
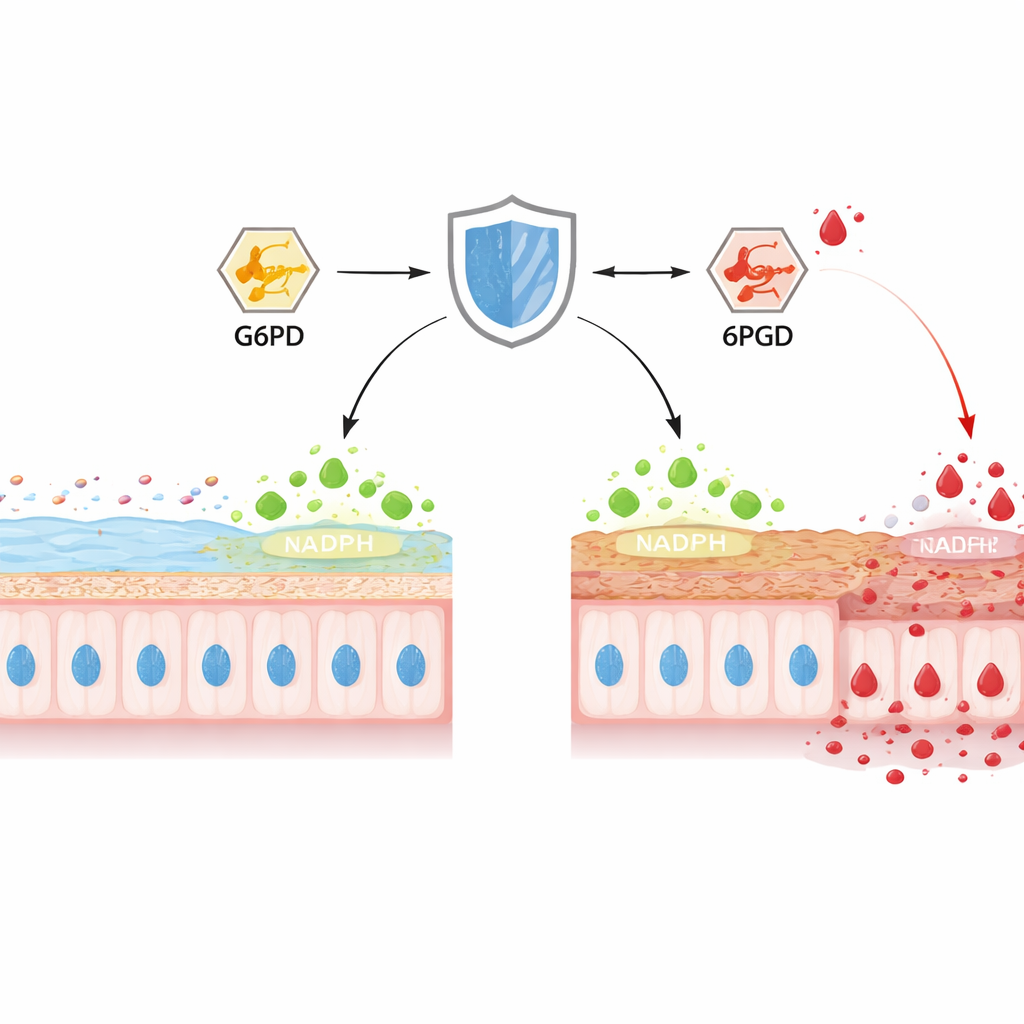
Dentro del colon, las células caliciformes fabrican constantemente MUC2, la principal proteína del moco que forma el gel protector interno. Los autores se centraron en TIGAR, una proteína conocida por dirigir la glucosa hacia una vía que produce NADPH, una «potencia reductora» clave que mantiene a raya a los oxidantes dañinos. En ratones con colitis inducida químicamente, los niveles de TIGAR en el colon disminuyeron a lo largo de varios días, justo cuando la capa de moco se afinaba, la superficie epitelial se erosionaba y las bacterias se acercaban al tejido. Cuando los investigadores eliminaron selectivamente TIGAR solo en el revestimiento intestinal de los ratones, la colitis comenzó antes y fue más severa, con criptas distorsionadas, menos células caliciformes y mucha menos MUC2 madura. Medidas de la química celular revelaron NADPH agotado, sistemas antioxidantes debilitados y picos de especies reactivas de oxígeno y nitrógeno, vinculando la pérdida de TIGAR con un intenso estrés oxidativo y el fallo de la barrera.
El uso de la glucosa se reorienta hacia una quema derrochadora
Para entender cómo TIGAR moldea el metabolismo, el equipo perfiló cientos de pequeñas moléculas en líneas celulares tipo caliciforme y en tejido de colon de ratón. La eliminación de TIGAR no cambió cuánto glucosa importaban las células ni la rapidez con que los animales consumían oxígeno, pero alteró profundamente el destino de esa glucosa. Usando azúcar marcada, mostraron que menos carbono circulaba por la vía de las pentosas fosfato —la principal fuente de NADPH— mientras que más se empujaba hacia la glucólisis clásica, terminando en lactato. Dos metabolitos llamaron la atención: el 6‑fosfogluconato, un punto clave en la vía de las pentosas, se acumuló fuertemente, y los niveles de lactato aumentaron en células y tejidos carentes de TIGAR, especialmente durante la colitis. Los datos de expresión génica sugirieron que las enzimas de la glucólisis estaban incrementadas, mientras que los niveles proteicos de dos enzimas clave de las pentosas fosfato, G6PD y 6PGD, no cambiaron, insinuando que su actividad —no su abundancia— estaba siendo bloqueada.
Una marca química que desactiva enzimas antioxidantes
Los investigadores identificaron entonces el mecanismo de bloqueo: la lactilación, una etiqueta química añadida a proteínas usando lactato como donante. En modelos de colitis y en cultivos celulares inflamados, la lactilación proteica general aumentó, y tanto G6PD como 6PGD presentaron altos niveles de esta modificación. La espectrometría de masas identificó posiciones específicas de lisina en cada enzima —K432 en G6PD y K38 en 6PGD— como sitios principales de lactilación. El modelado estructural y pruebas con mutaciones mostraron que modificar estos puntos interfiere con la formación del dímero activo de G6PD y con la unión del cofactor en 6PGD, reduciendo drásticamente su capacidad de generar NADPH. Bloquear la producción de lactato o impedir la lactilación en estos sitios restauró la actividad enzimática, aumentó el NADPH, redujo el estrés oxidativo y mejoró la maduración de MUC2. En ratones deficientes en TIGAR, la entrega de versiones mutantes de G6PD y 6PGD que no podían ser lactiladas preservó el grosor del moco y redujo la intrusión bacteriana en la capa interna.
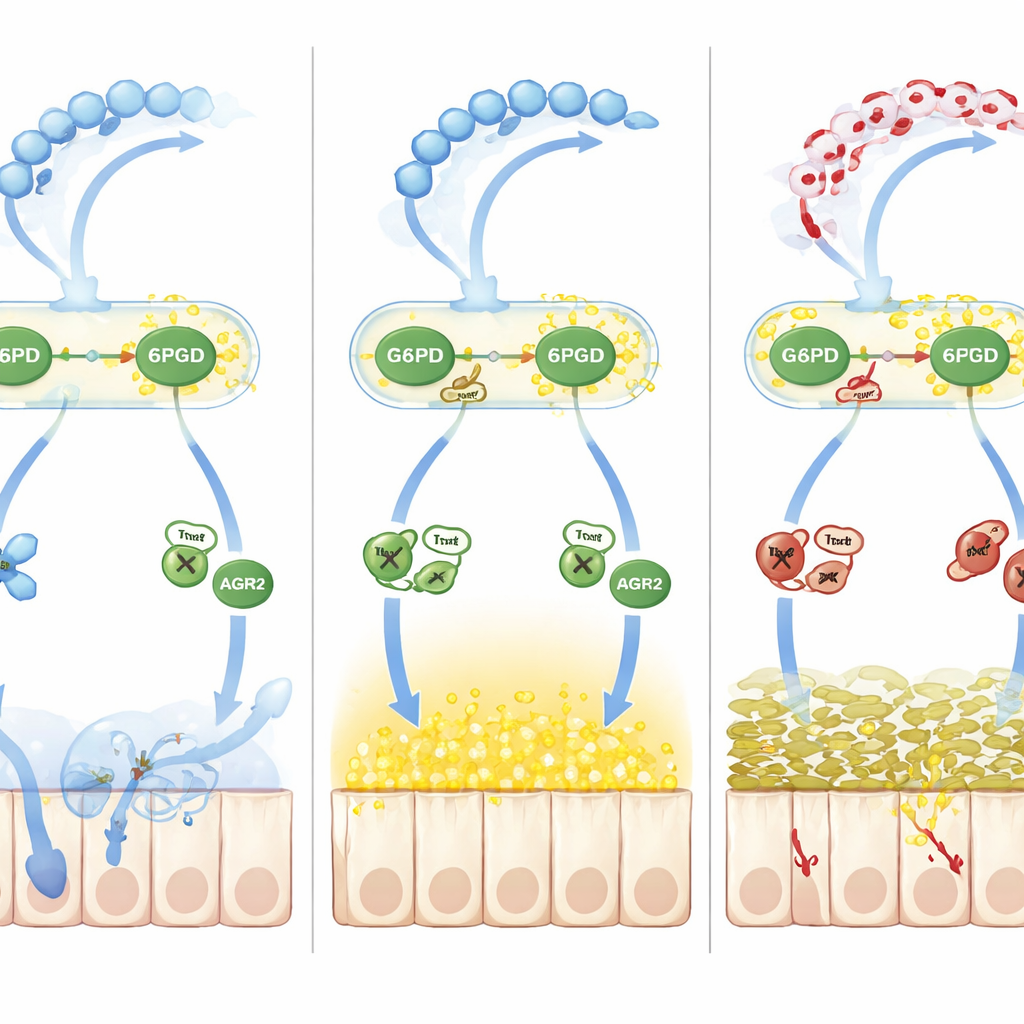
Cómo el desequilibrio redox descarrila el procesamiento del moco
Más allá de la simple oxidación, el equipo siguió una segunda ola de daño impulsada por el óxido nítrico. El aumento de óxido nítrico en la colitis incrementó la S‑nitrosilación, otra marca química reversible sobre residuos de cisteína. Una proteína chaperona de plegamiento llamada AGR2, esencial para convertir los precursores de MUC2 en su forma madura en el retículo endoplásmico, quedó fuertemente S‑nitrosilada en una cisteína crítica (Cys81). Este cambio debilitó la interacción de AGR2 con los precursores de MUC2, provocando acumulación de proteínas mal plegadas y elevación del estrés del retículo endoplásmico, reduciendo aún más el conjunto de moco correctamente formado. El intermediario clave fue la tioredoxina‑1 (Trx1), una enzima sensible al estado redox que puede tanto eliminar como transferir grupos nitrosilo según su propio estado de oxidación. Cuando el NADPH escaseó porque G6PD y 6PGD estaban lactiladas y lentas, Trx1 cambió de un modo denitrosilante protector a un modo transnitrosilante dañino, trasladando grupos nitrosilo a AGR2 y profundizando el defecto del moco.
Qué significa esto para las personas con colitis
En conjunto, el trabajo describe una reacción en cadena: la inflamación crónica reduce TIGAR en las células epiteliales intestinales; esto desvía la glucosa de las rutas productoras de NADPH, aumenta el lactato y lactila G6PD y 6PGD; la producción de NADPH cae, Trx1 se sobreoxida, AGR2 se nitrosila en exceso y MUC2 no madura, dejando la barrera mucosa delgada y permeable. Para un lector no especializado, el mensaje es que un cambio sutil en cómo las células intestinales queman azúcar puede traducirse en una brecha física en el escudo mucoso del intestino. Protegiendo la función de TIGAR, previniendo la lactilación dañina de G6PD y 6PGD, o reequilibrando la química de Trx1 y AGR2, tratamientos futuros podrían ayudar a reforzar la barrera mucosa y controlar la inflamación en la colitis ulcerosa.
Cita: Wu, D., Su, S., Zhang, P. et al. TIGAR regulates intestinal mucus barrier integrity by inhibiting lactylation of G6PD/6PGD in ulcerative colitis. Nat Commun 17, 3382 (2026). https://doi.org/10.1038/s41467-026-70263-z
Palabras clave: colitis ulcerosa, barrera mucosa intestinal, TIGAR, estrés oxidativo, metabolismo de la glucosa