Clear Sky Science · nl
TIGAR reguleert de integriteit van de intestinale slijmlaag door remming van lactylatie van G6PD/6PGD bij colitis ulcerosa
Waarom de slijmerige beschermlaag van de darm ertoe doet
Het slijmvlies van onze darmen is bedekt met een gladde slijmlaag die triljoenen microben op afstand houdt. Bij colitis ulcerosa, een chronische ziekte die de dikke darm ontstoken doet raken, dunner of scheurt dit beschermende laagje vaak, waardoor bacteriën en irriterende stoffen de darmwand kunnen bereiken. Deze studie onderzoekt waarom die slijmbarrière faalt, en volgt het verhaal van suikerstofwisseling in gespecialiseerde slijmproducerende cellen tot aan schade in de darm—met de nadruk op een molecuul genaamd TIGAR als een veelbelovend nieuw therapiedoelwit.
Een verborgen beschermer in darmcellen
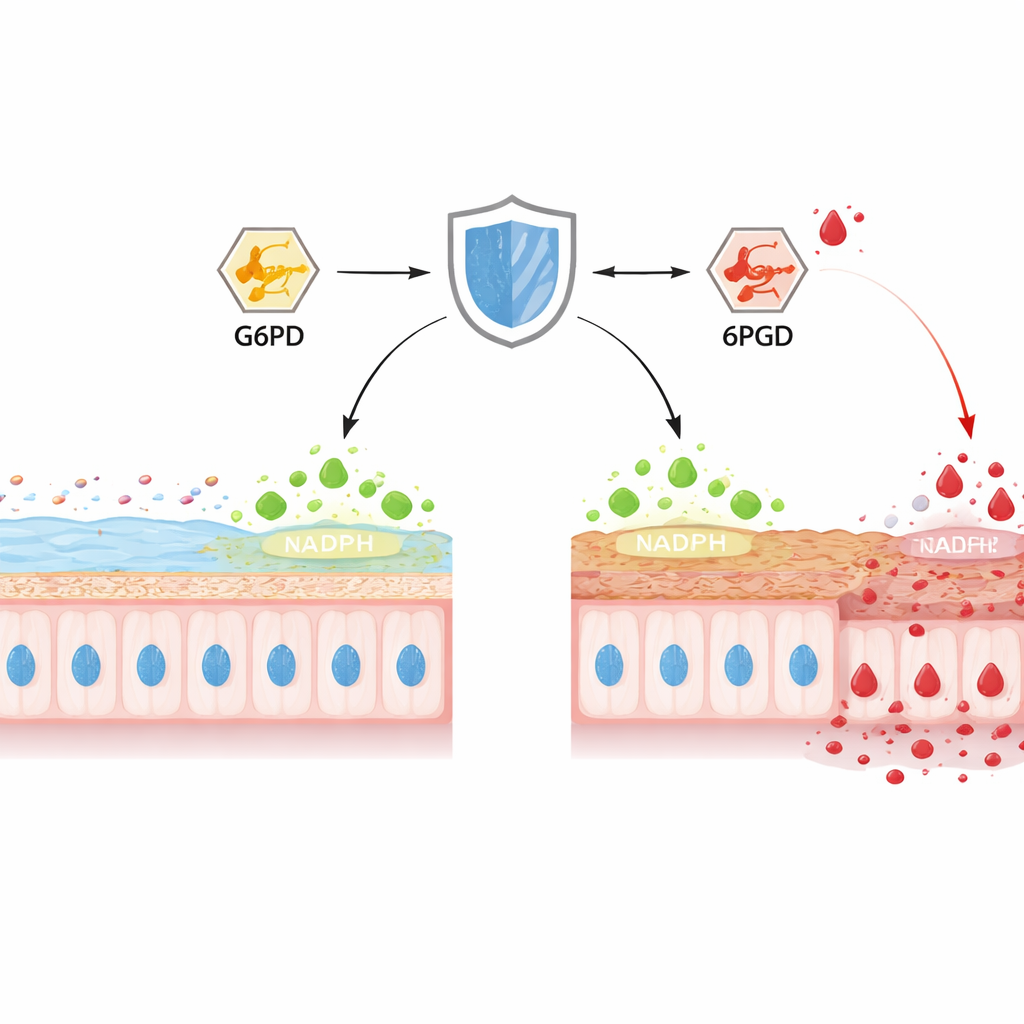
In de dikke darm maken gobletcellen continu MUC2 aan, het belangrijkste slijmeiwit dat de innerlijke beschermende gel vormt. De auteurs concentreerden zich op TIGAR, een eiwit dat eerder bekendstond om het sturen van glucose naar een route die NADPH produceert, een cruciale „reducerende kracht” die schadelijke oxidanten onder controle houdt. Bij muizen met chemisch geïnduceerde colitis daalde het TIGAR‑niveau in de dikke darm in de loop van enkele dagen, precies toen de slijmlaag dunner werd, het epitheliale oppervlak erosie vertoonde en bacteriën dichter bij het weefsel kwamen. Wanneer de onderzoekers TIGAR selectief verwijderden alleen in het darmepitheel van muizen, begon colitis eerder en werd ernstiger, met vervormde crypten, minder gobletcellen en aanzienlijk minder rijpe MUC2. Chemische metingen in cellen toonden uitgeputte NADPH, verzwakte antioxiderende systemen en pieken in reactieve zuurstof‑ en stikstofsoorten, waarmee het verlies van TIGAR werd gekoppeld aan intense oxidatieve stress en barrièrefalen.
Suikergebruik verlegd naar verspilde verbranding
Om te begrijpen hoe TIGAR de stofwisseling beïnvloedt, profilde het team honderden kleine moleculen in goblet‑achtige cellijnen en in muisdarmweefsel. Het weghalen van TIGAR veranderde niet hoeveel glucose cellen opnamen of hoe snel hele dieren zuurstof verbrandden, maar het wijzigde diepgaand het lot van die glucose. Met gelabelde suiker toonden ze aan dat minder koolstof door de pentosefosfaatroute stroomde—de belangrijkste bron van NADPH—terwijl meer werd geduwd naar klassieke glycolyse, eindigend in lactaat. Twee metabolieten vielen op: 6‑fosfogluconaat, een knooppunt in de pentosefosfaatroute, stapelde zich sterk op, en lactaatniveaus stegen in cellen en weefsels zonder TIGAR, vooral tijdens colitis. Genexpressiegegevens suggereerden dat enzymen van de glycolyse omhoog werden geschroefd, terwijl de eiwitniveaus van twee sleutelenzymen van de pentosefosfaatroute, G6PD en 6PGD, ongewijzigd bleven, wat impliceert dat hun activiteit—niet hun hoeveelheid—werd geblokkeerd.
Een chemische markering die antioxiderende enzymen uitschakelt
De onderzoekers ontdekten vervolgens het remmechanisme: lactylatie, een chemische markering die aan eiwitten wordt toegevoegd met lactaat als donor. In colitismodellen en in ontstekingscelkweken steeg de algehele eiwitlactylatie, en zowel G6PD als 6PGD droegen hoge niveaus van deze modificatie. Massaspectrometrie wees specifieke lysineposities op elk enzym aan—K432 op G6PD en K38 op 6PGD—als belangrijke lactylatieplaatsen. Structurele modellering en mutatietests toonden dat modificatie van deze plekken de manier waarop G6PD zijn actieve dimeer vormt en hoe 6PGD zijn cofactor bindt verstoort, waardoor hun vermogen om NADPH te genereren sterk afneemt. Het blokkeren van lactaatproductie of het voorkomen van lactylatie op deze sites herstelde enzymactiviteit, verhoogde NADPH, verlaagde oxidatieve stress en verbeterde MUC2‑rijping. Bij TIGAR‑deficiënte muizen behielden toegediende mutantversies van G6PD en 6PGD die niet konden worden gelactyleerd de dikte van het slijm en verminderden ze de bacteriële indringing in de binnenste laag.
Hoe redox‑onevenwicht de slijmverwerking ontspoort
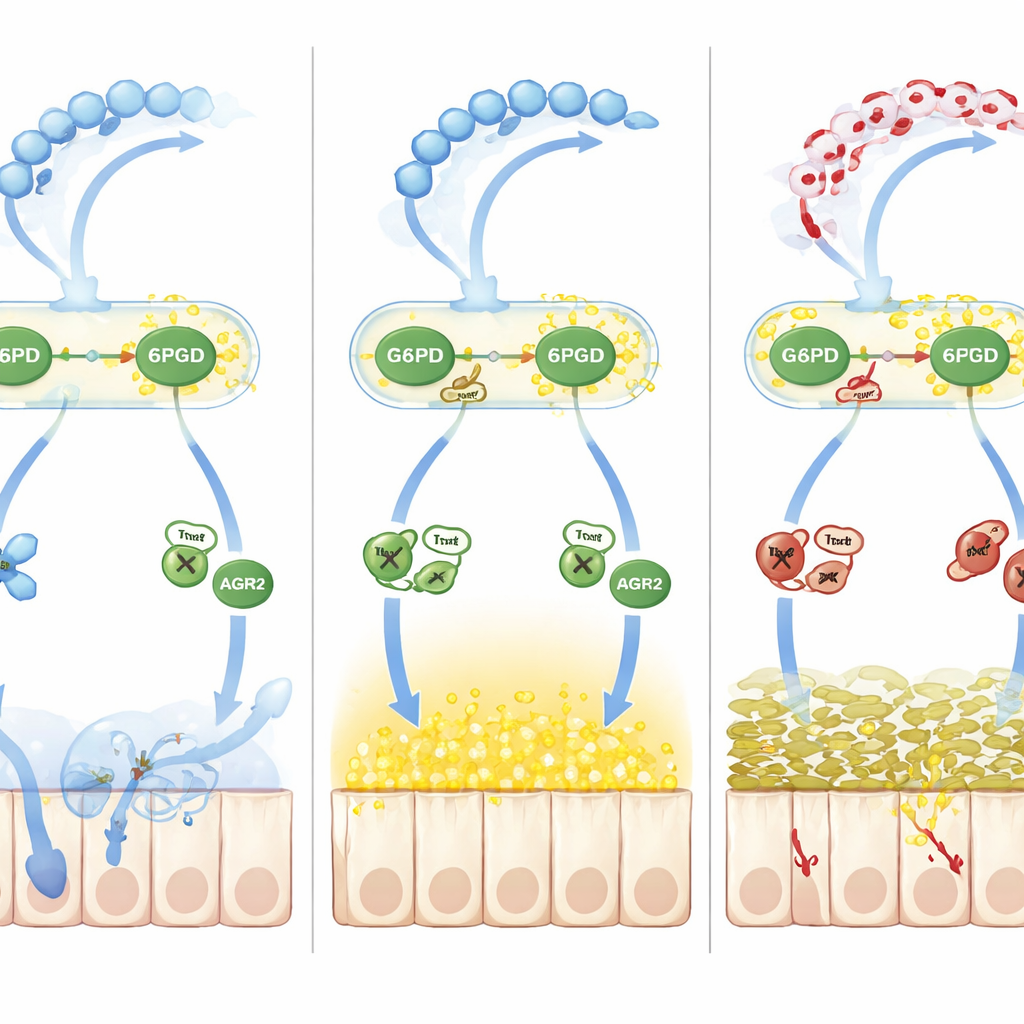
Voorbij eenvoudige oxidatie volgde het team een tweede golf van schade aangedreven door stikstofoxide. Verhoogd stikstofoxide bij colitis vergrootte S‑nitrosylatie, een andere omkeerbare chemische markering op cysteïneresiduen. Een vouwhulp‑eiwit genaamd AGR2, essentieel voor het omzetten van MUC2‑voorlopers naar hun rijpe vorm in het endoplasmatisch reticulum, werd sterk S‑nitrosyleerd bij een kritisch cysteïne (Cys81). Deze wijziging verzwakte AGR2’s binding aan MUC2‑voorlopers, waardoor misgevouwen eiwitten zich ophoopten en ER‑stress toenam, wat de voorraad correct gevormd slijm verder verkleinde. De cruciale tussenpersoon was thioredoxine‑1 (Trx1), een redox‑gevoelig enzym dat afhankelijk van zijn eigen oxidatietoestand ofwel nitrosylgroepen kan verwijderen of overdragen. Wanneer NADPH schaars was doordat G6PD en 6PGD gelactyleerd en traag waren, schakelde Trx1 van een beschermende denitrosylerende modus naar een schadelijke transnitrosylerende modus, waarbij nitrosylgroepen op AGR2 werden overgebracht en het slijmdefect werd verdiept.
Wat dit betekent voor mensen met colitis
Al met al schetst het werk een kettingreactie: chronische ontsteking verlaagt TIGAR in darmepitheelcellen; dit leidt ertoe dat glucose wordt weggevoerd van NADPH‑producerende routes, lactaat toeneemt en G6PD en 6PGD worden gelactyleerd; NADPH‑productie daalt, Trx1 raakt overgeoxideerd, AGR2 wordt overmatig nitrosyleerd en MUC2 rijpt niet goed, waardoor de slijmbarrière dun en lekkend wordt. Voor een niet‑specialistische lezer is de boodschap dat een subtiele verschuiving in hoe darmcellen suiker verbranden kan vertalen naar een tastbare scheuring in het slijmerige schild van de darm. Door TIGAR‑functie te beschermen, schadelijke lactylatie van G6PD en 6PGD te voorkomen, of de chemie van Trx1 en AGR2 te herbepalen, kunnen toekomstige behandelingen mogelijk de slijmbarrière versterken en de ontsteking bij colitis ulcerosa temmen.
Bronvermelding: Wu, D., Su, S., Zhang, P. et al. TIGAR regulates intestinal mucus barrier integrity by inhibiting lactylation of G6PD/6PGD in ulcerative colitis. Nat Commun 17, 3382 (2026). https://doi.org/10.1038/s41467-026-70263-z
Trefwoorden: colitis ulcerosa, intestinale slijmbarrière, TIGAR, oxidatieve stress, glucosestofwisseling