Clear Sky Science · pl
TIGAR reguluje integralność jelitowej bariery śluzowej przez hamowanie laktylacji G6PD/6PGD w wrzodziejącym zapaleniu jelita grubego
Dlaczego śluzowa tarcza jelit ma znaczenie
Wyściółka naszych jelit jest pokryta śluzową warstwą, która utrzymuje biliony mikroorganizmów w bezpiecznej odległości. W wrzodziejącym zapaleniu jelita grubego — przewlekłej chorobie wywołującej zapalenie okrężnicy — ta ochronna powłoka często się przerzedza lub ulega uszkodzeniu, umożliwiając bakteriom i drażniącym czynnikom dotarcie do ściany jelita. Niniejsze badanie bada, dlaczego bariera śluzowa zawodzi, prowadząc ślad od metabolizmu cukrów w wyspecjalizowanych komórkach wydzielających śluz aż do uszkodzeń jelita — i wskazuje cząsteczkę zwaną TIGAR jako obiecujący nowy cel terapeutyczny.
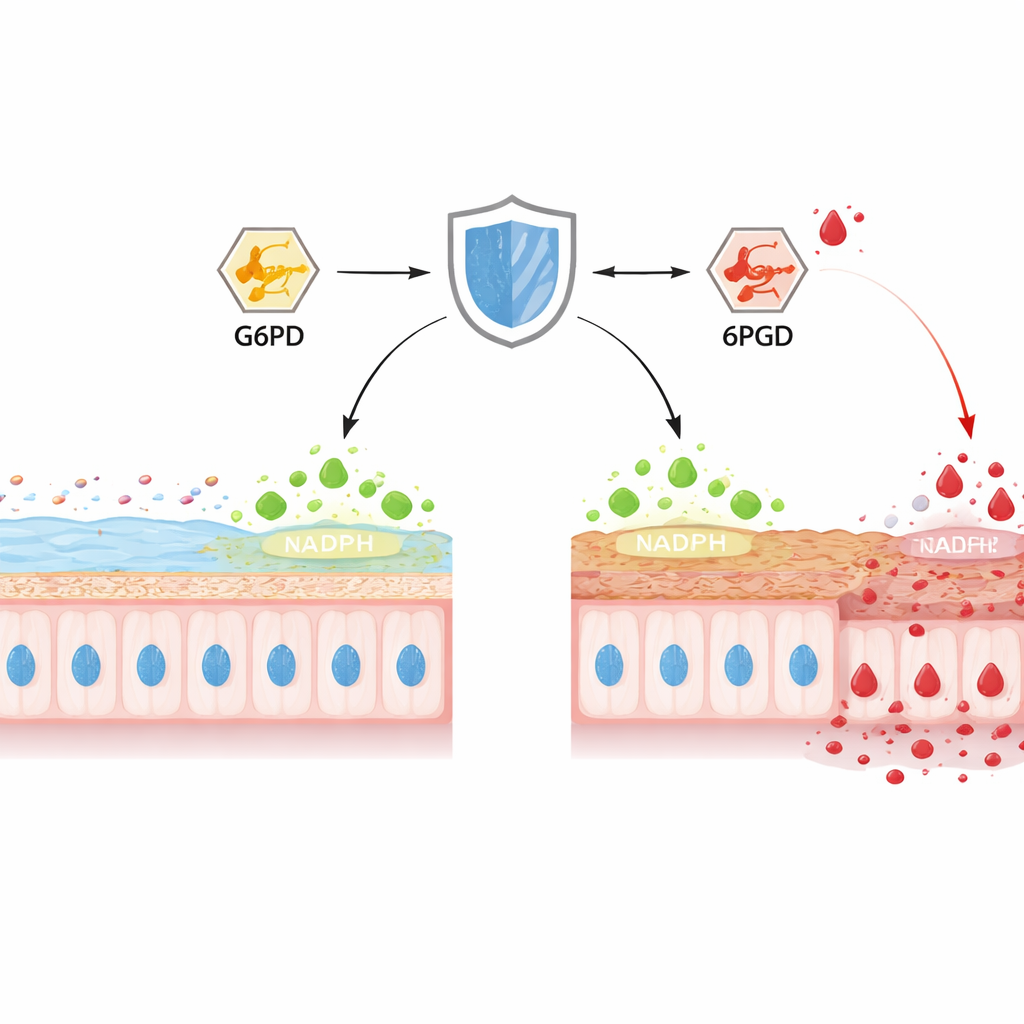
Ukryty obrońca w komórkach jelit
W wnętrzu jelita grubego komórki kubkowe stale wytwarzają MUC2, główne białko śluzu tworzące wewnętrzny żel ochronny. Autorzy skupili się na TIGAR — białku wcześniej znanym z kierowania glukozy do ścieżki wytwarzającej NADPH, kluczową „moc redukującą” utrzymującą pod kontrolą szkodliwe utleniacze. U myszy z chemicznie wywołanym zapaleniem okrężnicy poziomy TIGAR w jelicie spadały w ciągu kilku dni, równocześnie z przerzedzeniem warstwy śluzowej, erozją powierzchni nabłonka i zbliżaniem się bakterii do tkanki. Gdy badacze selektywnie usunęli TIGAR wyłącznie w wyścielającej jelito warstwie u myszy, zapalenie zaczynało się wcześniej i przebiegało ciężej, z zniekształconymi kryptami, mniejszą liczbą komórek kubkowych i wyraźnym spadkiem dojrzałego MUC2. Pomiary chemii komórkowej ujawniły wyczerpanie NADPH, osłabienie systemów antyoksydacyjnych oraz wzrost reaktywnych form tlenu i azotu, łącząc utratę TIGAR z intensywnym stresem oksydacyjnym i utratą bariery.
Wykorzystanie cukru przebudowane na nieefektywne spalanie
Aby zrozumieć, jak TIGAR kształtuje metabolizm, zespół przeanalizował setki małych cząsteczek w liniach komórkowych przypominających komórki kubkowe oraz w tkance jelita myszy. Usunięcie TIGAR nie zmieniło tego, ile glukozy komórki importowały ani jak szybko całe zwierzęta zużywały tlen, ale głęboko zmieniło los tej glukozy. Używając znakowanej sacharozy (glukozy), wykazali, że mniej atomów węgla przepływało przez szlak pentozofosforanowy — główne źródło NADPH — podczas gdy więcej kierowało się do klasycznej glikolizy, kończącej się wytworzeniem mleczanu. Wyraźnie wyróżniały się dwa metabolity: 6‑fosfoglukonian, centrum szlaku pentozofosforanowego, akumulował się silnie, a poziomy mleczanu wzrastały w komórkach i tkankach pozbawionych TIGAR, szczególnie podczas zapalenia. Dane dotyczące ekspresji genów sugerowały, że enzymy glikolizy zostały wzmocnione, podczas gdy poziomy białek dwóch kluczowych enzymów szlaku pentozofosforanowego, G6PD i 6PGD, pozostały niezmienione, co sugeruje, że blokowana była ich aktywność — nie obfitość.
Chemiczny znacznik, który neutralizuje enzymy antyoksydacyjne
Następnie badacze odkryli mechanizm blokujący: laktylacja, chemiczny znacznik dodawany do białek z wykorzystaniem mleczanu jako donora. W modelach zapalenia i w hodowlach komórek zapalnych całkowita laktylacja białek wzrastała, a zarówno G6PD, jak i 6PGD wykazywały wysokie poziomy tej modyfikacji. Spektrometria mas precyzyjnie wskazała konkretne pozycje lizyn na każdym enzymie — K432 w G6PD i K38 w 6PGD — jako główne miejsca laktylacji. Modelowanie strukturalne i testy mutacyjne pokazały, że modyfikacja tych miejsc zakłóca tworzenie aktywnego dimeru przez G6PD oraz wiązanie kofaktora przez 6PGD, ostro zmniejszając ich zdolność do generowania NADPH. Hamowanie produkcji mleczanu lub zapobieganie laktylacji w tych miejscach przywracało aktywność enzymów, zwiększało NADPH, obniżało stres oksydacyjny i poprawiało dojrzewanie MUC2. U myszy pozbawionych TIGAR podawanie mutantów G6PD i 6PGD, które nie mogły być laktylowane, zachowało grubość śluzu i zmniejszyło wtargnięcie bakterii do wewnętrznej warstwy.
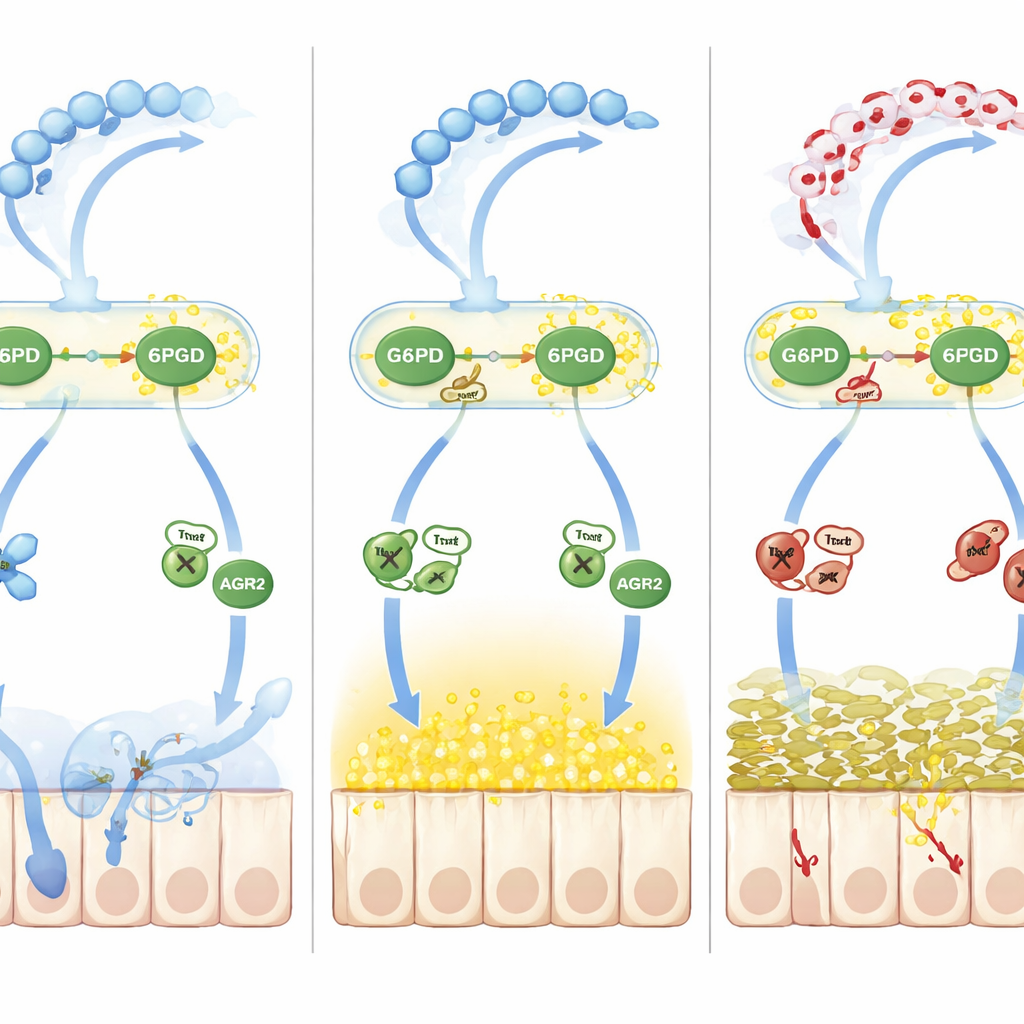
Jak nierównowaga redoks zaburza przetwarzanie śluzu
Ponad prostą oksydacją zespół prześledził drugą falę uszkodzeń napędzaną przez tlenek azotu. Podwyższony tlenek azotu w zapaleniu zwiększał S‑nitrozylację, inną odwracalną modyfikację chemiczną reszt cysteinowych. Białko pomocnicze w fałdowaniu zwane AGR2, niezbędne do przekształcania prekursora MUC2 w jego dojrzałą formę w retikulum endoplazmatycznym, stało się silnie S‑nitrozylowane w krytycznej cysteinie (Cys81). Ta zmiana osłabiła wiązanie AGR2 z prekursorami MUC2, powodując akumulację nieprawidłowo sfałdowanych białek i wzrost stresu retikulum endoplazmatycznego, dalej zmniejszając pulę prawidłowo uformowanego śluzu. Kluczowym pośrednikiem był tioredoksyna‑1 (Trx1), enzym wrażliwy na stan redoks, który może usuwać lub przenosić grupy nitrozylowe w zależności od własnego stanu utlenienia. Gdy NADPH było rzadkie z powodu laktylacji i spowolnienia G6PD i 6PGD, Trx1 przestawiał się z trybu ochronnego denitrozylującego na szkodliwy tryb transnitrozylujący, przesyłając grupy nitrozylowe na AGR2 i pogłębiając defekt śluzowy.
Co to oznacza dla osób z zapaleniem
W sumie praca nakreśla reakcję łańcuchową: przewlekłe zapalenie obniża poziom TIGAR w komórkach nabłonka jelitowego; to zmienia kierunek wykorzystania glukozy z dróg wytwarzających NADPH, zwiększa poziom mleczanu i prowadzi do laktylacji G6PD i 6PGD; produkcja NADPH spada, Trx1 ulega nadmiernemu utlenieniu, AGR2 jest nadmiernie nitrozylowany, a MUC2 nie dojrzewa prawidłowo, pozostawiając barierę śluzową cienką i nieszczelną. Dla czytelnika popularnonaukowego przesłanie jest takie, że subtelne przesunięcie sposobu, w jaki komórki jelit spalają cukier, może przełożyć się na namacalny uszczerbek w śluzowej tarczy jelita. Ochrona funkcji TIGAR, zapobieganie szkodliwej laktylacji G6PD i 6PGD lub przywrócenie równowagi chemii Trx1 i AGR2 może w przyszłości pomóc wzmocnić barierę śluzową i złagodzić zapalenie we wrzodziejącym zapaleniu jelita grubego.
Cytowanie: Wu, D., Su, S., Zhang, P. et al. TIGAR regulates intestinal mucus barrier integrity by inhibiting lactylation of G6PD/6PGD in ulcerative colitis. Nat Commun 17, 3382 (2026). https://doi.org/10.1038/s41467-026-70263-z
Słowa kluczowe: wrzodziejące zapalenie jelita grubego, jelitowa bariera śluzowa, TIGAR, stres oksydacyjny, metabolizm glukozy