Clear Sky Science · sv
Förlust av ATRX kopplar genominstabilitet vid en G-rik upprepning till dysreglering av människans alfa-globinuttryck
Varför detta är viktigt för blod och cancer
Våra röda blodkroppar är beroende av noggrant reglerade gener som bygger hemoglobin, det protein som transporterar syre. Ett protein som kallas ATRX sitter på DNA och hjälper till att hålla det stabilt; mutationer i ATRX ger upphov till en ärftlig anemi med intellektuell funktionsnedsättning och förekommer ofta i flera cancerformer. Denna studie använder alpha-globin-genklustret som ett fall för att visa, på molekylär nivå, hur förlust av ATRX kan skada DNA vid ett repetitivt stycke och tyst slå av närliggande gener. Att förstå denna händelsekedja hjälper till att förklara en sällsynt mänsklig sjukdom och belyser hur genominstabilitet mer generellt kan förändra genaktivitet.
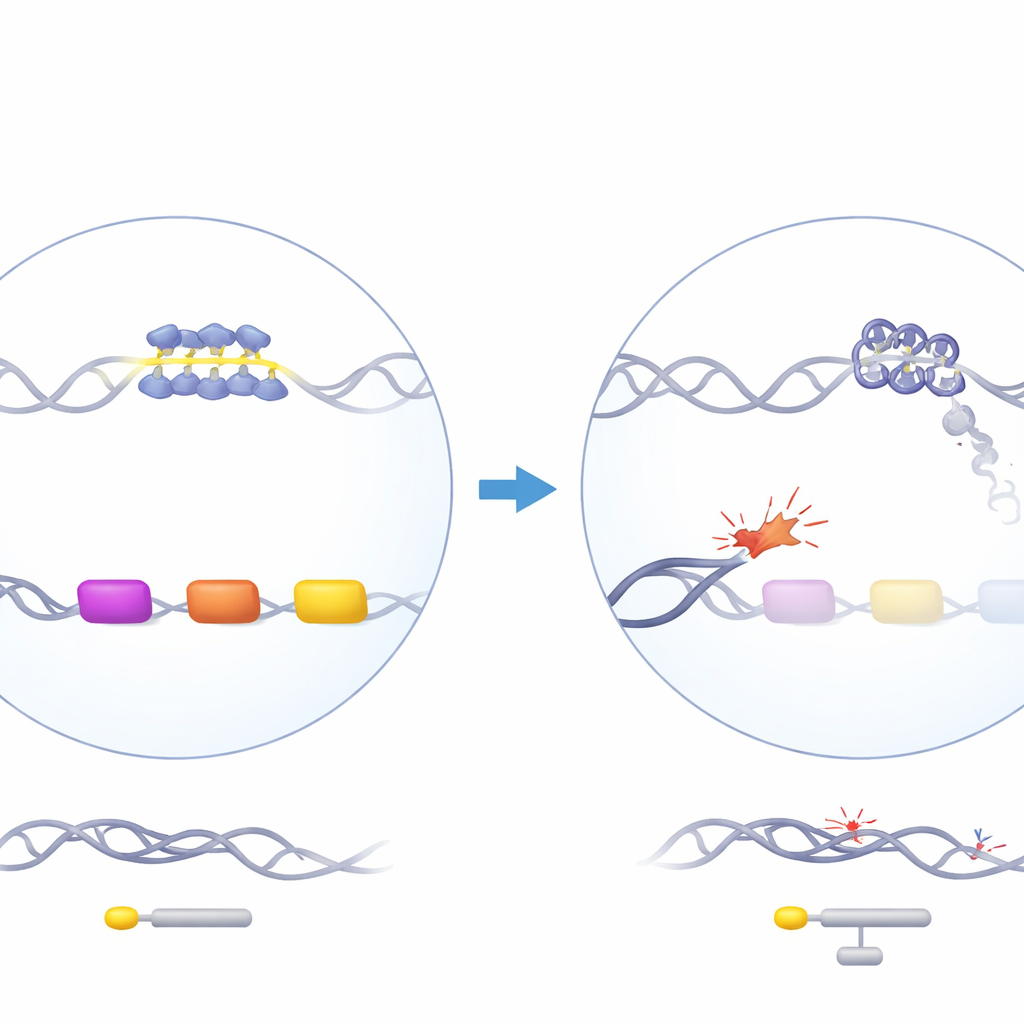
En skyddsprotein med en förbryllande effekt
ATRX är ett kromatinremodelleringsprotein som hjälper till att organisera DNA och deltar i replikation, transkription och DNA-reparation. När ATRX är muterat hos människor utvecklar patienterna ATR-X-syndrom, vilket inkluderar mild alfa-talassemi: deras alfa-globingeners aktivitet, nödvändig för att bygga hemoglobin, är nedsatt. Intressant nog påverkar förlust av ATRX alfa-globin men inte beta-globin, trots att båda behövs i lika mängd. Alfa-globingenarna ligger i ett genrikt, GC-rikt område på kromosom 16 som innehåller flera repetitiva DNA-element, inklusive en särskilt G-rik variabelt antal tandemupprepning (VNTR) belägen precis uppströms om de alfa-liknande globingenrna. Tidigare genetiskt arbete visade att längden på denna upprepning korrelerar med hur starkt alfa-globin är reducerat hos patienter, vilket tyder på att detta ovanliga DNA-stycke kan vara centralt för problemet.
Zooma in på de drabbade cellerna
För att undersöka detta tog författarna bort ATRX i mänskliga blodstam- och progenitorceller med CRISPR-genredigering och mognade sedan dessa celler till röda blodkroppsförstadier i kultur. En analys av cellpopulationen som helhet visade endast en måttlig minskning av en alfa-lik gen, HBM, och inga stora förändringar i andra globingenrer, vilket speglar de blygsamma blodförändringar som ses hos patienter. När de däremot analyserade enskilda kolonier och enskilda celler framträdde en annan bild. Endast en delmängd av ATRX-defekta celler visade en kraftig reduktion av HBM och i mindre grad av huvud-alfa-globingenarna. Dessa samma celler uppvisade tecken på aktiverat DNA-skaderespons, inklusive ökade markörer för brott på DNA och förhöjd modifiering av ett histonprotein (H2A) som är kopplat till reparation av skador och tystning av närliggande gener. Detta antyder att nedreglering av alfa-globin huvudsakligen sker i celler där förlust av ATRX har tillåtit lokal DNA-skada att ackumuleras.
En besvärlig G-rik upprepning som svag punkt
Teamet fokuserade sedan på den G-rika VNTR som är inbäddad i en närliggande pseudogen kallad HBZP1. Med en immortaliserad mänsklig erytroid cellinje spårade de ATRX-bindning över alpha-globin-området och fann att ATRX specifikt rekryteras till denna VNTR när den omgivande DNA-sekvensen transkriberas. De byggde ett system där ATRX snabbt kunde degraderas och observerade att förlust av ATRX minskade HBM-uttrycket, återgivande sjukdomsfenotypen. Slående nog, när de raderade själva VNTR från genomet, minskade inte HBM-nivåerna längre vid borttag av ATRX. Läkemedel som stabiliserar ovanliga fyrsträngade DNA-strukturer kända som G-kvadrupel gav en liknande nedgång i HBM-uttryck, men endast när VNTR fanns kvar. Genomomfattande analyser visade att många andra gener som felregleras vid ATRX-förlust också innehåller GC-rika repetitiva element, vilket pekar på en generell sårbarhet vid sådana platser.
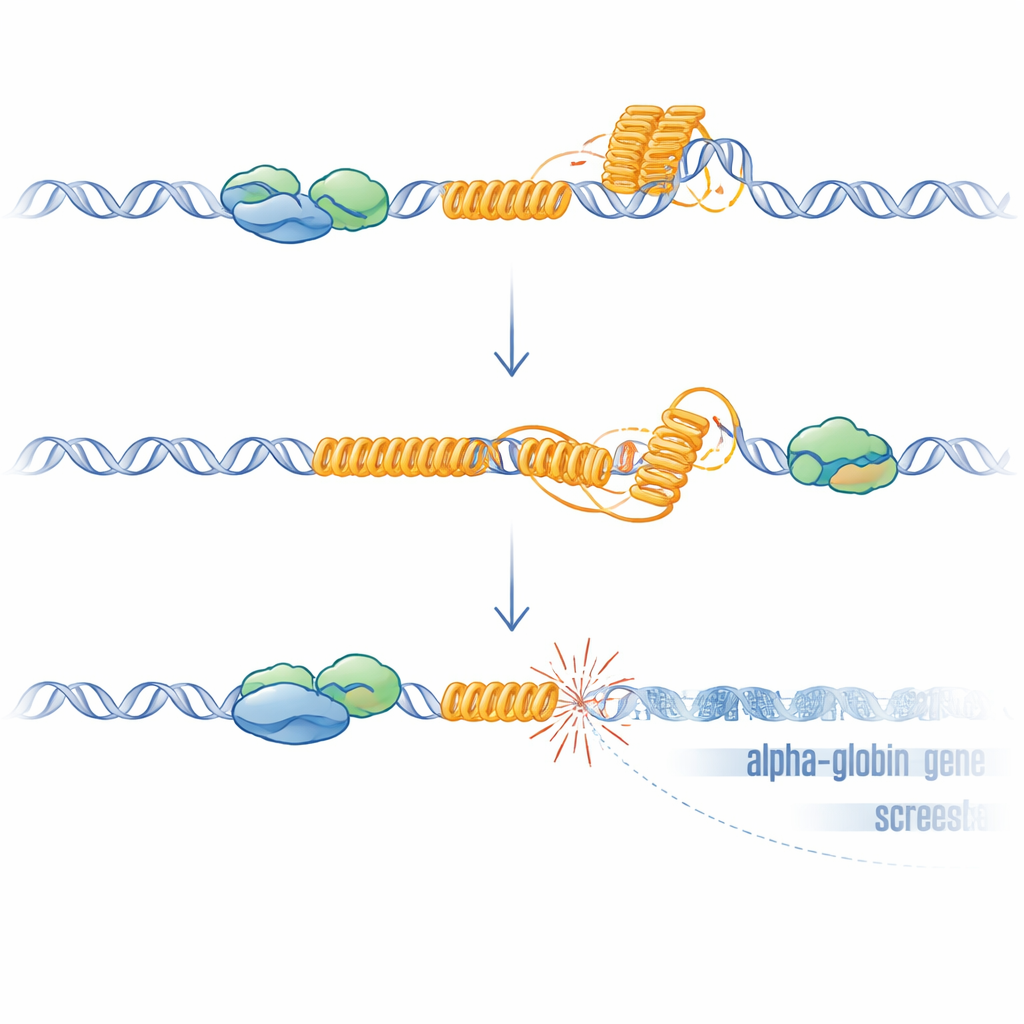
Från märkliga DNA-former till brutna gener
G-rika upprepningar som denna VNTR kan veckas till G-kvadrupelstrukturer och främja bildning av R-loopar, hybridstrukturer där nyligen syntetiserat RNA fastnar på DNA-mallen. Båda strukturerna kan bromsa eller stanna maskineriet som kopierar och läser DNA, vilket orsakar stress och brott. Forskarna visade att utan ATRX ökade R-looparna över genomet och var särskilt förhöjda vid VNTR. När de överuttryckte RNas H, ett enzym som tar bort R-loopar, återhämtade sig HBM-uttrycket delvis, vilket stödjer en orsakssamband för dessa strukturer. För att testa om DNA-skada ensam var tillräcklig för att tysta närliggande gener använde de CRISPR för att skapa riktade brott precis uppströms om HBM i celler där VNTR hade raderats. Dessa artificiella brott, även i frånvaro av upprepningen, minskade återigen HBM och, i mindre grad, alfa-globingenrna, där den närmaste genen påverkades mest. Denna avståndsberoende effekt matchar vad som ses hos patienter och är förenlig med välkänd spridning av transkriptionell repression från platser för dubbelsträngsbrott.
Vad detta betyder för sjukdom och vidare
Sammantaget beskriver arbetet en tydlig modell: i friska celler binder ATRX till en G-rik upprepning nära alfa-globingenarna under transkription och hjälper till att förebygga eller lösa G-kvadrupelstrukturer och R-loopar och skyddar därmed regionen från DNA-skada. När ATRX saknas ackumuleras dessa ovanliga DNA- och RNA-strukturer vid upprepningen, vilket leder till lokala DNA-brott, aktivering av en skaderespons och ett repressivt kromatinläge som dämpar uttrycket av närliggande gener i en avståndsberoende manér, med HBM som drabbas hårdast. Denna mekanism förklarar varför ATR-X-syndrom endast orsakar mild, fläckvis alfa-talassemi, varför svårighetsgraden varierar med upprepningens längd och varför musmodeller som saknar denna människaspecifika upprepning inte visar samma bloddefekt. Mer allmänt antyder det att repetitiva, G-rika sekvenser spridda i vårt genom kan fungera som dolda sprickzoner: om skyddande faktorer som ATRX sviktar kan de bli hotspotpar för instabilitet som tyst omprogrammerar genaktivitet under utveckling, åldrande och cancer.
Citering: Shen, Y., Gupta, K., Tan-Wong, S.M. et al. ATRX loss couples genome instability at a G-rich repeat to dysregulation of human alpha-globin expression. Nat Commun 17, 2749 (2026). https://doi.org/10.1038/s41467-026-69169-7
Nyckelord: ATRX, alfa-globin, DNA-skada, G-kvadrupel, R-loopar