Clear Sky Science · ja
Gリッチ反復配列でのゲノム不安定性とヒトαグロビン発現の異常調節を結びつけるATRX欠失
血液とがんにとっての意義
赤血球は酸素を運ぶタンパク質ヘモグロビンを生成する遺伝子の精密な制御に依存しています。ATRXと呼ばれるタンパク質はDNA上に働きかけて安定性を保ち、ATRXの変異は知的障害を伴う遺伝性貧血の一形態を引き起こし、いくつかのがんで一般的に見られます。本研究はα-グロビン遺伝子クラスターをモデルとして用い、ATRXを失うことが反復配列上のDNAを損傷させ、近傍の遺伝子を静かにオフにする仕組みを分子レベルで示しています。この一連の出来事を理解することで、希少なヒト疾患の説明に役立つとともに、ゲノム不安定性が広く遺伝子活性をどのように変えうるかについての洞察が得られます。
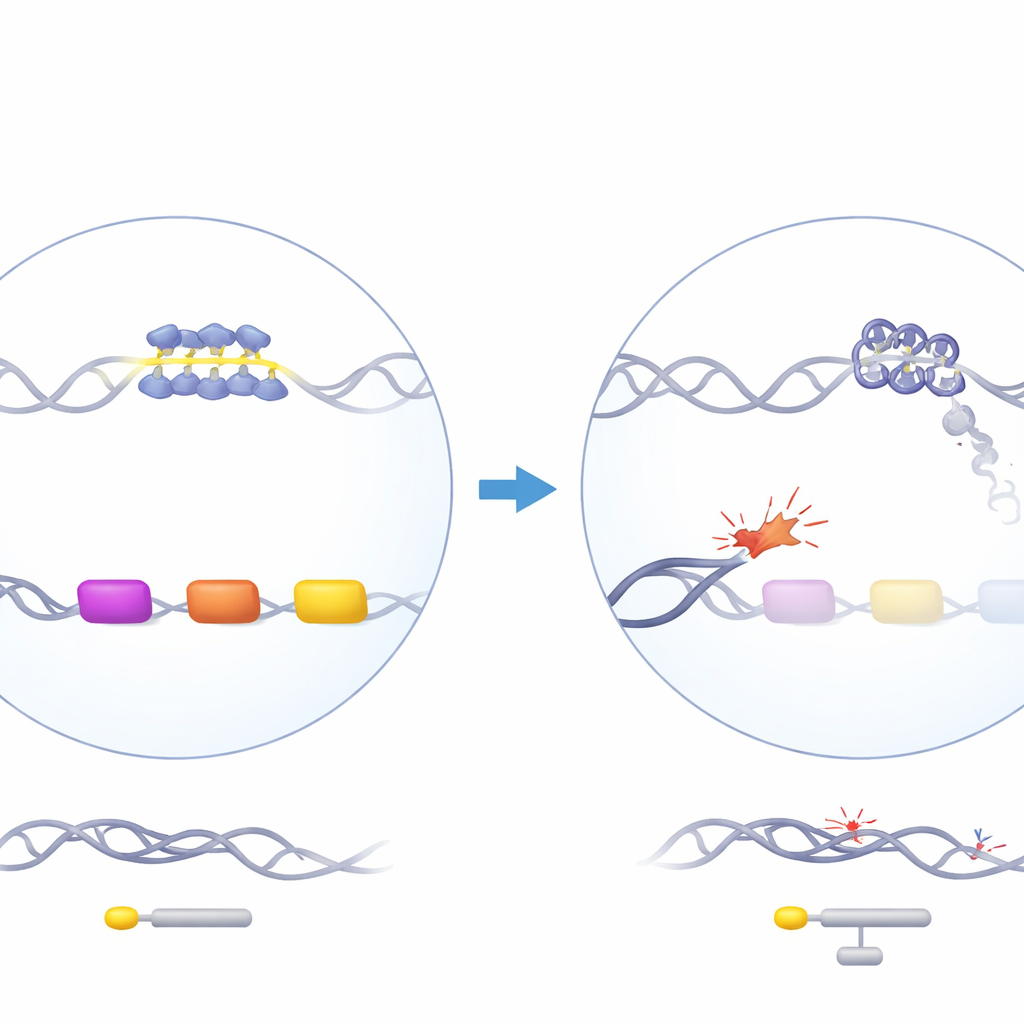
不可解な影響をもつ守護者タンパク質
ATRXはクロマチンリモデリング因子で、DNAの配置を助け、複製、転写、DNA修復に関与します。ヒトでATRXが変異すると、患者はATR-X症候群を発症し、軽度のαサラセミアを含みます:ヘモグロビン合成に必要なα-グロビン遺伝子の働きが低下します。興味深いことに、ATRX欠失はβ-グロビンではなくα-グロビンに影響を与しますが、どちらも等しい量が必要です。α-グロビン遺伝子は染色体16上の遺伝子に富みGC含量の高い領域に位置し、いくつかの反復DNA要素を含みます。特にα様グロビン遺伝子の直上流に位置するGに富む可変数タンデム反復(VNTR)が注目されます。以前の遺伝学的研究は、この反復の長さが患者におけるα-グロビン低下の強さと相関することを示しており、この特徴的なDNA配列が問題の中心である可能性を示唆していました。
影響を受ける細胞を拡大して観察
調査のため、著者らはCRISPR遺伝子編集を用いてヒトの造血幹・前駆細胞からATRXを除去し、それらを培養で赤血球前駆細胞へ成熟させました。集団として細胞を観察すると、α様遺伝子の一つであるHBMに軽度の低下が見られ、他のグロビン遺伝子には大きな変化はなく、患者で観察される穏やかな血液学的変化を反映していました。しかし、単一コロニーや単一細胞を解析すると異なる光景が現れました。ATRX欠失細胞の一部のみがHBMの強い低下と、やや程度は小さいが主要なα-グロビン遺伝子の低下を示しました。これらの同一の細胞は、DNA損傷応答の活性化を示す指標、すなわち切断されたDNAの増加や損傷修復・近傍遺伝子沈黙に関連するヒストンタンパク質(H2A)の修飾増加を示しました。これは、α-グロビンの発現低下が主にATRX欠失により局所的なDNA損傷が蓄積した細胞で起きることを示唆します。
弱点としての問題あるGリッチ反復
研究チームは隣接する偽遺伝子HBZP1に埋め込まれたGリッチなVNTRに注目しました。不死化ヒト赤芽球系細胞株を用い、α-グロビン領域全体でのATRX結合を追跡したところ、転写が行われている際にATRXが特異的にこのVNTRへリクルートされることが分かりました。ATRXを速やかに分解できる系を設計すると、ATRXを失うことでHBM発現が低下し、疾患表現型を再現しました。注目すべきは、ゲノムからVNTR自体を削除すると、ATRXを除去してもHBMレベルは低下しなくなることです。G四重鎖と呼ばれる特異な四本鎖DNA構造を安定化する薬は同様のHBM発現低下を引き起こしましたが、これはVNTRが存在する場合に限られました。ゲノムワイド解析は、ATRX欠失で誤制御される他の多くの遺伝子もGCに富む反復要素を含んでいることを示し、そのような部位に一般的な脆弱性があることを示唆しました。
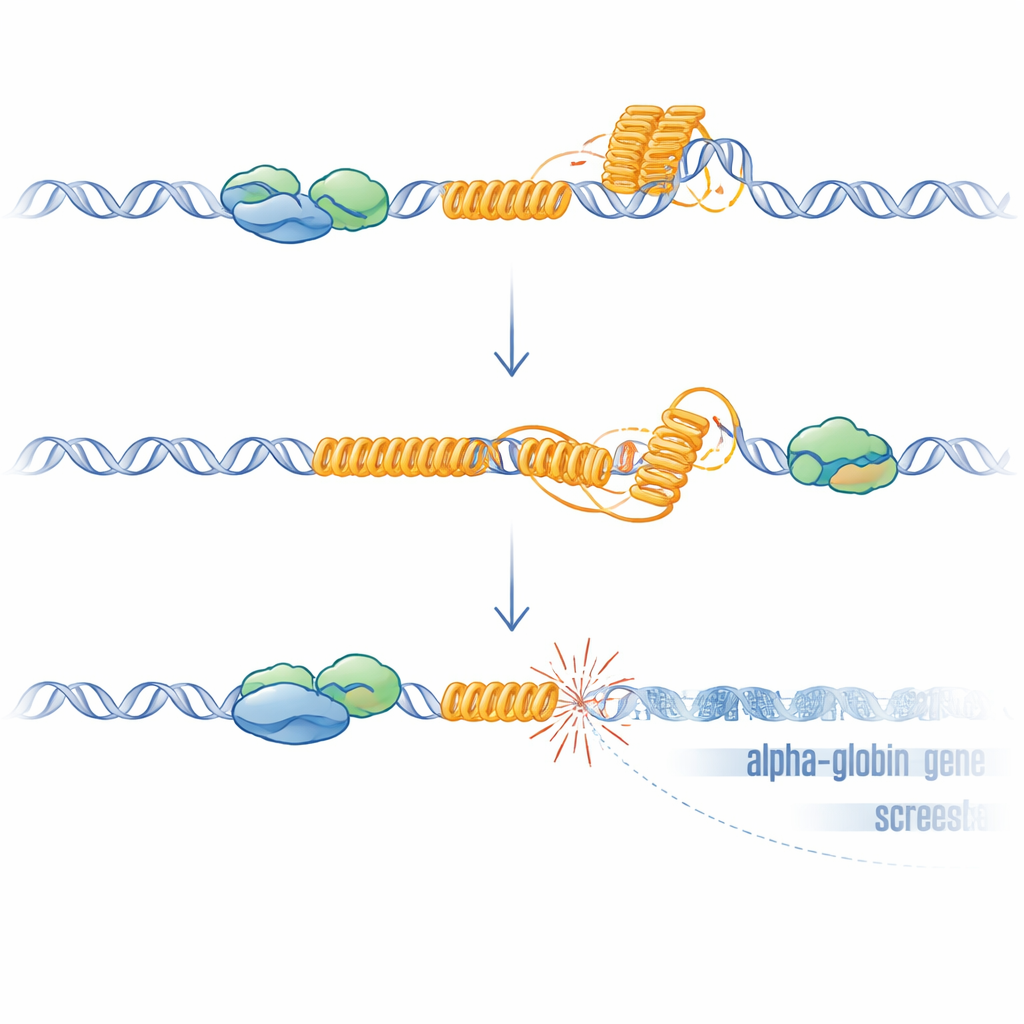
奇妙なDNA構造から壊れた遺伝子へ
このVNTRのようなGに富む反復配列はG四重鎖を形成し、生成されたRNAが鋳型DNAに付着したままになるRループの形成を促進します。これら両方の構造はDNAを複製・読み取る機構を遅らせたり停止させたりし、ストレスや切断を引き起こします。研究者らは、ATRXがないとRループがゲノム全体で増加し、特にVNTRで顕著になることを示しました。Rループを除去する酵素であるRNase Hを過剰発現させるとHBM発現が部分的に回復し、これらの構造が因果的役割を果たすことを支持しました。DNA損傷だけで近傍遺伝子がサイレンシングされるかを試すために、彼らはVNTRが削除された細胞でHBM直上流にCRISPRを用いて標的的な切断を作成しました。これらの人工的切断は、反復がない場合でも再びHBMを低下させ、より弱い影響ながらα-グロビン遺伝子も低下させ、最も近い遺伝子が最も影響を受けました。この距離依存的な効果は患者で見られる現象と一致し、二本鎖切断部位からの転写抑制の既知の広がりと整合します。
疾患とそれ以上の意味
総合すると、この研究は明確なモデルを提示します:健常な細胞では、ATRXは転写の際にα-グロビン遺伝子近傍のGリッチ反復に結合し、G四重鎖やRループを防いだり解消したりすることで、その領域をDNA損傷から守ります。ATRXが欠けると、これらの異常なDNAおよびRNA構造が反復部位に蓄積し、局所的なDNA切断、損傷応答の活性化、近傍遺伝子の発現を抑える抑制的なクロマチン環境を引き起こします。この効果は距離依存的で、HBMが最も強く影響を受けます。この機構はATR-X症候群がなぜ軽度で局所的なαサラセミアを引き起こすのか、反復長が重症度となぜ相関するのか、そしてこのヒト特異的な反復を欠くマウスモデルが同じ血液異常を示さない理由を説明します。より広くは、ゲノムに散在する反復的でGに富む配列は隠れた弱点として機能し得て、ATRXのような保護因子が失われると不安定性のホットスポットとなり、発生、老化、がんで遺伝子活性を静かに書き換える可能性があることを示唆しています。
引用: Shen, Y., Gupta, K., Tan-Wong, S.M. et al. ATRX loss couples genome instability at a G-rich repeat to dysregulation of human alpha-globin expression. Nat Commun 17, 2749 (2026). https://doi.org/10.1038/s41467-026-69169-7
キーワード: ATRX, α-グロビン, DNA損傷, G四重鎖, Rループ