Clear Sky Science · pt
Perda de ATRX conecta instabilidade genômica em um repetido rico em G à desregulação da expressão do alfa-globina humana
Por que isso importa para sangue e câncer
Nossas hemácias dependem de um controle fino dos genes que produzem a hemoglobina, a proteína que transporta oxigênio. Uma proteína chamada ATRX se liga ao DNA e ajuda a mantê-lo estável; mutações em ATRX causam uma forma hereditária de anemia com deficiência intelectual e são comuns em vários tipos de câncer. Este estudo usa o cluster do gene da alfa-globina como caso de teste para mostrar, em detalhe molecular, como a perda de ATRX pode danificar o DNA em um trecho repetitivo e silenciar discretamente genes próximos. Entender essa cadeia de eventos ajuda a explicar um distúrbio humano raro e esclarece como a instabilidade genômica pode alterar a atividade gênica de forma mais ampla.
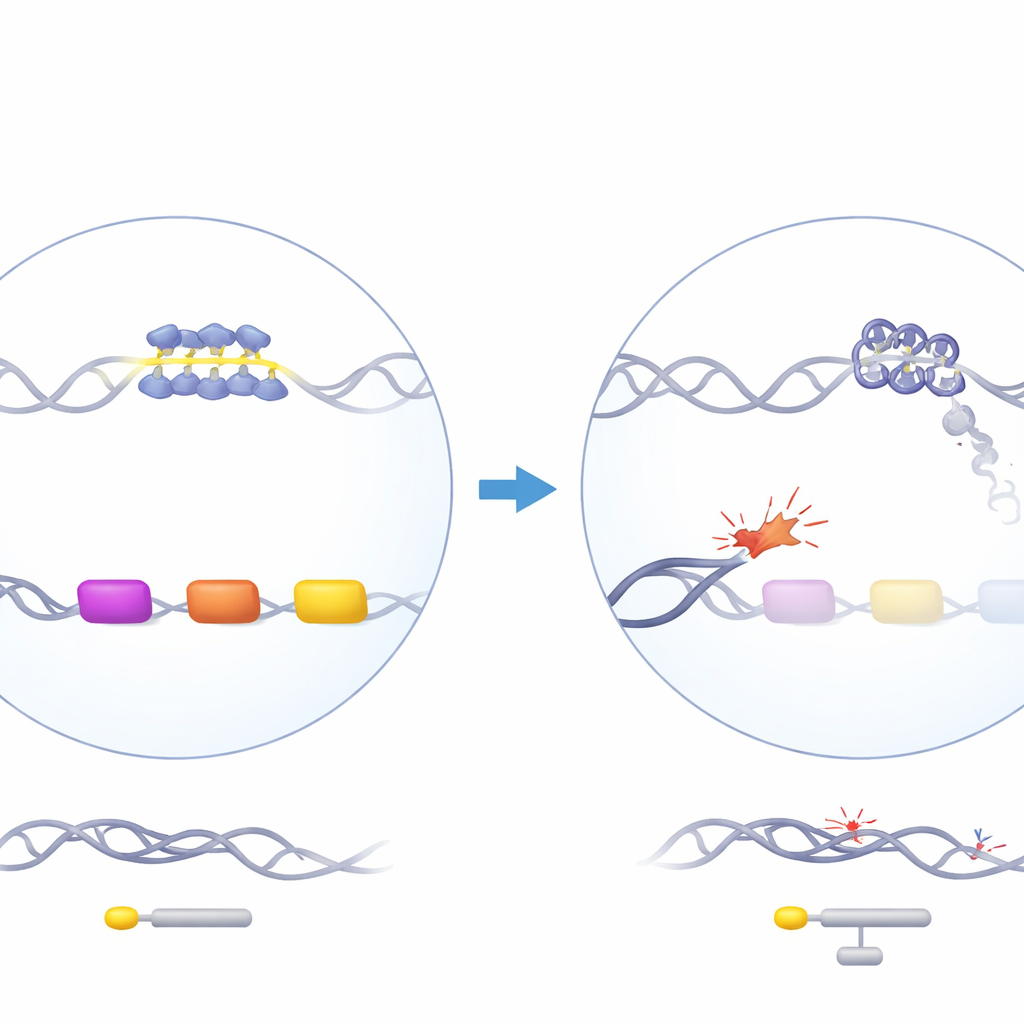
Uma proteína guardiã com um efeito enigmático
ATRX é uma proteína remodeladora de cromatina que ajuda a organizar o DNA e participa da replicação, transcrição e reparo do DNA. Quando o ATRX é mutado em humanos, os pacientes desenvolvem a síndrome ATR-X, que inclui uma alfa-talassemia branda: seus genes da alfa-globina, necessários para montar a hemoglobina, ficam subativos. Curiosamente, a perda de ATRX afeta a alfa-globina, mas não a beta-globina, embora ambas sejam necessárias em quantidades equivalentes. Os genes da alfa-globina estão em uma região rica em genes e GC do cromossomo 16 que contém vários elementos de DNA repetitivo, incluindo um repetitivo em tandem de número variável (VNTR) particularmente rico em G localizado logo a montante dos genes semelhantes à globina alfa. Trabalhos genéticos anteriores mostraram que o comprimento desse repetido correlaciona com a intensidade da redução da alfa-globina em pacientes, sugerindo que esse trecho estranho de DNA pode ser central para o problema.
Aproximando-se das células afetadas
Para investigar, os autores removeram o ATRX em células-tronco e progenitoras sanguíneas humanas usando edição gênica CRISPR e então maturaram essas células em precursores de hemácias em cultura. Olhar a população celular como um todo mostrou apenas uma queda discreta em um gene semelhante à alfa, HBM, e nenhuma alteração importante em outros genes da globina, refletindo as mudanças sanguíneas modestamente observadas em pacientes. No entanto, quando analisaram colônias individuais e células únicas, surgiu um quadro diferente. Apenas um subconjunto das células deficientes em ATRX mostrou forte redução de HBM e, em menor grau, dos genes principais da alfa-globina. Essas mesmas células exibiram assinaturas de ativação da resposta a danos no DNA, incluindo aumento de marcadores de DNA quebrado e maior modificação de uma histona (H2A) associada ao reparo de danos e silenciamento de genes próximos. Isso sugeriu que a redução da alfa-globina ocorre principalmente em células onde a perda de ATRX permitiu o acúmulo de danos locais ao DNA.
Um repetitivo rico em G problemático como ponto fraco
A equipe então concentrou-se no VNTR rico em G embutido em um pseudogene próximo chamado HBZP1. Usando uma linhagem eritroide humana imortalizada, rastrearam a ligação do ATRX ao longo da região da alfa-globina e descobriram que o ATRX é recrutado especificamente a esse VNTR quando o DNA circundante está sendo transcrito. Eles projetaram um sistema em que o ATRX podia ser rapidamente degradado e observaram que a perda de ATRX reduziu a expressão de HBM, novamente mimetizando o fenótipo da doença. De forma marcante, quando deletaram o próprio VNTR do genoma, a remoção do ATRX deixou de reduzir os níveis de HBM. Drogas que estabilizam estruturas incomuns de quatro fitas de DNA conhecidas como G-quadruplexos produziram uma queda semelhante na expressão de HBM, mas apenas quando o VNTR estava presente. Análises genômicas revelaram que muitos outros genes desregulados pela perda de ATRX também contêm elementos repetitivos ricos em GC, apontando para uma vulnerabilidade geral nesses locais.
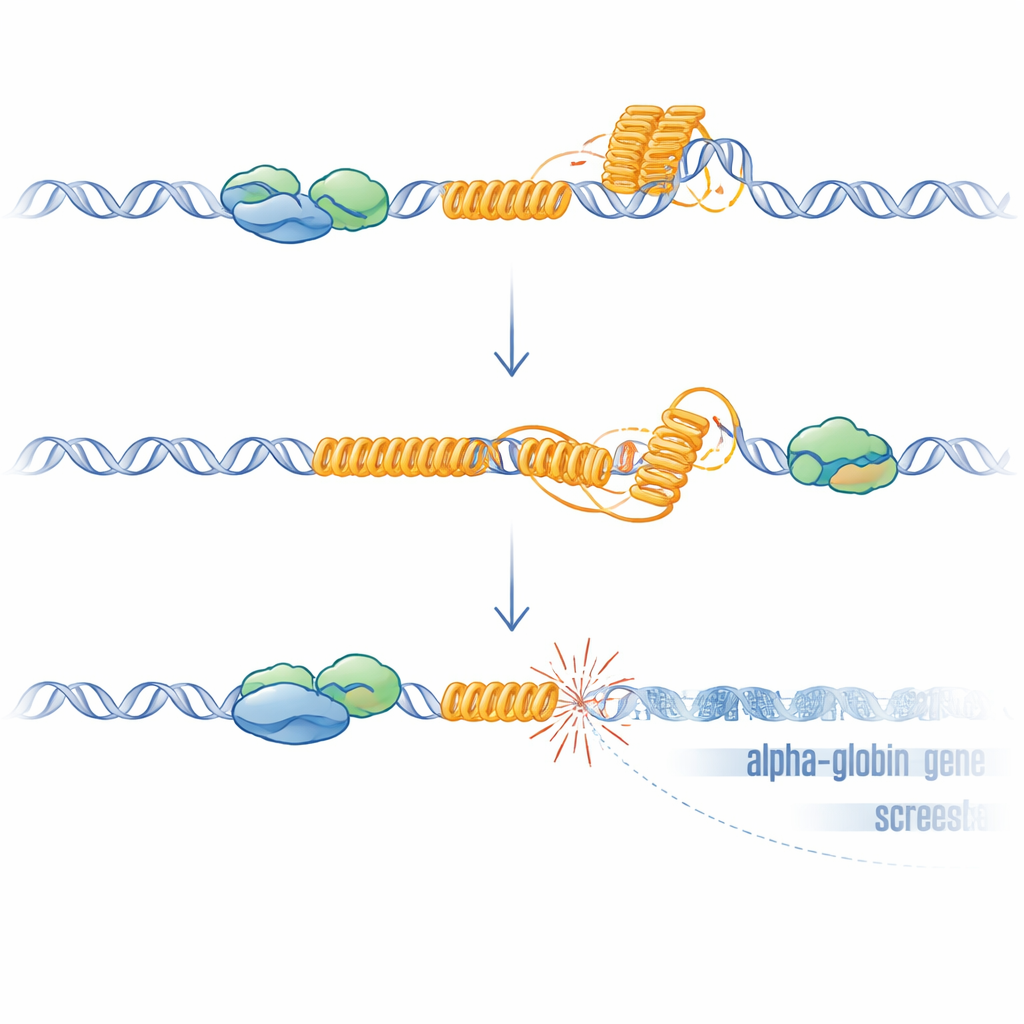
De formas estranhas de DNA a genes quebrados
Repetidos ricos em G como esse VNTR podem se dobrar em G-quadruplexos e favorecer a formação de R-loops, estruturas híbridas onde o RNA recém-sintetizado permanece preso à fita molde de DNA. Ambas as estruturas podem desacelerar ou bloquear a maquinaria que copia e lê o DNA, causando estresse e quebras. Os pesquisadores mostraram que, sem ATRX, os R-loops aumentaram por todo o genoma e foram particularmente elevados no VNTR. Quando superexpressaram RNase H, uma enzima que remove R-loops, a expressão de HBM se recuperou parcialmente, sustentando um papel causal dessas estruturas. Para testar se o dano ao DNA por si só era suficiente para silenciar os genes próximos, eles usaram CRISPR para criar quebras direcionadas logo a montante de HBM em células nas quais o VNTR havia sido deletado. Essas quebras artificiais, mesmo na ausência do repetido, novamente reduziram HBM e, mais fracamente, os genes da alfa-globina, com o gene mais próximo sendo o mais afetado. Esse efeito dependente da distância corresponde ao observado em pacientes e é consistente com o espalhamento conhecido de repressão transcricional a partir de sítios de quebras de dupla fita.
O que isso significa para a doença e além
Em conjunto, o trabalho delineia um modelo claro: em células saudáveis, o ATRX se liga a um repetido rico em G próximo aos genes da alfa-globina enquanto ele é transcrito, ajudando a prevenir ou dissolver G-quadruplexos e R-loops e assim protegendo a região de danos ao DNA. Quando o ATRX está ausente, essas estruturas incomuns de DNA e RNA se acumulam no repetido, levando a quebras locais no DNA, ativação da resposta a danos e a um ambiente cromatínico repressivo que reduz a expressão de genes próximos de forma dependente da distância, com HBM sendo o mais atingido. Esse mecanismo explica por que a síndrome ATR-X causa apenas uma alfa-talassemia leve e pontual, por que a gravidade varia com o comprimento do repetido e por que modelos murinos sem esse repetido específico de humanos não apresentam o mesmo defeito sanguíneo. Mais amplamente, sugere que sequências repetitivas ricas em G espalhadas pelo nosso genoma podem agir como falhas ocultas: se fatores protetores como o ATRX falham, elas podem se tornar pontos quentes de instabilidade que silenciosamente reconfiguram a atividade gênica no desenvolvimento, envelhecimento e câncer.
Citação: Shen, Y., Gupta, K., Tan-Wong, S.M. et al. ATRX loss couples genome instability at a G-rich repeat to dysregulation of human alpha-globin expression. Nat Commun 17, 2749 (2026). https://doi.org/10.1038/s41467-026-69169-7
Palavras-chave: ATRX, alfa-globina, danos ao DNA, G-quadruplexo, R-loops