Clear Sky Science · de
Verlust von ATRX koppelt Genominstabilität an einer G-reichen Wiederholung an die Fehlregulation der menschlichen Alpha-Globin-Expression
Warum das für Blut und Krebs wichtig ist
Unsere roten Blutkörperchen sind auf eine fein abgestimmte Kontrolle der Gene angewiesen, die Hämoglobin herstellen, das Protein, das Sauerstoff transportiert. Ein Protein namens ATRX bindet an die DNA und trägt zur Stabilität bei; Mutationen in ATRX verursachen eine erbliche Form von Anämie mit geistiger Behinderung und treten häufig in verschiedenen Krebsarten auf. Diese Studie nutzt den Alpha-Globin-Gencluster als Fallbeispiel und zeigt auf molekularer Ebene, wie der Verlust von ATRX DNA an einer repetitiven Sequenz schädigen und nahegelegene Gene stumm schalten kann. Das Verständnis dieser Ereigniskette hilft, eine seltene menschliche Erkrankung zu erklären und beleuchtet, wie Genominstabilität die Genaktivität allgemein verändern kann.
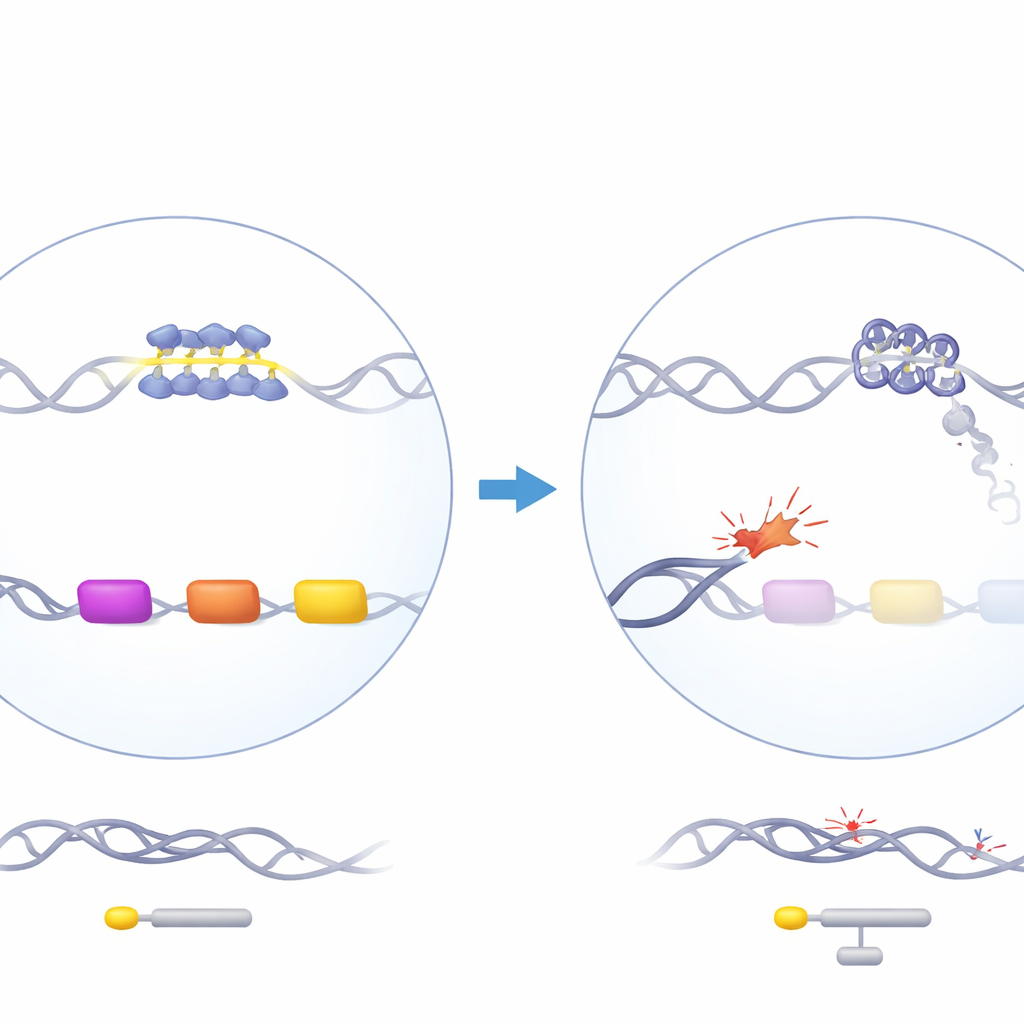
Ein Wächterprotein mit rätselhaftem Effekt
ATRX ist ein Chromatin-Remodelling-Protein, das die Organisation der DNA unterstützt und an Replikation, Transkription und DNA-Reparatur beteiligt ist. Wenn ATRX beim Menschen mutiert ist, entwickeln Patienten das ATR-X-Syndrom, das eine milde Alpha-Thalassämie einschließt: ihre Alpha-Globin-Gene, die zur Bildung von Hämoglobin nötig sind, sind unteraktiv. Auffällig ist, dass der Verlust von ATRX die Alpha-Globin-, nicht aber die Beta-Globin-Gene betrifft, obwohl beide in gleichen Mengen benötigt werden. Die Alpha-Globin-Gene liegen in einer gen- und GC-reichen Region auf Chromosom 16, die mehrere repetitive DNA-Elemente enthält, darunter eine besonders G-reiche variable Tandemwiederholung (VNTR) direkt stromaufwärts der alpha-ähnlichen Globin-Gene. Frühere genetische Untersuchungen zeigten, dass die Länge dieser Wiederholung mit der Stärke der Alpha-Globin-Reduktion bei Patienten korreliert, was darauf hindeutet, dass diese eigenartige DNA-Strecke zentral für das Problem sein könnte.
Ein Blick in die betroffenen Zellen
Um dies zu untersuchen, entfernten die Autoren ATRX in menschlichen Blutstamm- und Vorläuferzellen mittels CRISPR-Geneditierung und differenzierten diese Zellen anschließend in Kultur zu Vorstufen roter Blutkörperchen. Auf Populationsebene zeigte sich nur ein leichter Abfall eines alpha-ähnlichen Gens, HBM, und keine wesentlichen Veränderungen anderer Globin-Gene, was die moderaten Blutveränderungen bei Patienten widerspiegelt. Analysen einzelner Kolonien und Einzelzellen ergaben jedoch ein anderes Bild. Nur eine Untergruppe ATRX-defizienter Zellen wies eine starke Reduktion von HBM und in geringerem Maße der Haupt-Alpha-Globin-Gene auf. Dieselben Zellen zeigten Anzeichen einer aktivierten DNA-Schadensantwort, einschließlich erhöhter Marker für DNA-Brüche und verstärkter Modifikation eines Histonproteins (H2A), das mit Reparaturprozessen und der Stilllegung benachbarter Gene in Verbindung steht. Das deutet darauf hin, dass die Herunterregulierung von Alpha-Globin vor allem in Zellen stattfindet, in denen ATRX-Verlust lokale DNA-Schäden hat akkumulieren lassen.
Eine problematische G-reiche Wiederholung als Schwachstelle
Das Team konzentrierte sich dann auf die G-reiche VNTR, die in einem nahegelegenen Pseudogen namens HBZP1 eingebettet ist. In einer immortalisierten humanen erythroiden Zelllinie verfolgten sie die ATRX-Bindung über den Alpha-Globin-Bereich und fanden, dass ATRX speziell zu dieser VNTR rekrutiert wird, wenn die umgebende DNA transkribiert wird. Sie entwickelten ein System, in dem ATRX schnell abgebaut werden konnte, und beobachteten, dass der Verlust von ATRX die HBM-Expression verringerte — wiederum ein Phänotyp, der der Krankheit ähnelt. Bemerkenswerterweise führte die Entfernung der VNTR aus dem Genom dazu, dass das Entfernen von ATRX HBM-Spiegel nicht mehr senkte. Wirkstoffe, die ungewöhnliche viersträngige DNA-Strukturen, sogenannte G-Quadruplexe, stabilisieren, bewirkten einen ähnlichen Abfall der HBM-Expression, jedoch nur wenn die VNTR vorhanden war. Genomweite Analysen zeigten, dass viele andere Gene, die durch ATRX-Verlust fehlreguliert werden, ebenfalls GC-reiche repetitive Elemente enthalten, was auf eine allgemeine Verwundbarkeit an solchen Stellen hinweist.
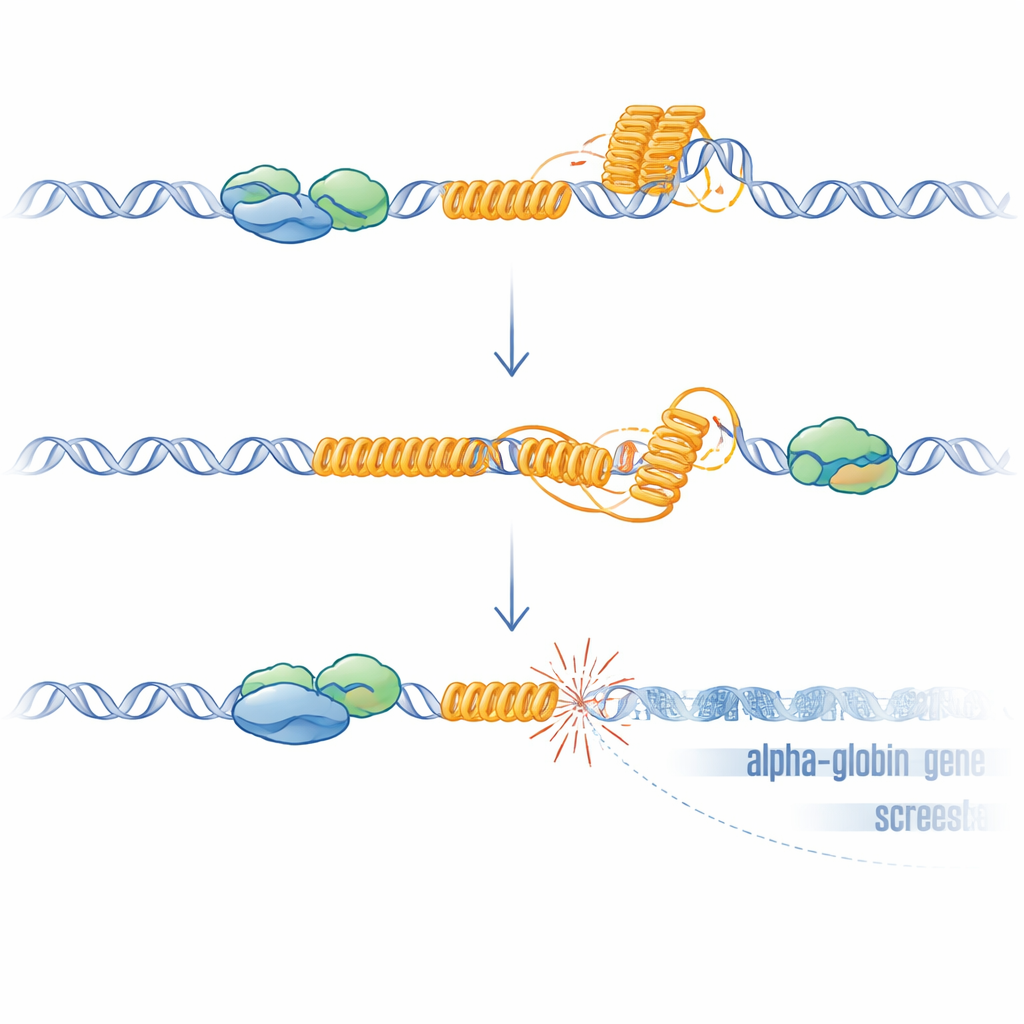
Von seltsamen DNA-Formen zu beschädigten Genen
G-reiche Wiederholungen wie diese VNTR können sich zu G-Quadruplexen falten und die Bildung von R-Loops fördern — Hybridstrukturen, bei denen neu synthetisierte RNA an der DNA-Vorlage haften bleibt. Beide Strukturen können die Enzyme, die DNA kopieren und ablesen, verlangsamen oder blockieren und so Stress und Brüche verursachen. Die Forscher zeigten, dass ohne ATRX R-Loops im Genom zunahmen und besonders an der VNTR erhöht waren. Durch Überexpression von RNase H, einem Enzym, das R-Loops entfernt, erholte sich die HBM-Expression teilweise, was eine ursächliche Rolle dieser Strukturen stützt. Um zu testen, ob DNA-Schäden allein ausreichen, die benachbarten Gene stumm zu schalten, erzeugten sie mit CRISPR gezielte Brüche direkt stromaufwärts von HBM in Zellen, bei denen die VNTR entfernt worden war. Diese künstlichen Brüche reduzierten wiederum HBM und, schwächer ausgeprägt, die Alpha-Globin-Gene, wobei das nächstgelegene Gen am stärksten betroffen war. Dieser distanzabhängige Effekt entspricht den Beobachtungen bei Patienten und passt zu bekannten Ausbreitungsmechanismen transkriptioneller Repression von Stellen mit Doppelstrangbrüchen weg.
Was das für Krankheit und mehr bedeutet
Insgesamt skizziert die Arbeit ein klares Modell: In gesunden Zellen bindet ATRX an eine G-reiche Wiederholung nahe der Alpha-Globin-Gene während deren Transkription und hilft, G-Quadruplexe und R-Loops zu verhindern oder aufzulösen, wodurch die Region vor DNA-Schäden geschützt wird. Fehlt ATRX, häufen sich diese ungewöhnlichen DNA- und RNA-Strukturen an der Wiederholung an, was zu lokalen DNA-Brüchen, Aktivierung einer Schadensantwort und einer repressiven Chromatinumgebung führt, die die Expression benachbarter Gene in einer distanzabhängigen Weise dämpft — HBM am stärksten. Dieser Mechanismus erklärt, warum das ATR-X-Syndrom nur eine milde, punktuelle Alpha-Thalassämie verursacht, warum die Schwere mit der Wiederholungslänge variiert und warum Mausmodelle ohne diese menschenspezifische Wiederholung denselben Blutdefekt nicht zeigen. Allgemeiner legt es nahe, dass repetitive, G-reiche Sequenzen im Genom als verborgene Störungszonen fungieren können: Fällt ein Schutzfaktor wie ATRX aus, können sie zu Hotspots der Instabilität werden, die still und leise die Genaktivität in Entwicklung, Alterung und Krebs umschreiben.
Zitation: Shen, Y., Gupta, K., Tan-Wong, S.M. et al. ATRX loss couples genome instability at a G-rich repeat to dysregulation of human alpha-globin expression. Nat Commun 17, 2749 (2026). https://doi.org/10.1038/s41467-026-69169-7
Schlüsselwörter: ATRX, alpha-Globin, DNA-Schaden, G-Quadruplex, R-Loops