Clear Sky Science · nl
Verlies van ATRX koppelt genoominstabiliteit bij een G-rijke herhaling aan dysregulatie van menselijke alfa-globineexpressie
Waarom dit belangrijk is voor bloed en kanker
Onze rode bloedcellen zijn afhankelijk van nauwkeurig afgestuurde controle van de genen die hemoglobine maken, het eiwit dat zuurstof transporteert. Een eiwit genaamd ATRX bindt aan DNA en helpt het stabiel te houden; mutaties in ATRX veroorzaken een erfelijke vorm van anemie met verstandelijke beperking en komen vaak voor in verschillende soorten kanker. Deze studie gebruikt de alfa-globinegencluster als casus om, op moleculair niveau, te laten zien hoe verlies van ATRX DNA kan beschadigen op een repetitieve sequentie en stilletjes nabijgelegen genen kan uitschakelen. Inzicht in deze opeenvolging van gebeurtenissen helpt een zeldzame menselijke aandoening te verklaren en werpt licht op hoe genoominstabiliteit genactiviteit algemener kan veranderen.
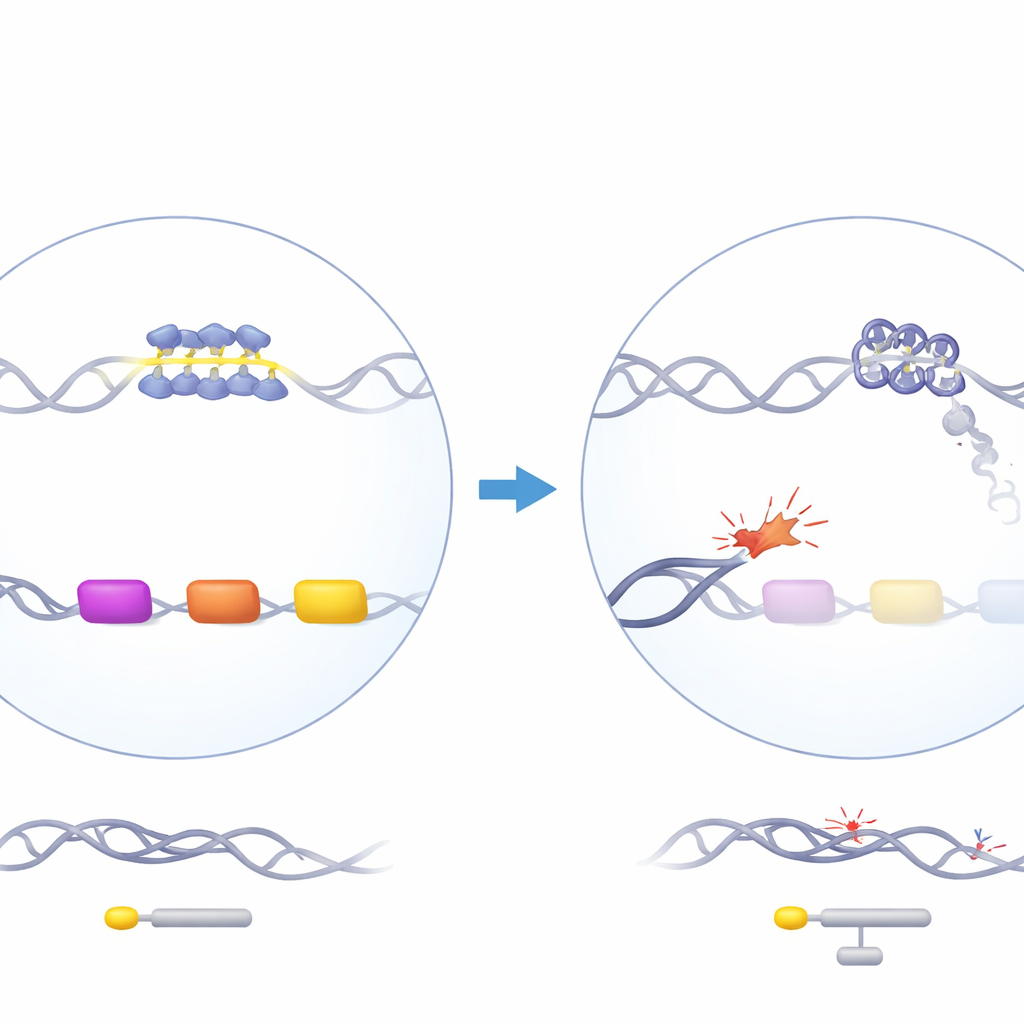
Een beschermend eiwit met een raadselachtig effect
ATRX is een chromatine-remodellerend eiwit dat helpt DNA te organiseren en betrokken is bij replicatie, transcriptie en DNA-herstel. Wanneer ATRX bij mensen gemuteerd is, ontwikkelen patiënten het ATR-X-syndroom, dat een milde alfa-thalassemie omvat: hun alfa-globinegenen, nodig voor de opbouw van hemoglobine, zijn onderactief. Intrigerend genoeg treft het verlies van ATRX alfa-globine maar niet bèta-globine, hoewel beide in gelijke hoeveelheden nodig zijn. De alfa-globinegenen liggen in een genrijke, GC-rijke regio van chromosoom 16 die meerdere repetitieve DNA-elementen bevat, waaronder een bijzonder G-rijke variable number tandem repeat (VNTR) vlakstroomopwaarts van de alfa-achtige globinegenen. Eerder genetisch werk toonde dat de lengte van deze herhaling correleert met hoe sterk alfa-globine bij patiënten verminderd is, wat suggereert dat deze vreemde DNA-strook centraal kan staan in het probleem.
Inzoomen op de aangedane cellen
Om dit te onderzoeken verwijderden de auteurs ATRX in menselijke bloedstam- en voorlopercellen met CRISPR-genbewerking en lieten deze cellen vervolgens in cultuur rijpen tot voorlopers van rode bloedcellen. Een analyse van de hele celpopulatie toonde slechts een milde daling van één alfa-achtig gen, HBM, en geen grote veranderingen in andere globinegenen, wat het bescheiden bloedbeeld bij patiënten weerspiegelt. Toen ze echter individuele kolonies en enkele cellen analyseerden, ontstond een ander beeld. Slechts een subset van ATRX-deficiënte cellen toonde sterke reductie van HBM en, in mindere mate, van de belangrijkste alfa-globinegenen. Dezezelfde cellen vertoonden tekenen van een geactiveerde DNA-schaderespons, waaronder verhoogde markers van gebroken DNA en toegenomen modificatie van het histoneiwit H2A, dat geassocieerd is met herstel van schade en het onderdrukken van nabijgelegen genen. Dit suggereert dat downregulatie van alfa-globine vooral optreedt in cellen waar het verlies van ATRX lokale DNA-schade heeft laten oplopen.
Een lastig G-rijke herhaling als zwakke plek
Het team richtte zich vervolgens op de G-rijke VNTR ingebed in een nabijgelegen pseudogen genoemd HBZP1. Met een geïmmortaliseerde menselijke erytroïde cellijn volgden ze ATRX-bindingsplaatsen in de alfa-globine-regio en vonden dat ATRX specifiek naar deze VNTR wordt gerekruteerd wanneer het omringende DNA wordt getranscribeerd. Ze bouwden een systeem waarin ATRX snel afgebroken kon worden en observeerden dat verlies van ATRX HBM-expressie verminderde, opnieuw het ziektefenotype nabootsend. Opmerkelijk was dat het verwijderen van de VNTR zelf uit het genoom ervoor zorgde dat het weghalen van ATRX HBM-niveaus niet langer verlaagde. Geneesmiddelen die ongewone vierstrengige DNA-structuren, G-quadruplexen, stabiliseren gaven een vergelijkbare daling van HBM-expressie, maar alleen wanneer de VNTR aanwezig was. Genoomwijde analyses lieten zien dat veel andere genen die door ATRX-verlies ontregeld worden ook GC-rijke repetitieve elementen bevatten, wat wijst op een algemene kwetsbaarheid op dergelijke locaties.
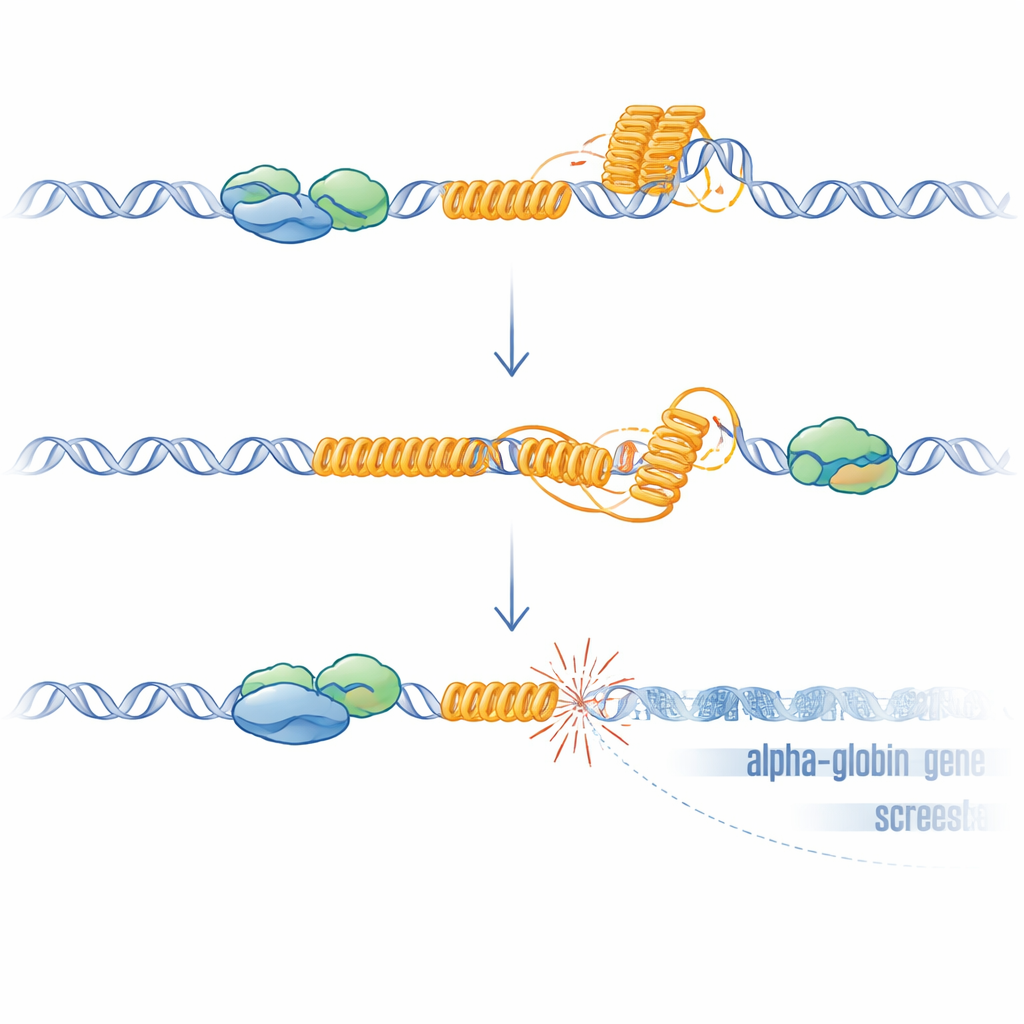
Van vreemde DNA-vormen naar gebroken genen
G-rijke herhalingen zoals deze VNTR kunnen vouwen tot G-quadruplexen en de vorming van R-lussen bevorderen, hybride structuren waarin nieuw gevormd RNA vast blijft zitten aan de DNA-sjabloon. Beide structuren kunnen het machinerie die DNA kopieert en leest vertragen of doen vastlopen, wat stress en breuken veroorzaakt. De onderzoekers toonden aan dat zonder ATRX R-lussen in het hele genoom toenamen en bijzonder hoog waren bij de VNTR. Wanneer ze RNase H overexpresseerden, een enzym dat R-lussen verwijdert, herstelde HBM-expressie gedeeltelijk, wat een oorzakelijke rol voor deze structuren ondersteunt. Om te testen of DNA-schade alleen voldoende was om de nabijgelegen genen te stilleggen, gebruikten ze CRISPR om gerichte breuken net stroomopwaarts van HBM te creëren in cellen waarin de VNTR was verwijderd. Deze kunstmatige breuken, zelfs in afwezigheid van de herhaling, verminderden opnieuw HBM en, zwakker, de alfa-globinegenen, waarbij het dichtstbijzijnde gen het meest werd getroffen. Dit afstandsafhankelijke effect komt overeen met wat bij patiënten wordt gezien en past bij het bekende verspreiden van transcriptierepressie weg van locaties van dubbelstrengsbreuken.
Wat dit betekent voor ziekte en daarbuiten
Gezamenlijk schetst het werk een helder model: in gezonde cellen bindt ATRX aan een G-rijke herhaling nabij de alfa-globinegenen terwijl deze wordt getranscribeerd, en helpt het G-quadruplexen en R-lussen te voorkomen of op te lossen, waardoor de regio tegen DNA-schade wordt beschermd. Wanneer ATRX ontbreekt, hopen deze ongewone DNA- en RNA-structuren zich op bij de herhaling, wat leidt tot lokale DNA-breuken, activatie van een schadeantwoord en een repressieve chromatineomgeving die de expressie van nabijgelegen genen op een afstandsafhankelijke manier dempt, waarbij HBM het hardst wordt getroffen. Dit mechanisme verklaart waarom het ATR-X-syndroom slechts milde, ongelijkmatige alfa-thalassemie veroorzaakt, waarom de ernst varieert met de lengte van de herhaling, en waarom muismodellen zonder deze mens-specifieke herhaling niet hetzelfde bloeddefect tonen. In bredere zin suggereert het dat repetitieve, G-rijke sequenties verspreid door ons genoom als verborgen breuklijnen kunnen fungeren: als beschermende factoren zoals ATRX falen, kunnen ze hotspots van instabiliteit worden die genactiviteit stilletjes hereenkabelen tijdens ontwikkeling, veroudering en kanker.
Bronvermelding: Shen, Y., Gupta, K., Tan-Wong, S.M. et al. ATRX loss couples genome instability at a G-rich repeat to dysregulation of human alpha-globin expression. Nat Commun 17, 2749 (2026). https://doi.org/10.1038/s41467-026-69169-7
Trefwoorden: ATRX, alfa-globine, DNA-schade, G-quadruplex, R-lussen