Clear Sky Science · pl
Utrata ATRX łączy niestabilność genomu w G‑bogatym repetytywnym odcinku z zaburzeniem ekspresji ludzkiego alfa‑globiny
Dlaczego to ma znaczenie dla krwi i nowotworów
Nasze czerwone krwinki zależą od precyzyjnej kontroli genów kodujących hemoglobinę, białko transportujące tlen. Białko zwane ATRX wiąże się z DNA i pomaga utrzymać jego stabilność; mutacje w ATRX powodują uwarunkowaną dziedzicznie anemię z upośledzeniem intelektualnym i występują często w kilku nowotworach. W tym badaniu klaster genów alfa‑globiny wykorzystano jako model, aby pokazać szczegółowo molekularnie, w jaki sposób utrata ATRX może uszkadzać DNA w repetytywnym odcinku i „cicho” wyłączać pobliskie geny. Zrozumienie tego łańcucha zdarzeń pomaga wyjaśnić rzadkie ludzkie schorzenie i rzuca światło na to, jak niestabilność genomu może szerzej zmieniać aktywność genów.
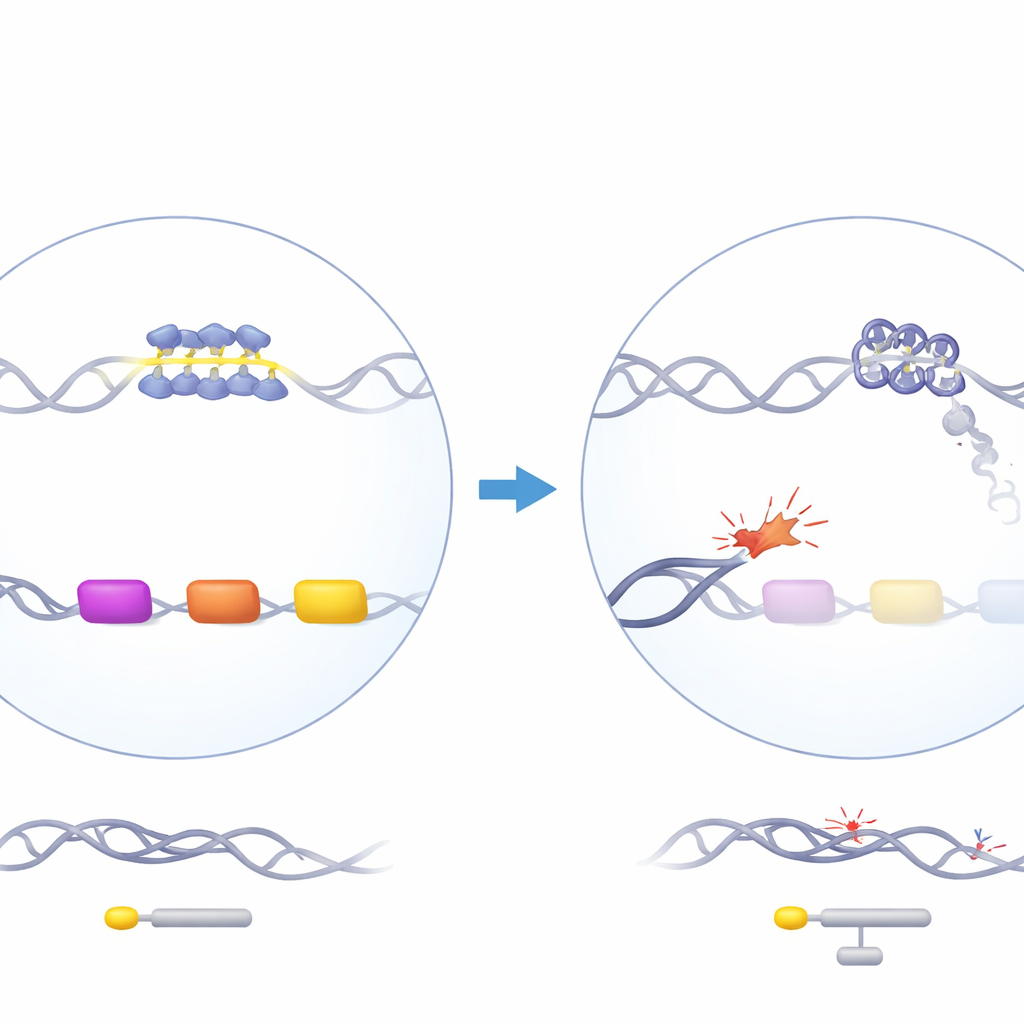
Opiekun chromatinowy o zagadkowym wpływie
ATRX to białko remodelujące chromatynę, które pomaga organizować DNA i uczestniczy w replikacji, transkrypcji i naprawie DNA. Gdy ATRX jest zmutowany u ludzi, chorzy rozwijają zespół ATR‑X, obejmujący łagodną formę alfa‑talasemii: ich geny alfa‑globiny, potrzebne do budowy hemoglobiny, są niedoczynne. Zaskakująco, utrata ATRX wpływa na alfa‑globinę, a nie na beta‑globinę, mimo że obie są wymagane w równych ilościach. Geny alfa‑globiny leżą w bogatym w geny i GC rejonie chromosomu 16, który zawiera kilka repetytywnych elementów DNA, w tym szczególnie G‑bogaty powtarzalny tandemowy element o zmiennej liczbie kopii (VNTR) położony tuż w górę od genów podobnych do alfa‑globiny. Wcześniejsze badania genetyczne wykazały, że długość tego powtórzenia koreluje z nasileniem obniżenia alfa‑globiny u pacjentów, co sugeruje, że ten nietypowy fragment DNA może odgrywać kluczową rolę.
Przyglądając się dotkniętym komórkom
Aby to zbadać, autorzy usunęli ATRX w ludzkich komórkach macierzystych i progenitorowych krwi za pomocą edycji genowej CRISPR, a następnie doprowadzili te komórki do dojrzałości w kierunku prekursorów erytrocytów w hodowli. Analiza populacji komórek jako całości wykazała tylko łagodny spadek jednego genu podobnego do alfa, HBM, i brak dużych zmian w innych genach globiny, co odzwierciedla umiarkowane zmiany krwi obserwowane u pacjentów. Jednak przy analizie pojedynczych kolonii i pojedynczych komórek wyłonił się inny obraz. Tylko podzbiór komórek pozbawionych ATRX wykazywał silne obniżenie HBM, a w mniejszym stopniu głównych genów alfa‑globiny. Te same komórki prezentowały sygnatury aktywowanej odpowiedzi na uszkodzenia DNA, w tym zwiększone markery pęknięć DNA i nasilone modyfikacje histonu (H2A) związane z naprawą uszkodzeń i wyciszaniem pobliskich genów. To sugeruje, że obniżenie ekspresji alfa‑globiny zachodzi głównie w komórkach, w których utrata ATRX pozwoliła na gromadzenie się lokalnych uszkodzeń DNA.
G‑bogaty repeat jako słabe ogniwo
Zespół skoncentrował się następnie na G‑bogatym VNTR osadzonym w pobliskim pseudogenie HBZP1. Używając immortalizowanej ludzkiej linii erytroidalnej, śledzili wiązanie ATRX w całym regionie alfa‑globiny i odkryli, że ATRX jest specyficznie rekrutowany do tego VNTR, gdy otaczające DNA jest transkrybowane. Zaprojektowali system, w którym ATRX mógł być szybko degradowany i zaobserwowali, że utrata ATRX zmniejsza ekspresję HBM, ponownie odwzorowując fenotyp chorobowy. Co istotne, po usunięciu samego VNTR z genomu, usunięcie ATRX przestało obniżać poziomy HBM. Leki stabilizujące nietypowe czterorzędowe struktury DNA zwane G‑quadrupleksami wywołały podobny spadek ekspresji HBM, lecz tylko gdy VNTR był obecny. Analizy ogólnogenomowe wykazały, że wiele innych genów, których regulacja jest zaburzona przez utratę ATRX, również zawiera GC‑bogate elementy repetytywne, wskazując na ogólną wrażliwość takich miejsc.
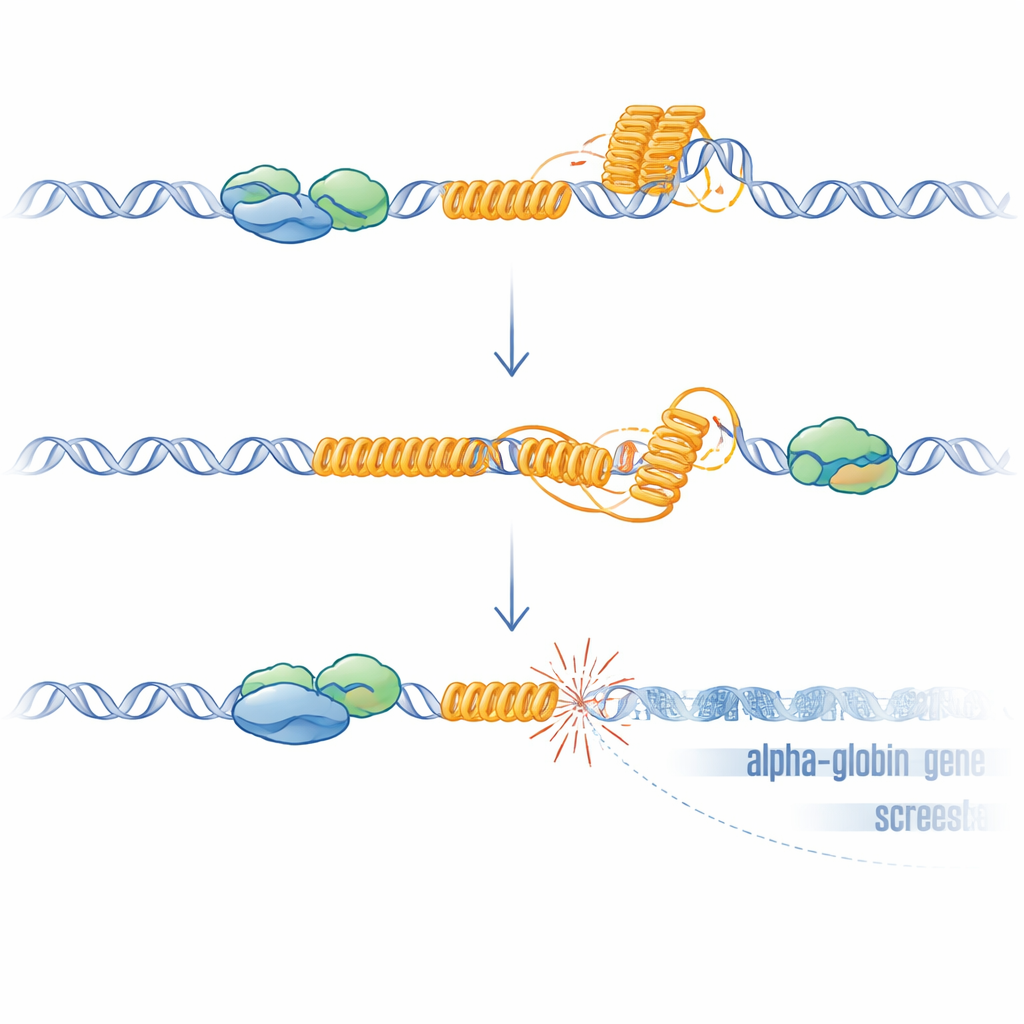
Od dziwnych kształtów DNA do uszkodzonych genów
G‑bogate repetytywy takie jak ten VNTR mogą składać się w G‑quadrupleksy i sprzyjać formowaniu się R‑pętli — hybrydowych struktur, w których nowo powstały RNA pozostaje przyklejony do matrycy DNA. Obie struktury mogą spowalniać lub zatrzymywać maszynerię kopiującą i odczytującą DNA, powodując stres i pęknięcia. Badacze wykazali, że bez ATRX R‑pętli zwiększały się w całym genomie i były szczególnie podwyższone na VNTR. Gdy nadeksprymowali RNazę H, enzym usuwający R‑pętle, ekspresja HBM częściowo się odtworzyła, co wspiera przyczynową rolę tych struktur. Aby przetestować, czy samo uszkodzenie DNA wystarczy, by wyciszyć pobliskie geny, użyli CRISPR do stworzenia celowanych pęknięć tuż w górę od HBM w komórkach, w których VNTR został usunięty. Te sztuczne pęknięcia, nawet bez powtórzenia, ponownie obniżyły HBM i, słabiej, geny alfa‑globiny, przy czym najsilniej dotknięty był gen najbliższy miejscu pęknięcia. Ten zależny od odległości efekt odpowiada obserwacjom u pacjentów i jest zgodny ze znanym rozprzestrzenianiem się represji transkrypcyjnej od miejsc podwójnych złamań nici DNA.
Co to znaczy dla chorób i nie tylko
Podsumowując, praca przedstawia jasny model: w zdrowych komórkach ATRX wiąże się z G‑bogatym powtórzeniem w pobliżu genów alfa‑globiny podczas ich transkrypcji, pomagając zapobiegać lub rozpuszczać G‑quadrupleksy i R‑pętle oraz chroniąc region przed uszkodzeniem DNA. Gdy ATRX jest nieobecny, te nietypowe struktury DNA i RNA gromadzą się na repetytywie, prowadząc do lokalnych pęknięć DNA, aktywacji odpowiedzi na uszkodzenia i tworzenia represyjnej chromatyny, która tłumi ekspresję pobliskich genów w sposób zależny od odległości, z najsilniejszym efektem na HBM. Ten mechanizm wyjaśnia, dlaczego zespół ATR‑X powoduje tylko łagodną, mozaikowatą alfa‑talassemię, dlaczego nasilenie zależy od długości powtórzenia i dlaczego modele mysie, którym brakuje tego ludzkiego specyficznego powtórzenia, nie wykazują tego samego defektu krwi. Szerzej rzecz biorąc, sugeruje to, że powtarzalne, G‑bogate sekwencje rozsiane po genomie mogą działać jak ukryte uskoki: jeśli czynniki ochronne, takie jak ATRX, zawodzą, mogą stać się ogniskami niestabilności, które dyskretnie przestawiają aktywność genów w rozwoju, starzeniu i nowotworzeniu.
Cytowanie: Shen, Y., Gupta, K., Tan-Wong, S.M. et al. ATRX loss couples genome instability at a G-rich repeat to dysregulation of human alpha-globin expression. Nat Commun 17, 2749 (2026). https://doi.org/10.1038/s41467-026-69169-7
Słowa kluczowe: ATRX, alfa‑globina, uszkodzenia DNA, G‑czterorzędowość (G‑quadruplex), R‑pętle