Clear Sky Science · it
Perdita di ATRX collega l’instabilità del genoma a un ripetuto ricco di G con la disregolazione dell’espressione dell’alfa-globina umana
Perché è importante per il sangue e il cancro
Le nostre cellule del sangue rosso dipendono da un controllo finemente regolato dei geni che producono l’emoglobina, la proteina che trasporta l’ossigeno. Una proteina chiamata ATRX si lega al DNA e contribuisce a mantenerne la stabilità; mutazioni in ATRX causano una forma ereditaria di anemia con disabilità intellettiva e sono frequenti in diversi tumori. Questo studio utilizza il cluster dei geni dell’alfa-globina come caso di studio per mostrare, a livello molecolare, come la perdita di ATRX possa danneggiare il DNA in un tratto ripetuto e spegnere silenziosamente geni vicini. Comprendere questa catena di eventi aiuta a spiegare un raro disturbo umano e fa luce su come l’instabilità del genoma possa alterare l’attività genica più in generale.
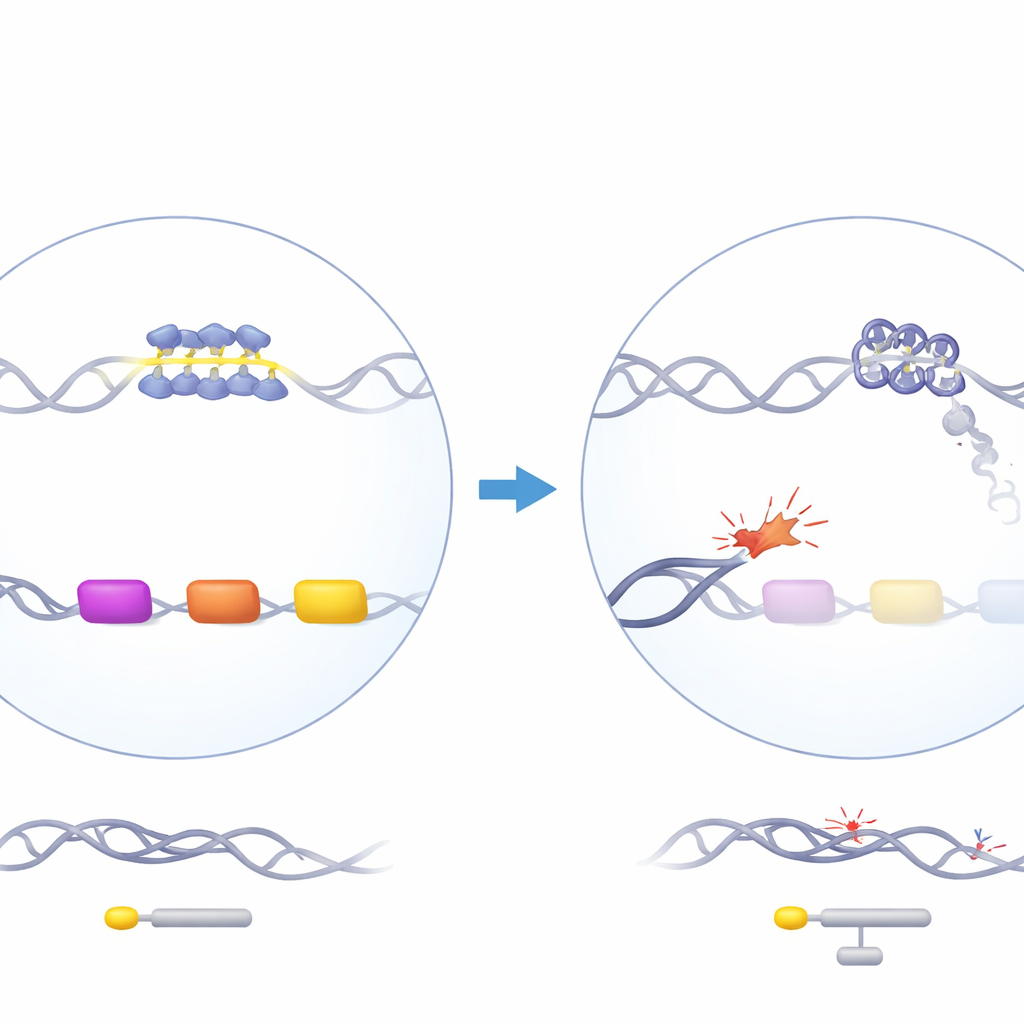
Una proteina guardiana con un effetto sconcertante
ATRX è una proteina di rimodellamento della cromatina che contribuisce a organizzare il DNA ed è coinvolta nella replicazione, trascrizione e riparazione del DNA. Quando ATRX è mutato nell’uomo, i pazienti sviluppano la sindrome ATR-X, che include una lieve alfa-talassemia: i loro geni dell’alfa-globina, necessari per costruire l’emoglobina, risultano sottoattivi. È intrigante che la perdita di ATRX colpisca l’alfa-globina ma non la beta-globina, nonostante entrambe siano richieste in quantità uguali. I geni dell’alfa-globina si trovano in una regione ricca di geni e di GC del cromosoma 16 che contiene diversi elementi ripetuti di DNA, incluso un VNTR (ripetizione in tandem a numero variabile) particolarmente ricco di G situato appena a monte dei geni globinici simili all’alfa. Lavori genetici precedenti hanno mostrato che la lunghezza di questa ripetizione si correla con l’entità della riduzione dell’alfa-globina nei pazienti, suggerendo che questo tratto di DNA insolito potrebbe essere centrale nel problema.
Osservare le cellule colpite
Per indagare, gli autori hanno rimosso ATRX nelle cellule staminali e progenitrici del sangue umano usando l’editing genetico CRISPR e hanno poi fatto maturare queste cellule in precursori dei globuli rossi in coltura. L’analisi della popolazione cellulare nel suo insieme mostrò solo un lieve calo di un gene simile all’alfa, HBM, e nessun cambiamento importante negli altri geni globinici, rispecchiando le modeste alterazioni ematologiche osservate nei pazienti. Tuttavia, analisi di colonie singole e di singole cellule rivelarono un quadro diverso. Solo un sottoinsieme di cellule prive di ATRX mostrava una forte riduzione di HBM e, in misura minore, dei principali geni dell’alfa-globina. Quelle stesse cellule presentavano firme di una risposta al danno del DNA attivata, inclusi marcatori aumentati di DNA rotto e una maggiore modificazione di un’istona (H2A) associata alla riparazione del danno e alla silenziamento dei geni vicini. Ciò suggerisce che la downregulation dell’alfa-globina avvenga principalmente nelle cellule in cui la perdita di ATRX ha permesso l’accumulo di danni locali al DNA.
Un ripetuto ricco di G come punto debole
Il gruppo si è quindi concentrato sul VNTR ricco di G inserito in un pseudogene vicino chiamato HBZP1. Utilizzando una linea cellulare eritroide umana immortalizzata, hanno monitorato il legame di ATRX nell’intera regione dell’alfa-globina e hanno scoperto che ATRX viene reclutato specificamente su questo VNTR quando il DNA circostante è trascritto. Hanno progettato un sistema in cui ATRX poteva essere degradato rapidamente e hanno osservato che la perdita di ATRX riduceva l’espressione di HBM, riproducendo ancora il fenotipo della malattia. Colpisce che, quando hanno eliminato il VNTR dal genoma, la rimozione di ATRX non abbassava più i livelli di HBM. Farmaci che stabilizzano le insolite strutture a quattro filamenti del DNA note come G-quadruplex provocarono una diminuzione simile dell’espressione di HBM, ma solo quando il VNTR era presente. Analisi a livello genomico rivelarono che molti altri geni misregolati dalla perdita di ATRX contengono anch’essi elementi ripetuti ricchi di GC, indicando una vulnerabilità generale in questi siti.
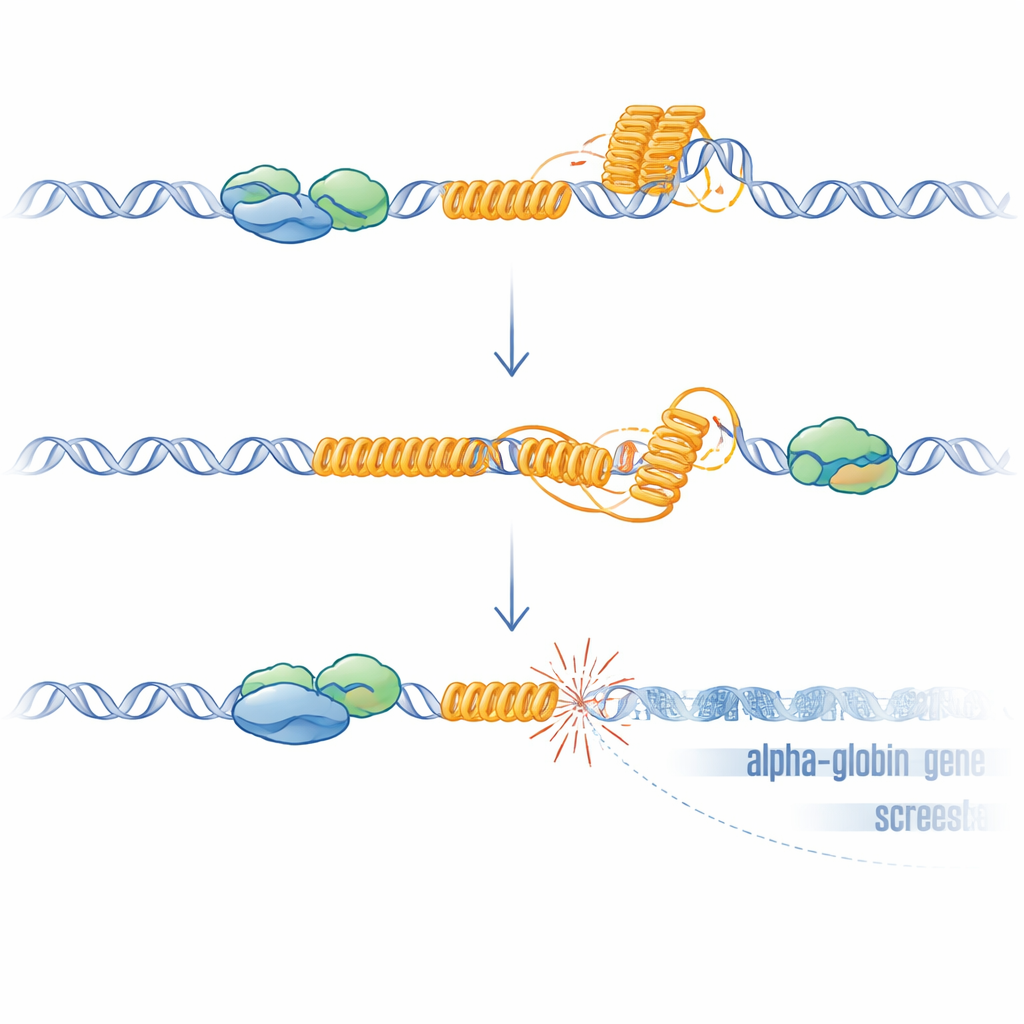
Dalle forme di DNA insolite ai geni danneggiati
I ripetuti ricchi di G come questo VNTR possono ripiegarsi in G-quadruplex e favorire la formazione di R-loop, strutture ibride in cui l’RNA appena sintetizzato rimane attaccato al filamento di DNA stampo. Entrambe le strutture possono rallentare o bloccare la macchina che copia e legge il DNA, causando stress e rotture. I ricercatori hanno mostrato che, in assenza di ATRX, le R-loop aumentavano in tutto il genoma e risultavano particolarmente elevate al VNTR. Quando sovraesprimevano RNase H, un enzima che rimuove le R-loop, l’espressione di HBM si è parzialmente ripristinata, sostenendo un ruolo causale di queste strutture. Per testare se il danno al DNA da solo fosse sufficiente a silenziare i geni vicini, hanno usato CRISPR per creare rotture mirate appena a monte di HBM in cellule in cui il VNTR era stato eliminato. Queste rotture artificiali, anche in assenza della ripetizione, ridussero di nuovo HBM e, in misura minore, i geni dell’alfa-globina, con il gene più vicino che risultava il più colpito. Questo effetto dipendente dalla distanza corrisponde a quanto osservato nei pazienti ed è coerente con la nota propagazione della repressione trascrizionale a partire dai siti di rottura a doppio filamento.
Cosa significa per la malattia e oltre
Nel complesso, il lavoro delinea un modello chiaro: nelle cellule sane, ATRX si lega a un ripetuto ricco di G vicino ai geni dell’alfa-globina durante la trascrizione, contribuendo a prevenire o sciogliere G-quadruplex e R-loop e quindi proteggendo la regione dal danno al DNA. Quando ATRX manca, queste insolite strutture di DNA e RNA si accumulano sulla ripetizione, portando a rotture locali del DNA, attivazione della risposta al danno e a un ambiente cromatinico repressivo che attenua l’espressione dei geni vicini in modo dipendente dalla distanza, con HBM il più colpito. Questo meccanismo spiega perché la sindrome ATR-X provoca solo una alfa-talassemia lieve e irregolare, perché la gravità varia con la lunghezza della ripetizione e perché i modelli murini privi di questa ripetizione specifica dell’uomo non mostrano lo stesso difetto ematico. Più in generale, suggerisce che sequenze ripetute e ricche di G disseminate nel nostro genoma possano agire come faglie nascoste: se fattori protettivi come ATRX vengono meno, possono diventare punti caldi di instabilità che rimodulano silenziosamente l’attività genica nello sviluppo, nell’invecchiamento e nel cancro.
Citazione: Shen, Y., Gupta, K., Tan-Wong, S.M. et al. ATRX loss couples genome instability at a G-rich repeat to dysregulation of human alpha-globin expression. Nat Commun 17, 2749 (2026). https://doi.org/10.1038/s41467-026-69169-7
Parole chiave: ATRX, alfa-globina, danno al DNA, G-quadruplex, R-loop