Clear Sky Science · he
אובדן ATRX מקשר בין אי־יציבות הגנום בחזרה עשירה ב-G לוויסות לקוי של ביטוי האלפא־גלובין האנושי
מדוע זה חשוב לדם ולסרטן
תאי הדם האדומים שלנו תלויים בוויסות מדויק של הגנים שמייצרים המוגלובין, החלבון שמעביר חמצן. חלבון הנקרא ATRX קשור ל‑DNA ומסייע לשמור על יציבותו, ומוטציות ב‑ATRX גורמות לצורה תורשתית של אנמיה עם פיגור שיכולות להופיע גם בשכיחות גבוהה בסוגי סרטן שונים. המחקר הזה משתמש במכלול גני האלפא־גלובין כמערכת ניסוי כדי להראות, ברזולוציה מולקולרית, כיצד אובדן ATRX עלול לפגוע ב‑DNA במקטע חוזר ולהשבית בשקט גנים סמוכים. הבנת שרשרת האירועים הזו מסייעת להסביר מחלה אנושית נדירה ומאירה כיצד אי־יציבות גנומית יכולה לשנות פעילות גנים בהיקפים רחבים יותר.
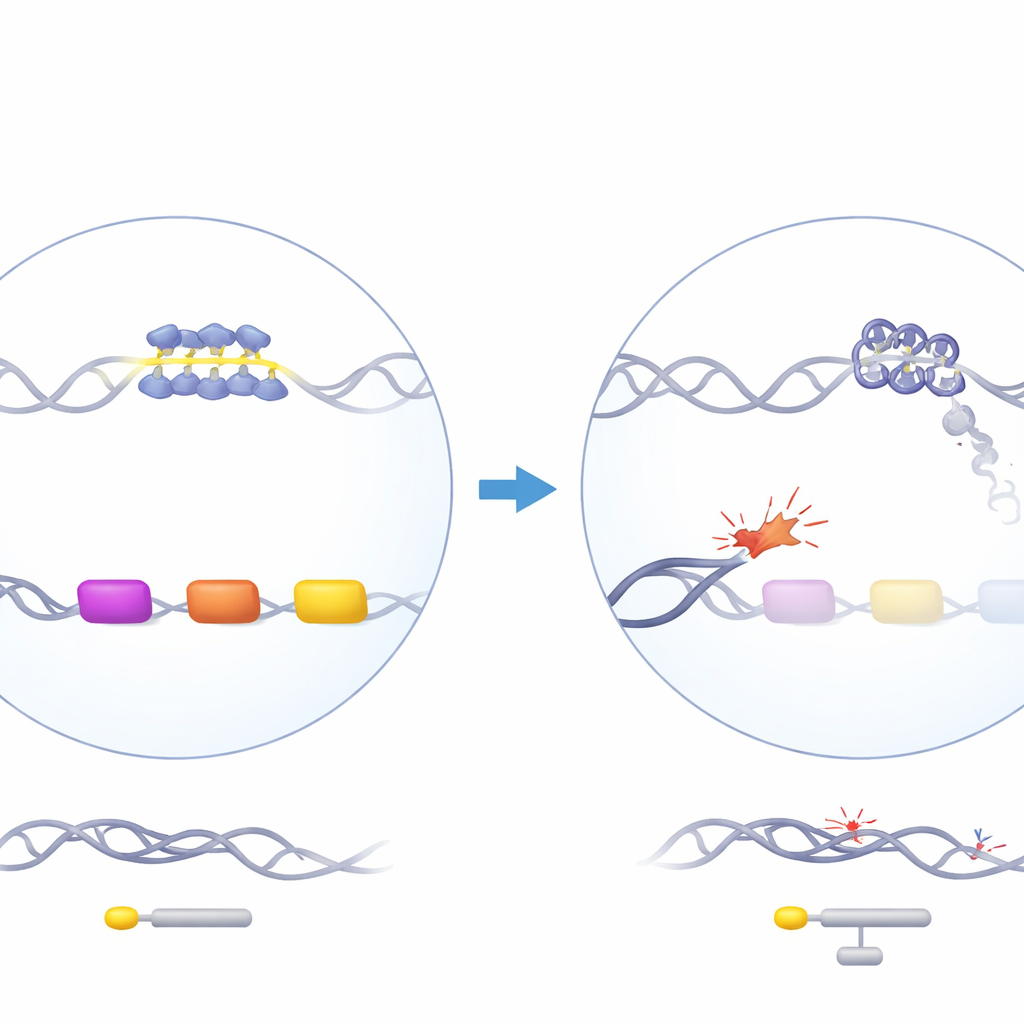
חלבון שומר עם השפעה מסתורית
ATRX הוא חלבון לרה‑אופרציה של הכרומטין שעוזר לארגן את ה‑DNA ומשתתף ברפליקציה, שיעתוק ותיקון DNA. כש‑ATRX מוטנטי בבני אדם, החולים מפתחים תסמונת ATR‑X, הכוללת תת‑המוגלובינמיה אלפא קלה: הגנים של האלפא־גלובין, הנחוצים לבניית המוגלובין, פועלים ברמה נמוכה. באופן מעניין, אובדן ATRX משפיע על האלפא־גלובין אך לא על הבטא־גלובין, אף על פי ששניהם נדרשים בכמויות שוות. גני האלפא־גלובין נמצאים באזור עשיר בגנים ובעשיר ב‑GC בכרומוזום 16 הכולל מספר אלמנטים חוזרים ב‑DNA, וביניהם וריאבל נומבר טנדם ריפיט (VNTR) עשיר במיוחד ב‑G הממוקם מעט מעלה לזרם מהגנים הדומים לאלפא. עבודות גנטיות קודמות הראו שאורך החזרה הזו מתאם עם חומרת הירידה בביטוי האלפא־גלובין בחולים, מרמז שהמקטע המוזר הזה של ה‑DNA עשוי להיות במרכז הבעיה.
התמקדות בתאים המושפעים
כדי לחקור את הנושא, החוקרים הסירו את ATRX בתאי גזע ומחוללי דם אנושיים באמצעות עריכת גנים CRISPR ולאחר מכן בשלו תאים אלה לתאים מקדימים של דם אדום בתרבית. הסתכלות על האוכלוסייה כולה הראתה רק ירידה קלה בגene דמוי־אלפא אחד, HBM, ולא שינוי משמעותי בגנים אחרים של גלובין, ומה שחיק מהשינויים הממוצעים בדם שנצפו בחולים. עם זאת, ניתוח קווי מושבה בודדים ותאים בודדים חשף תמונה שונה. רק תת־קבוצה של תאים חסרי ATRX הראתה ירידה חדה ב‑HBM ובמידה פחותה בגני האלפא הראשיים. אותם תאים הראו גם סימני תגובה לנזק ב‑DNA, כולל עלייה בסמנים של DNA שבור והגברה של שינוי בחלבון היסטון (H2A) המקושר לתיקון נזק ולהשתקה של גנים סמוכים. ממצאים אלה מרמזים שהדיכוי של האלפא־גלובין מתרחש בעיקר בתאים שבהם אובדן ATRX איפשר הצטברות נזק מקומי ב‑DNA.
חוסר תיאום במקטע חוזר עשיר ב‑G כנקודת תורפה
הצוות התמקד אז ב‑VNTR העשיר ב‑G המשולב בפסאודו‑גן סמוך בשם HBZP1. באמצעות קו תאי אריתרואידי אנושי ממוות, עקבו אחרי קשירת ATRX ברחבי אזור האלפא־גלובין וגילו ש‑ATRX מגוייס במיוחד ל‑VNTR הזה כאשר ה‑DNA הסמוך מועתק. הם הנדסו מערכת שבה ATRX יכול היה להיות מפורק במהירות והתבוננו כי אובדן ATRX הקטין את ביטוי HBM, שוב המדמה את פנוטיפ המחלה. באופן בולט, כאשר הם מחקו את ה‑VNTR עצמו מן הגנום, הסרת ATRX כבר לא הורידה את רמות HBM. תרופות שמייצבות מבני DNA יוצאי דופן בת ארבעה תילים, המכונים G‑קוואדראפלקסים, גרמו לירידה דומה בביטוי HBM, אך רק אם ה‑VNTR נוכח. ניתוחים על היקף הגנום הראו שגנים רבים נוספים שמשתנים בשל אובדן ATRX גם כן מכילים אלמנטים חוזרים עשירים ב‑GC, ומצביעים על פגיעות כללית באתרי כזה.
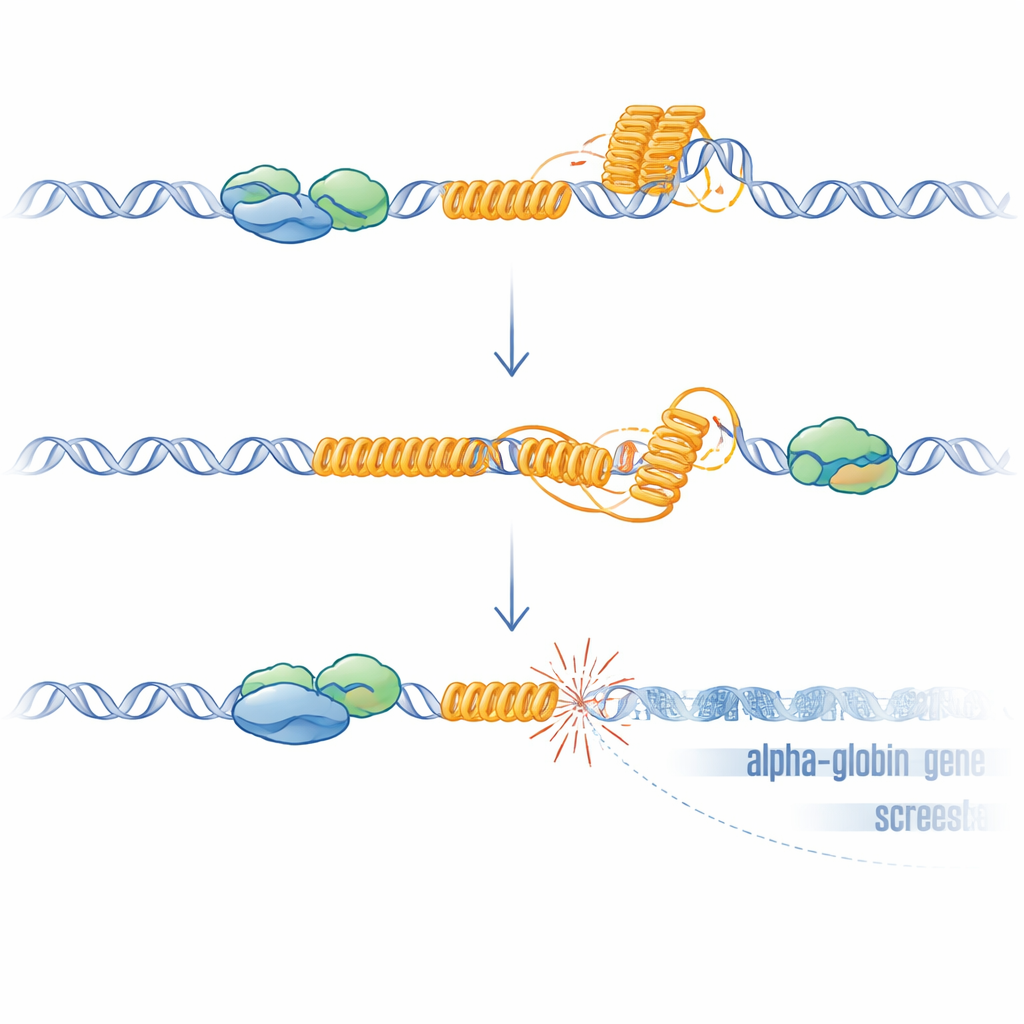
ממבנים DNA מוזרים לגנים שבורים
חזרות עשירות ב‑G כמו ה‑VNTR הזה יכולות לקפל למבני G‑קוואדראפלקס ולקדם היווצרות R‑לופים, מבנים היברידיים שבהם RNA חדש נשאר תקוע על תבנית ה‑DNA. שני המבנים הללו יכולים להאט או לעצור את המערכות שמעתיקות וקוראות DNA, ולגרום ללחץ ושבירה. החוקרים הראו כי בלי ATRX, R‑לופים עלו ברחבי הגנום והיו מוגברים במיוחד ב‑VNTR. כאשר הם הביטו ביטוי יתר של RNase H, אנזים שמסיר R‑לופים, ביטוי HBM התאושש בחלקו, תומך בתפקיד סיבתי למבנים אלה. כדי לבדוק האם נזק ל‑DNA בלבד מספיק להשתיק את הגנים הסמוכים, הם השתמשו ב‑CRISPR ליצירת שבירות ממוקדות ממש מעלה לזרם של HBM בתאים שבהם ה‑VNTR הוסר. שבירות מלאכותיות אלה, אפילו בהיעדר החזרה, שוב הורידו את HBM ובמידה פחותה את גני האלפא, כאשר הגן הקרוב ביותר הושפע ביותר. האפקט התלוי מרחק זה תואם את מה שנצפה בחולים ומתיישב עם הדיווחים על התפשטות השתיקה השעתוקית מאתרי שברי גדילי DNA כפולים.
מה המשמעות לכך למחלה ולמעבר לה
ביחד, העבודה מציגה מודל ברור: בתאים בריאים, ATRX נקשר לחזרה עשירה ב‑G סמוך לגני האלפא־גלובין בזמן שיועתקת, ועוזר למנוע או לפרק G‑קוואדראפלקסים ו‑R‑לופים ובכך מגן על האזור מנזקי DNA. כאשר ATRX חסר, מבני DNA ו‑RNA יוצאי דופן אלה מצטברים בחזרה, גורמים לשברי DNA מקומיים, להפעיל תגובת נזק וליצור כרומטין מדכא שמחליש את הביטוי של גנים סמוכים באופן תלוי מרחק, כאשר HBM נפגעת הכי חזק. מנגנון זה מסביר מדוע תסמונת ATR‑X גורמת רק לאלפא‑תלסמיה קלה ומפוצלת, מדוע החומרה משתנה לפי אורך החזרה, ולמה מודלים עכבריים החסרים את החזרה הייחודית לאדם אינם מראים את התקלה הדמית הזו. באופן רחב יותר, זה מציע כי רצפים חוזרים ועשירים ב‑G המפוזרים בגנום שלנו יכולים לפעול כקווי פיצול נסתרים: אם גורמי מגן כמו ATRX נכשלים, הם עלולים להפוך לאתרים חמים של אי‑יציבות שמשנים בשקט את פעילות הגנים בהתפתחות, בהזדקנות ובסרטן.
ציטוט: Shen, Y., Gupta, K., Tan-Wong, S.M. et al. ATRX loss couples genome instability at a G-rich repeat to dysregulation of human alpha-globin expression. Nat Commun 17, 2749 (2026). https://doi.org/10.1038/s41467-026-69169-7
מילות מפתח: ATRX, אלפא־גלובין, נזקי DNA, G‑קוואדראפלקס, R‑לופים