Clear Sky Science · ar
فقدان ATRX يربط عدم استقرار الجينوم عند متكرر غني بالجوانين بخلل تنظيم تعبير الجلوبين-ألفا البشري
لماذا هذا مهم للدم والسرطان
تعتمد خلايا الدم الحمراء لدينا على ضبط دقيق للجينات المسؤولة عن صنع الهيموغلوبين، البروتين الذي ينقل الأكسجين. بروتين يُدعى ATRX يرتبط بالحمض النووي ويساعد في الحفاظ على استقراره، وطفرات في ATRX تسبب شكلاً موروثًا من فقر الدم المصاحب لاضطرابٍ ذهنيّ وتشيع في عدة أنواع من السرطان. تستخدم هذه الدراسة مجموعة جينات الجلوبين-ألفا كحالة اختبار لتُظهر، بتفصيل جزيئي، كيف أن فقدان ATRX يمكن أن يتلف الحمض النووي عند موضع مكرر ويطفئ بهدوء الجينات القريبة. فهم سلسلة الأحداث هذه يساعد على تفسير اضطراب نادر لدى البشر ويسلط الضوء على كيفية تأثير عدم استقرار الجينوم على نشاط الجينات بشكل أوسع.
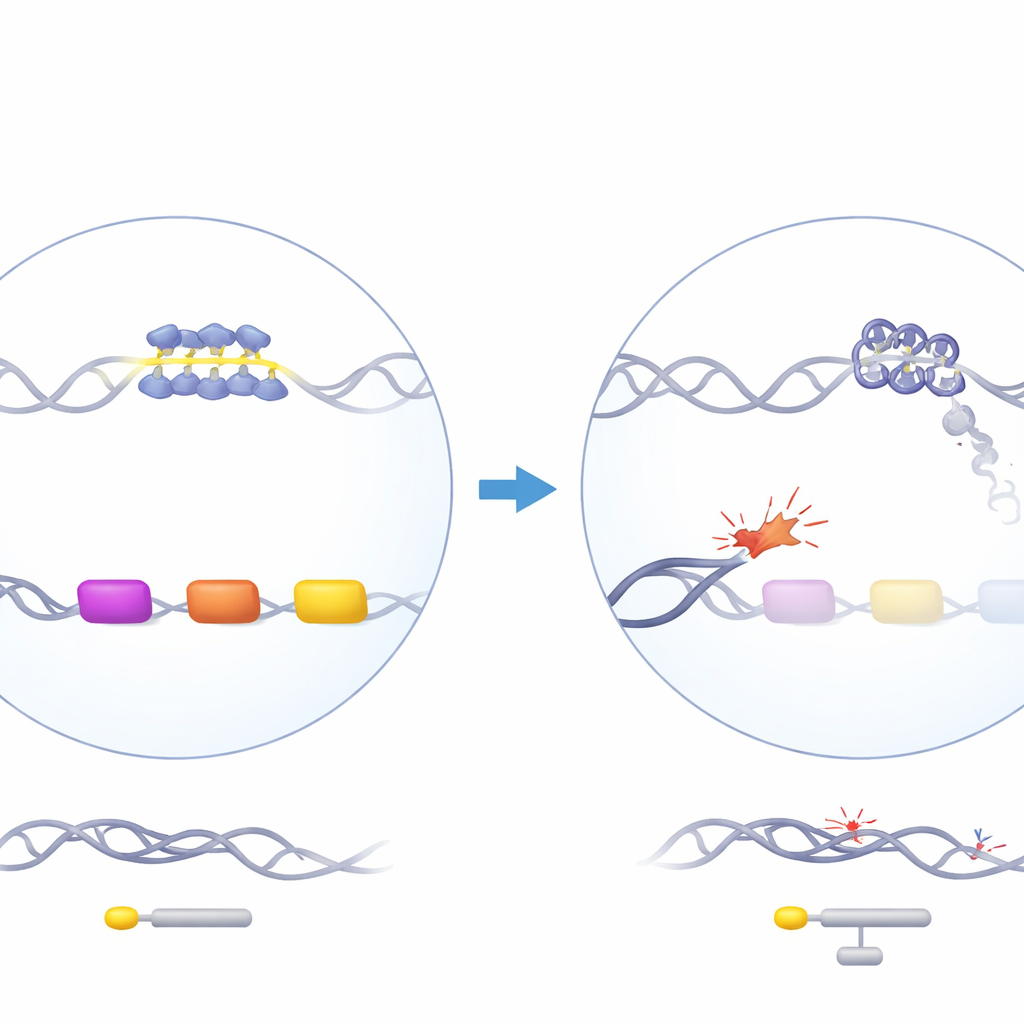
بروتين حارس بتأثير محيِّر
ATRX هو بروتين لإعادة تشكيل الكروماتين يساعد على تنظيم الحمض النووي ويشارك في النسخ والتكاثر وإصلاح الحمض النووي. عندما يتعرض ATRX للطفرات لدى الإنسان، يظهر مرض ATR-X، الذي يتضمن ثلاسيميا-ألفا خفيفة: جينات الجلوبين-ألفا، اللازمة لبناء الهيموغلوبين، تكون أقل نشاطًا. على نحو مدهش، يؤثر فقدان ATRX على الجلوبين-ألفا لكنه لا يؤثر على الجلوبين-بيتا، رغم أن كلاهما مطلوبان بكميات متساوية. تجلس جينات الجلوبين-ألفا في منطقة غنية بالجِينات وغنية بالمركبات GC على الكروموسوم 16 تحتوي على عدة عناصر مكررة من الحمض النووي، بما في ذلك تكرار متسلسل متغير الطول غني بالجوانين (VNTR) يقع مباشرة أمام جينات الجلوبين الشبيهة بالألفا. أظهرت أعمال جينية سابقة أن طول هذا التكرار يتوافق مع مدى انخفاض الجلوبين-ألفا في المرضى، ما يوحي بأن هذا المقطع الغريب من الحمض النووي قد يكون محور المشكلة.
التقريب على الخلايا المتأثرة
للتحقيق في ذلك، أزال المؤلفون ATRX من خلايا جذعية وسلفية دموية بشرية باستخدام تحرير الجينوم CRISPR ثم نَضَّجوا هذه الخلايا إلى مراحل ما قبل خلايا الدم الحمراء في استزراع. أظهر النظر إلى مجموع الخلايا انخفاضًا طفيفًا في جين شبيه واحد للألفا، HBM، ولا تغيرًا كبيرًا في جينات الجلوبين الأخرى، مما يعكس التغيرات الدموية المتواضعة المرصودة في المرضى. ومع ذلك، عندما حللوا المستعمرات الفردية والخلايا المنفردة، برزت صورة مختلفة. أظهر فقط جزء من الخلايا الناقصة ATRX انخفاضًا قويًا في HBM، وإلى درجة أقل في الجينات الرئيسية للجلوبين-ألفا. هذه الخلايا نفسها أظهرت علامات استجابة نشطة لضرر الحمض النووي، بما في ذلك ازدياد مؤشرات القطع في الحمض النووي وزيادة تعديل بروتين الهستون (H2A) المرتبط بإصلاح الضرر وكبت الجينات القريبة. هذا يشير إلى أن تقليل نشاط الجلوبين-ألفا يحدث بشكل رئيسي في الخلايا التي أدى فيها فقدان ATRX إلى تراكم ضرر موضعي في الحمض النووي.
متكرر غني بالجوانين كنقطة ضعف
ركز الفريق بعد ذلك على VNTR الغني بالجوانين المضمّن في جين زائف مجاور يُدعى HBZP1. باستخدام سلالة خلوية بشرية حمرية متحوِّلة، تعقّبوا ارتباط ATRX عبر منطقة الجلوبين-ألفا ووجدوا أن ATRX يُستَدعى تحديدًا إلى هذا VNTR عندما يكون الحمض النووي المحيط قيد النسخ. صمّموا نظامًا يمكن فيه إذابة ATRX بسرعة ولاحظوا أن فقدان ATRX خفّض تعبير HBM، مما يحاكي مرة أخرى النمط المرضي. اللافت أنه عندما حذفوا VNTR نفسه من الجينوم، لم يعد فقدان ATRX يخفض مستويات HBM. العقاقير التي تثبّت هياكل الحمض النووي غير الاعتيادية ذات الخيوط الأربعة المعروفة باسم G-quadruplexes سبّبت انخفاضًا مشابهًا في تعبير HBM، لكن فقط عند وجود VNTR. أكدت تحليلات على مستوى الجينوم أن العديد من الجينات الأخرى التي ينظّمها ATRX بشكل غير طبيعي تحتوي أيضًا عناصر مكررة غنية بـGC، مما يشير إلى قابلية عامة لهذه المواقع.
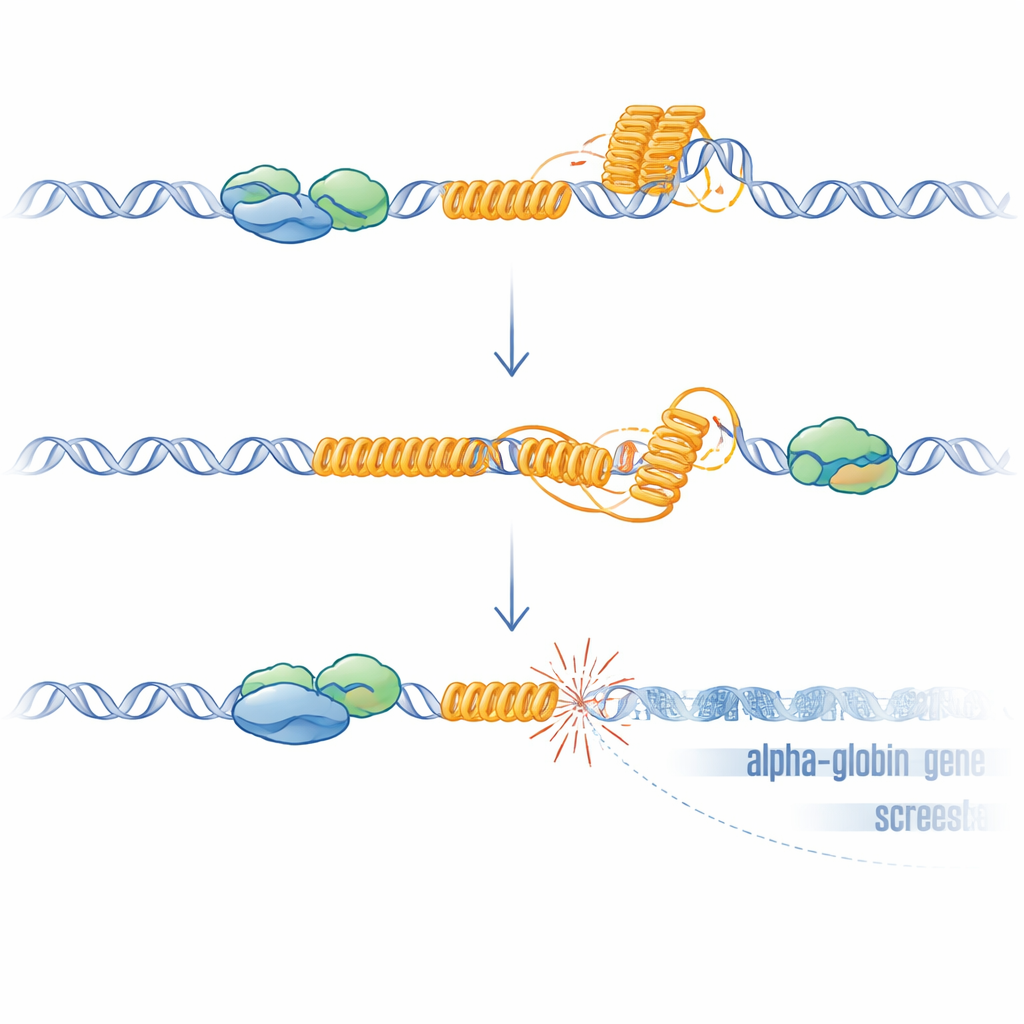
من أشكال حمض نووي غريبة إلى جينات مكسورة
يمكن أن تطوى التكرارات الغنية بالجوانين مثل هذا VNTR لتشكل G-quadruplexes وتُسهِم في تكوين R-loops، وهي هياكل هجينة يبقى فيها الحمض الريبي الجديد ملتصقًا بقالب الحمض النووي. كلا البنيتين يمكن أن تبطئ أو توقف الآلات التي تنسخ وتقرأ الحمض النووي، مسببة إجهادًا وكسورًا. أظهر الباحثون أنه بدون ATRX، ازداد عدد R-loops عبر الجينوم وارتفع بشكل خاص عند VNTR. عندما عبَّروا بكثرة عن RNase H، الإنزيم الذي يزيل R-loops، تعافى تعبير HBM جزئيًا، داعمًا دورًا سببيًا لهذه الهياكل. لاختبار ما إذا كان الضرر في الحمض النووي وحده يكفي لكبت الجينات المجاورة، استخدموا CRISPR لخلق كسور مستهدفة مباشرة أمام HBM في خلايا تم حذف VNTR منها. هذه الكسور الاصطناعية، حتى بغياب التكرار، قلّصت مجددًا HBM وبدرجة أقل جينات الجلوبين-ألفا، مع تأثر أقرب جين أكثر من غيره. هذا التأثير المعتمد على المسافة يتطابق مع ما يُرى في المرضى ويتفق مع الانتشار المعروف لكبت النسخ بعيدًا عن مواقع الكسور المزدوجة السلسلة.
ماذا يعني ذلك للمرض وما وراءه
تجمع النتائج معًا لتوضّح نموذجًا واضحًا: في الخلايا السليمة، يرتبط ATRX بتكرار غني بالجوانين قرب جينات الجلوبين-ألفا أثناء نسخه، مساعدًا على منع أو تفكيك G-quadruplexes وR-loops وبالتالي حماية المنطقة من ضرر الحمض النووي. عندما يغيب ATRX، تتراكم هذه الهياكل غير المعتادة من الحمض النووي والحمض النووي الريبي عند التكرار، مما يؤدي إلى كسور موضعية في الحمض النووي، وتنشيط استجابة الضرر، وبيئة كروماتينية قمعية تُضعِف تعبير الجينات القريبة بطريقة تعتمد على المسافة، حيث يتأثر HBM أشد الضرر. يشرح هذا الآلية سبب تسبب متلازمة ATR-X في ثلاسيميا-ألفا خفيفة ومبعثرة فقط، ولماذا تختلف شدة المرض باختلاف طول التكرار، ولماذا لا تظهر نماذج الفأر الخالية من هذا التكرار الخاص بالإنسان نفس العيب الدموي. وبشكل أوسع، يقترح أن التسلسلات المكررة والغنية بالجوانين المنتشرة في جينومنا يمكن أن تعمل كصدوع خفية: إذا فشلت عوامل الحماية مثل ATRX، يمكن أن تصبح نقاطًا ساخنة لعدم الاستقرار تعيد ببطء ضبط نشاط الجينات خلال التطور والشيخوخة والسرطان.
الاستشهاد: Shen, Y., Gupta, K., Tan-Wong, S.M. et al. ATRX loss couples genome instability at a G-rich repeat to dysregulation of human alpha-globin expression. Nat Commun 17, 2749 (2026). https://doi.org/10.1038/s41467-026-69169-7
الكلمات المفتاحية: ATRX, الجلوبين-ألفا, ضرر الحمض النووي, أربعة سوابق غوانينية (G-quadruplex), R-loops