Clear Sky Science · fr
La perte d’ATRX relie l’instabilité du génome sur une répétition riche en G à la dérégulation de l’expression de l’alpha-globine humaine
Pourquoi cela importe pour le sang et le cancer
Nos globules rouges dépendent d’un contrôle fin des gènes qui fabriquent l’hémoglobine, la protéine qui transporte l’oxygène. Une protéine appelée ATRX se lie à l’ADN et contribue à maintenir sa stabilité ; des mutations d’ATRX provoquent une forme d’anémie héréditaire associée à un retard intellectuel et sont fréquentes dans plusieurs cancers. Cette étude utilise le cluster de gènes alpha-globine comme modèle pour montrer, au niveau moléculaire, comment la perte d’ATRX peut endommager l’ADN au niveau d’un segment répété et silencieusement éteindre des gènes voisins. Comprendre cette chaîne d’événements aide à expliquer un trouble humain rare et éclaire plus généralement la façon dont l’instabilité du génome peut modifier l’activité génique.
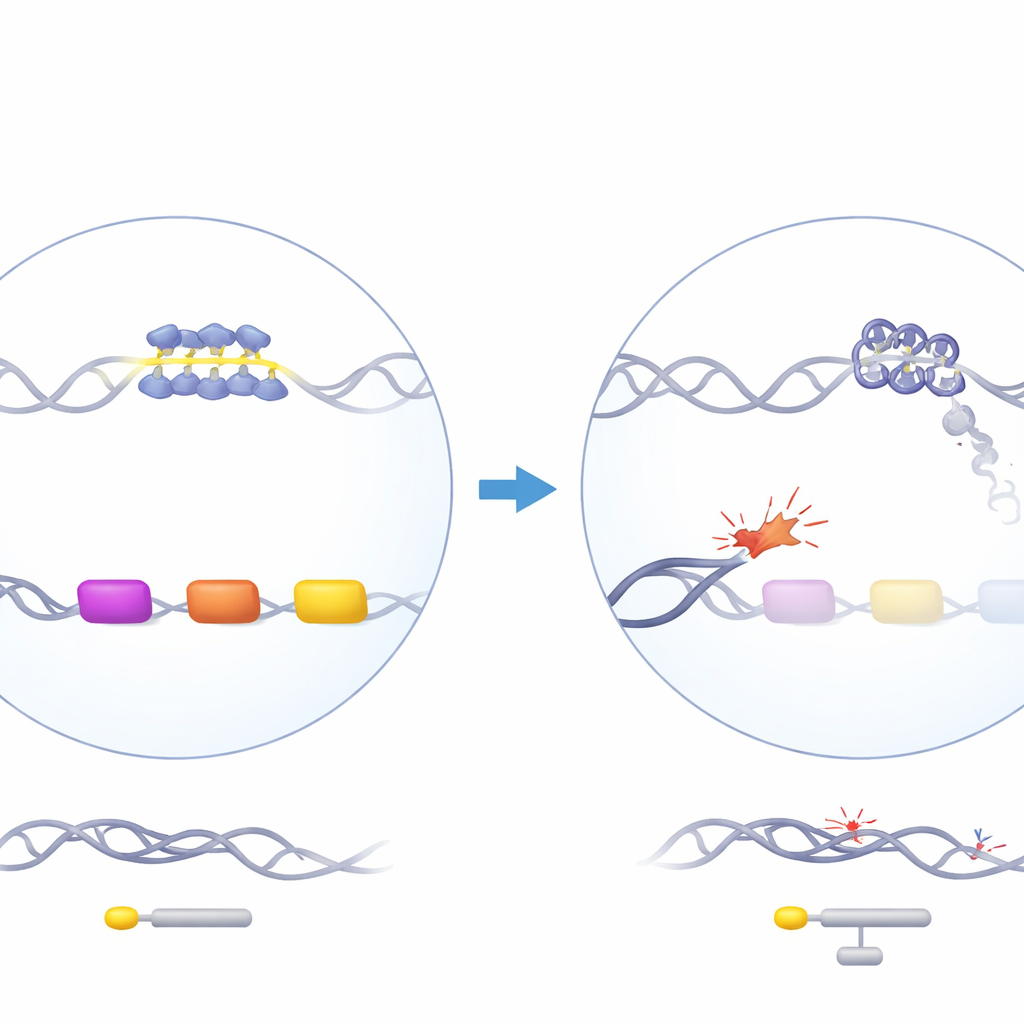
Une protéine gardienne au effet déroutant
ATRX est une protéine de remodelage de la chromatine qui aide à organiser l’ADN et intervient lors de la réplication, de la transcription et de la réparation de l’ADN. Lorsqu’ATRX est muté chez l’humain, les patients développent le syndrome ATR‑X, qui inclut une alpha-thalassémie légère : leurs gènes alpha-globine, nécessaires à la fabrication de l’hémoglobine, sont sous‑actifs. Fait intriguant, la perte d’ATRX affecte l’alpha‑globine mais pas la bêta‑globine, bien que les deux soient requises en quantités équivalentes. Les gènes alpha-globine se trouvent dans une région riche en gènes et en GC du chromosome 16 qui contient plusieurs éléments d’ADN répétitifs, y compris une répétition en tandem de nombre variable (VNTR) particulièrement riche en G située juste en amont des gènes de type alpha. Des travaux génétiques antérieurs ont montré que la longueur de cette répétition corrèle avec l’ampleur de la réduction de l’alpha-globine chez les patients, suggérant que cet étrange segment d’ADN pourrait être au cœur du problème.
Approche fine des cellules affectées
Pour enquêter, les auteurs ont supprimé ATRX dans des cellules souches et progénitrices sanguines humaines à l’aide de l’édition génique CRISPR, puis ont maturé ces cellules en précurseurs érythroïdes en culture. L’analyse de la population cellulaire dans son ensemble montrait seulement une baisse modérée d’un gène de type alpha, HBM, et aucun changement majeur dans les autres gènes de globine, reflétant les modifications sanguines modestes observées chez les patients. Cependant, l’analyse de colonies individuelles et de cellules uniques a révélé un autre tableau. Seul un sous‑ensemble de cellules déficientes en ATRX présentait une forte réduction de HBM et, dans une moindre mesure, des gènes alpha principaux. Ces mêmes cellules montraient des signatures d’activation de la réponse aux dommages de l’ADN, y compris une augmentation des marqueurs d’ADN cassé et une modification accrue d’une histone (H2A) liée à la réparation des dommages et au silence des gènes voisins. Cela suggère que la réduction de l’alpha‑globine survient principalement dans les cellules où la perte d’ATRX a permis l’accumulation de dommages locaux à l’ADN.
Une répétition riche en G comme point faible
L’équipe s’est alors concentrée sur la VNTR riche en G intégrée dans un pseudo‑gène voisin appelé HBZP1. En utilisant une lignée cellulaire érythroïde humaine immortalisée, ils ont suivi le liaison d’ATRX à travers la région alpha‑globine et trouvé qu’ATRX est spécifiquement recruté sur cette VNTR lorsque l’ADN environnant est transcrit. Ils ont mis au point un système permettant la dégradation rapide d’ATRX et observé que la perte d’ATRX réduisait l’expression de HBM, reproduisant à nouveau le phénotype pathologique. Fait remarquable, lorsqu’ils ont supprimé la VNTR du génome, la suppression d’ATRX n’entraînait plus de baisse de HBM. Des médicaments qui stabilisent les structures d’ADN inhabituelles à quatre brins appelées G‑quadruplexes provoquaient une diminution similaire de l’expression de HBM, mais seulement en présence de la VNTR. Des analyses à l’échelle du génome ont révélé que de nombreux autres gènes dérégulés par la perte d’ATRX contiennent aussi des éléments répétitifs riches en GC, pointant vers une vulnérabilité générale en ces sites.
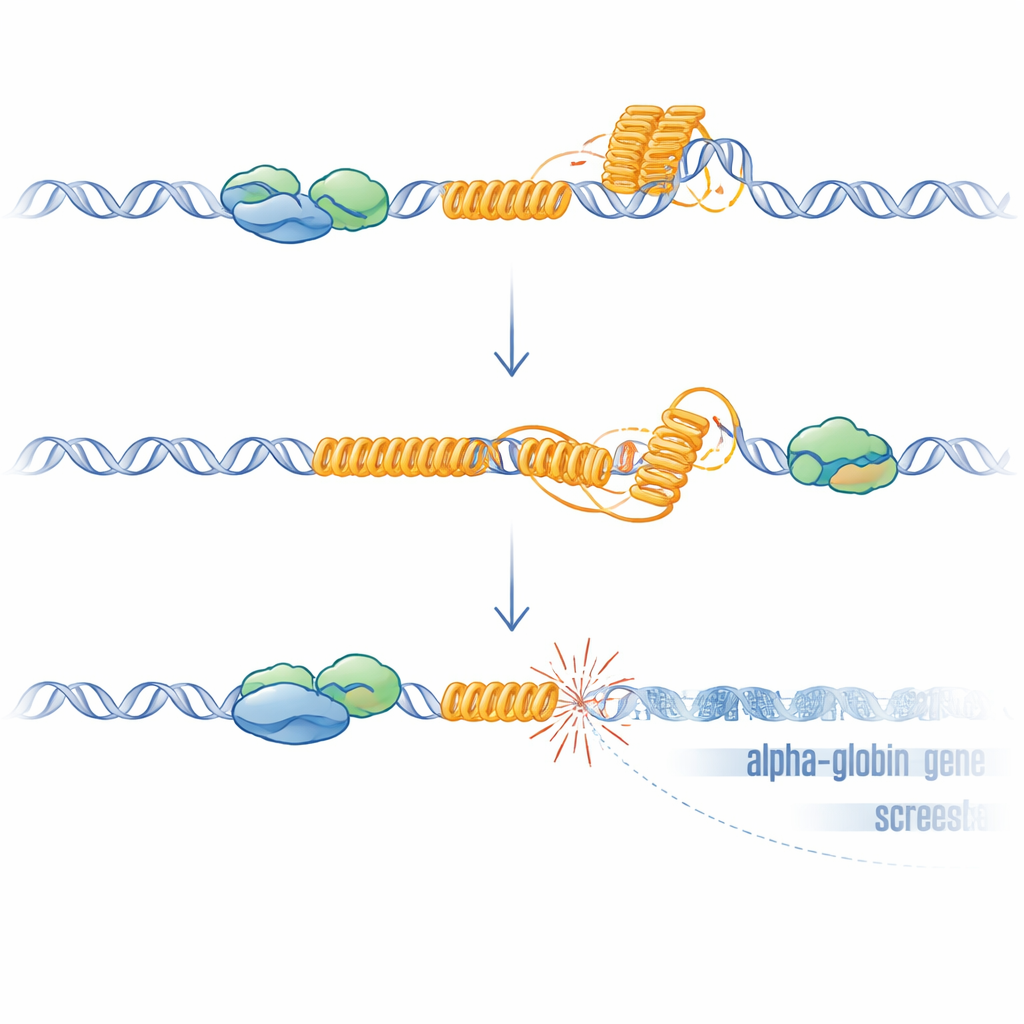
D’un ADN aux formes étranges à des gènes brisés
Les répétitions riches en G comme cette VNTR peuvent se replier en G‑quadruplexes et favoriser la formation de R‑boucles, structures hybrides où l’ARN nouvellement synthétisé reste accroché au brin d’ADN matrice. Ces deux structures peuvent ralentir ou bloquer les machineries de copie et de lecture de l’ADN, provoquant stress et cassures. Les chercheurs ont montré que, sans ATRX, les R‑boucles augmentent à l’échelle du génome et sont particulièrement élevées au niveau de la VNTR. Lorsqu’ils ont surexprimé la RNase H, une enzyme qui élimine les R‑boucles, l’expression de HBM a partiellement récupéré, soutenant un rôle causal de ces structures. Pour tester si les dommages à l’ADN suffisaient à silencier les gènes voisins, ils ont utilisé CRISPR pour créer des cassures ciblées juste en amont de HBM dans des cellules dont la VNTR avait été supprimée. Ces cassures artificielles, même en l’absence de la répétition, ont de nouveau réduit HBM et, plus faiblement, les gènes alpha‑globine, le gène le plus proche étant le plus affecté. Cet effet dépendant de la distance correspond à ce qui est observé chez les patients et est cohérent avec la propagation connue de la répression transcriptionnelle à partir de sites de cassures double brin.
Ce que cela signifie pour la maladie et au‑delà
Pris ensemble, ces travaux proposent un modèle clair : dans les cellules saines, ATRX se lie à une répétition riche en G proche des gènes alpha‑globine lors de leur transcription, aidant à prévenir ou à dissoudre les G‑quadruplexes et les R‑boucles et protégeant ainsi la région des dommages à l’ADN. Lorsque ATRX manque, ces structures d’ADN et d’ARN anormales s’accumulent à la répétition, entraînant des cassures locales, l’activation d’une réponse aux dommages et un environnement chromatinien répressif qui atténue l’expression des gènes voisins de manière dépendante de la distance, HBM étant le plus touché. Ce mécanisme explique pourquoi le syndrome ATR‑X provoque une alpha‑thalassémie légère et hétérogène, pourquoi la sévérité varie avec la longueur de la répétition, et pourquoi les modèles murins dépourvus de cette répétition spécifique à l’humain n’affichent pas le même défaut sanguin. Plus généralement, cela suggère que des séquences répétitives riches en G disséminées dans notre génome peuvent agir comme des lignes de faille cachées : si des facteurs protecteurs comme ATRX font défaut, elles peuvent devenir des points chauds d’instabilité qui reconfigurent discrètement l’activité génique lors du développement, du vieillissement et du cancer.
Citation: Shen, Y., Gupta, K., Tan-Wong, S.M. et al. ATRX loss couples genome instability at a G-rich repeat to dysregulation of human alpha-globin expression. Nat Commun 17, 2749 (2026). https://doi.org/10.1038/s41467-026-69169-7
Mots-clés: ATRX, alpha-globine, dommages à l’ADN, G-quadruplex, R-boucles