Clear Sky Science · ru
Потеря ATRX связывает нестабильность генома на G-богатом повторе с дисрегуляцией экспрессии человеческого альфа‑глобина
Почему это важно для крови и рака
Наши красные кровяные клетки зависят от тонко настроенного контроля генов, кодирующих гемоглобин — белок, который переносит кислород. Белок ATRX связывается с ДНК и помогает поддерживать её стабильность; мутации в ATRX вызывают форму наследственной анемии с интеллектуальной недостаточностью и часто встречаются при нескольких видах рака. В этом исследовании на кластере генов альфа‑глобина в молекулярных деталях показано, как утрата ATRX может вызывать повреждение ДНК на повторяющемся участке и тем самым «тихо» выключать близлежащие гены. Понимание этой последовательности событий помогает объяснить редкое заболевание человека и проливает свет на то, как нестабильность генома в целом может менять активность генов.
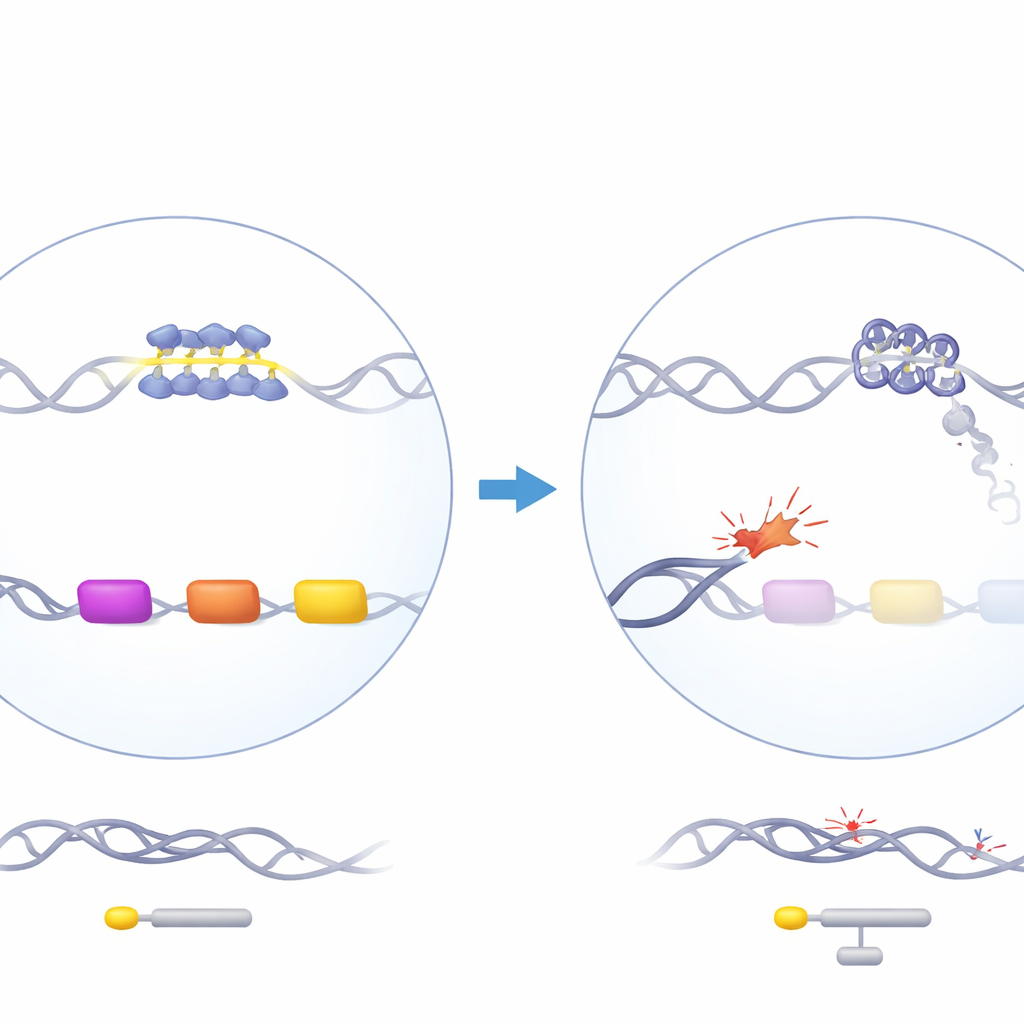
Белок‑страж с загадочным эффектом
ATRX — это хроматин‑ремоделирующий белок, который помогает организовывать ДНК и участвует в репликации, транскрипции и ремонте ДНК. При мутациях ATRX у людей развивается синдром ATR‑X, включающий лёгкую альфа‑талассемию: их гены альфа‑глобина, необходимые для сборки гемоглобина, недостаточно активны. Что интересно, потеря ATRX влияет на альфа‑глобин, но не на бета‑глобин, хотя оба требуются в равных количествах. Гены альфа‑глобина локализуются в богатом генами и GC‑богатом участке хромосомы 16, содержащем несколько повторяющихся элементов ДНК, включая особенно G‑богатый VNTR (вариабельный повтор с тандемной перестановкой), расположенный сразу выше генов, похожих на альфа‑глобин. Ранее генетические данные показали, что длина этого повтора коррелирует с тем, насколько сильно у пациентов снижается альфа‑глобин, что намекало на центральную роль этого необычного участка ДНК.
Уточнение картины в поражённых клетках
Чтобы исследовать это, авторы удалили ATRX в человеческих гемопоэтических стволовых и предшественниковых клетках с помощью CRISPR и затем довели эти клетки до предшественников красных кровяных клеток в культуре. Анализ популяции клеток в целом показал лишь небольшой спад в одном альфа‑похожем гене, HBM, и без заметных изменений в других глобин‑генах, что отражает умеренные изменения крови у пациентов. Однако анализ отдельных колоний и отдельных клеток показал иную картину. Только подмножество клеток с дефицитом ATRX демонстрировало сильное снижение HBM и, в меньшей степени, основных генов альфа‑глобина. Эти же клетки имели признаки активации ответа на повреждение ДНК, включая увеличение маркеров разрывов ДНК и усиленную модификацию гистона (H2A), связанную с ремонтом повреждений и подавлением соседних генов. Это указывало, что сниженная экспрессия альфа‑глобина возникает главным образом в клетках, где утрата ATRX позволила накопиться локальным повреждениям ДНК.
Проблемный G‑богатый повтор как слабое место
Команда сосредоточилась на G‑богатом VNTR, встроенном в близкий псевдоген HBZP1. На иммортализованной человеческой эритроидной клеточной линии они отслеживали связывание ATRX по региону альфа‑глобина и обнаружили, что ATRX специфически привлекается к этому VNTR во время транскрипции окружающей ДНК. Они создали систему, в которой ATRX можно быстро деградировать, и наблюдали, что потеря ATRX снижает экспрессию HBM, снова воспроизводя фенотип болезни. Поразительно, что при делеции самого VNTR из генома удаление ATRX больше не снижало уровни HBM. Лекарства, стабилизирующие необычные четырёхцепочечные структуры ДНК, известные как G‑четверные спирали, вызывали похожее падение экспрессии HBM, но только при наличии VNTR. Геномные анализы показали, что многие другие гены, нарушенно регулируемые при потере ATRX, также содержат GC‑богатые повторяющиеся элементы, указывая на общую уязвимость в таких участках.
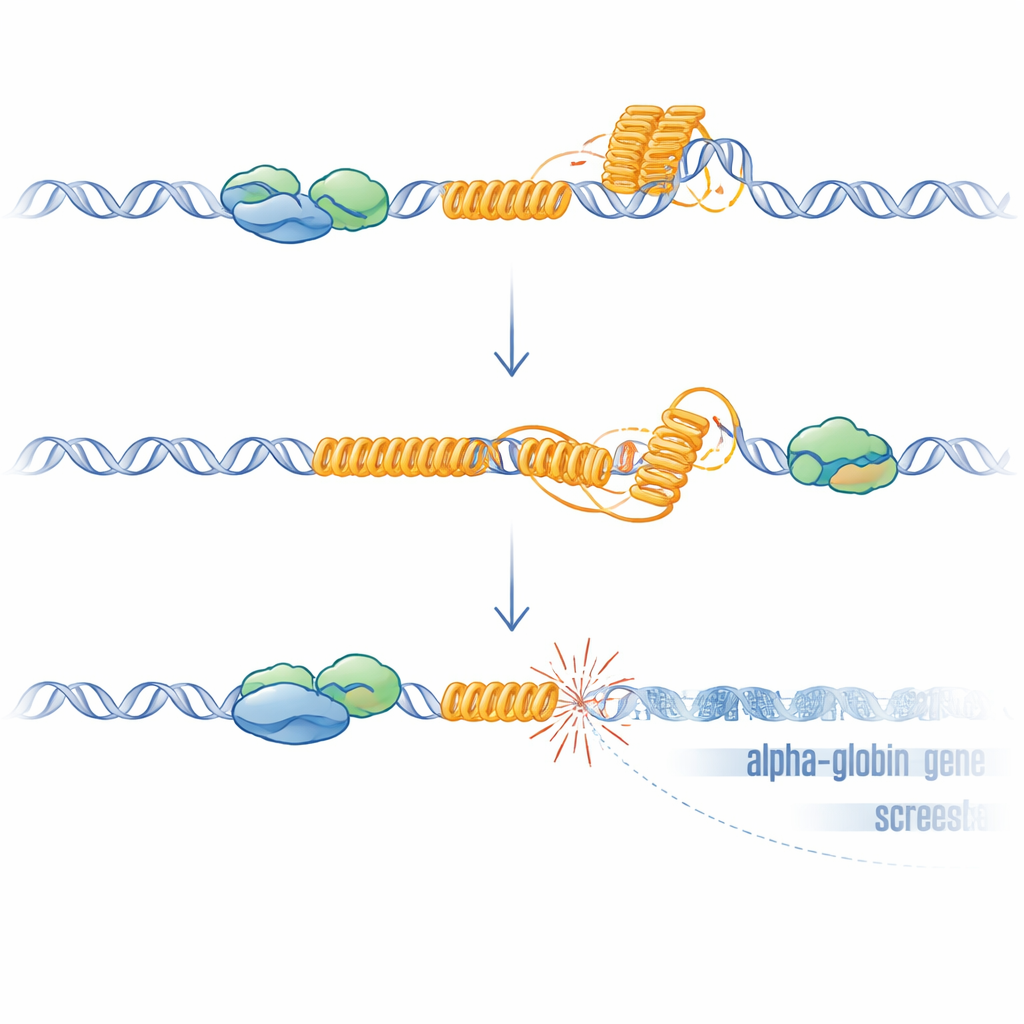
От необычных форм ДНК до повреждённых генов
G‑богатые повторы, такие как этот VNTR, могут складываться в G‑четверные спирали и способствовать образованию R‑петель — гибридных структур, в которых вновь синтезированная РНК остаётся прилепшей к матрице ДНК. Обе структуры могут замедлять или останавливать машинерию, копирующую и читающую ДНК, вызывая стресс и разрывы. Исследователи показали, что при отсутствии ATRX R‑петли увеличиваются по всему геному и особенно повышены на VNTR. При сверхэкспрессии RNase H — фермента, удаляющего R‑петли — экспрессия HBM частично восстановилась, что поддерживает причинную роль этих структур. Чтобы проверить, достаточно ли одного лишь повреждения ДНК для подавления соседних генов, они с помощью CRISPR создали целенаправленные разрывы прямо выше HBM в клетках, где VNTR был удалён. Эти искусственные разрывы, даже при отсутствии повтора, снова снижали HBM и, в меньшей степени, гены альфа‑глобина, причём ближний ген страдал сильнее. Этот зависимый от расстояния эффект соответствует наблюдениям у пациентов и согласуется с известным распространением транскрипционного репрессирования от мест двухцепочечных разрывов.
Что это означает для болезни и в более широком контексте
В совокупности работа выдвигает ясную модель: в здоровых клетках ATRX связывается с G‑богатым повтором рядом с генами альфа‑глобина во время транскрипции, помогая предотвращать или растворять G‑четверные спирали и R‑петли и таким образом защищая регион от повреждений ДНК. Когда ATRX отсутствует, эти необычные ДНК‑ и РНК‑структуры накапливаются на повторе, приводя к локальным разрывам ДНК, активации ответа на повреждение и к репрессивной хроматиновой среде, которая ослабляет экспрессию соседних генов в зависимости от расстояния, причём HBM страдает сильнее всего. Этот механизм объясняет, почему при синдроме ATR‑X возникает лишь лёгкая, участковая альфа‑талассемия, почему тяжесть зависит от длины повтора и почему мышиные модели, лишённые этого специфичного для человека повтора, не демонстрируют тот же дефект крови. В более широком смысле это указывает на то, что повторяющиеся G‑богатые последовательности, рассеянные по геному, могут выступать скрытыми разломами: если факторы защиты вроде ATRX дают сбой, они превращаются в «горячие точки» нестабильности, которые тихо перенастраивают активность генов в ходе развития, старения и при раке.
Цитирование: Shen, Y., Gupta, K., Tan-Wong, S.M. et al. ATRX loss couples genome instability at a G-rich repeat to dysregulation of human alpha-globin expression. Nat Commun 17, 2749 (2026). https://doi.org/10.1038/s41467-026-69169-7
Ключевые слова: ATRX, альфа‑глобин, повреждение ДНК, G‑четверная спираль, R‑петли