Clear Sky Science · es
Pérdida de ATRX vincula la inestabilidad genómica en un repetido rico en G con la desregulación de la expresión de alfa-globina humana
Por qué esto importa para la sangre y el cáncer
Nuestras células rojas dependen de un control muy fino de los genes que fabrican la hemoglobina, la proteína que transporta el oxígeno. Una proteína llamada ATRX se sitúa sobre el ADN y ayuda a mantenerlo estable; las mutaciones en ATRX provocan una forma hereditaria de anemia con discapacidad intelectual y son frecuentes en varios cánceres. Este estudio utiliza el clúster de genes de la alfa-globina como caso de estudio para mostrar, con detalle molecular, cómo la pérdida de ATRX puede dañar el ADN en un tramo repetitivo y silenciar discretamente genes cercanos. Entender esta cadena de eventos ayuda a explicar un trastorno humano raro y arroja luz sobre cómo la inestabilidad genómica puede alterar la actividad génica de forma más general.
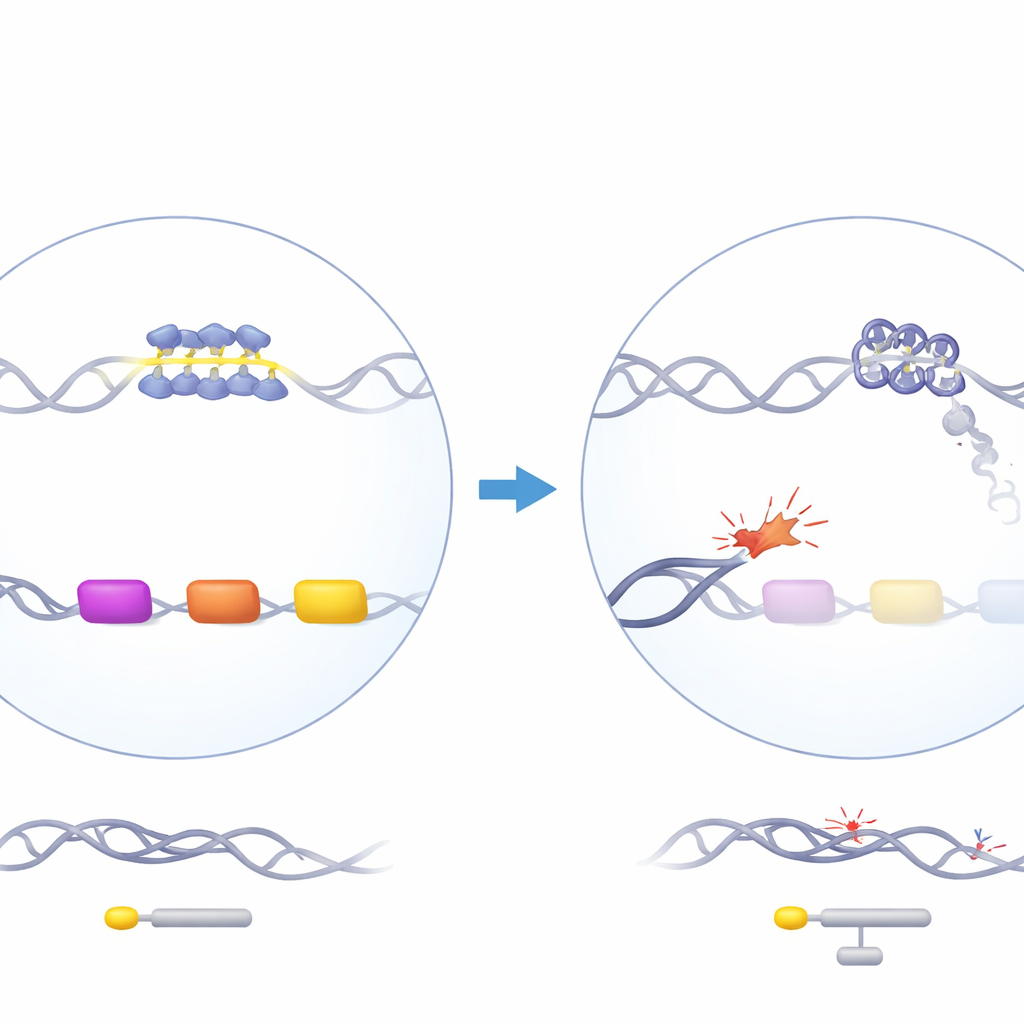
Una proteína guardiana con un efecto intrigante
ATRX es una proteína remodeladora de la cromatina que ayuda a organizar el ADN y participa en la replicación, la transcripción y la reparación del ADN. Cuando ATRX está mutado en humanos, los pacientes desarrollan el síndrome ATR-X, que incluye una alfa-talassemia leve: sus genes de alfa-globina, necesarios para construir la hemoglobina, están poco activos. De manera intrigante, la pérdida de ATRX afecta a la alfa-globina pero no a la beta-globina, aunque ambas son necesarias en cantidades iguales. Los genes de alfa-globina se ubican en una región rica en genes y en GC del cromosoma 16 que contiene varios elementos repetitivos de ADN, incluyendo un repetido de número variable de tandem (VNTR) particularmente rico en G situado justo río arriba de los genes tipo alfa. Trabajos genéticos anteriores mostraron que la longitud de este repetido se correlaciona con la magnitud de la reducción de la alfa-globina en pacientes, lo que sugiere que este tramo inusual de ADN podría ser central en el problema.
Acercándose a las células afectadas
Para investigar, los autores eliminaron ATRX en células madre y progenitoras sanguíneas humanas usando edición génica CRISPR y luego maduraron esas células hasta precursores de glóbulos rojos en cultivo. El análisis de la población celular en conjunto mostró solo una caída leve en un gen tipo alfa, HBM, y ningún cambio importante en otros genes de globina, reflejando los modestos cambios sanguíneos observados en pacientes. Sin embargo, al analizar colonias individuales y células únicas, emergió una imagen distinta. Solo un subconjunto de las células deficientes en ATRX mostró una fuerte reducción de HBM y, en menor medida, de los genes principales de alfa-globina. Esas mismas células presentaban firmas de una respuesta a daño en el ADN activada, incluyendo marcadores aumentados de ADN roto y una mayor modificación de una histona (H2A) relacionada con la reparación del daño y el silenciamiento de genes cercanos. Esto sugiere que la downregulación de la alfa-globina ocurre principalmente en las células donde la pérdida de ATRX ha permitido la acumulación local de daño en el ADN.
Un repetido rico en G como punto débil
El equipo se centró entonces en el VNTR rico en G incrustado en un pseudogén cercano llamado HBZP1. Usando una línea eritroide humana inmortalizada, rastrearon la unión de ATRX a lo largo de la región de la alfa-globina y hallaron que ATRX se recluta específicamente a este VNTR cuando el ADN circundante se está transcribiendo. Diseñaron un sistema en el que ATRX podía degradarse rápidamente y observaron que la pérdida de ATRX reducía la expresión de HBM, replicando de nuevo el fenotipo de la enfermedad. De forma llamativa, al eliminar el propio VNTR del genoma, la eliminación de ATRX dejó de reducir los niveles de HBM. Fármacos que estabilizan estructuras inusuales de cuatro hebras del ADN conocidas como G-cuádruplexes produjeron una caída similar en la expresión de HBM, pero solo cuando el VNTR estaba presente. Análisis a escala del genoma revelaron que muchos otros genes desregulados por la pérdida de ATRX también contienen elementos repetitivos ricos en GC, lo que apunta a una vulnerabilidad general en tales sitios.
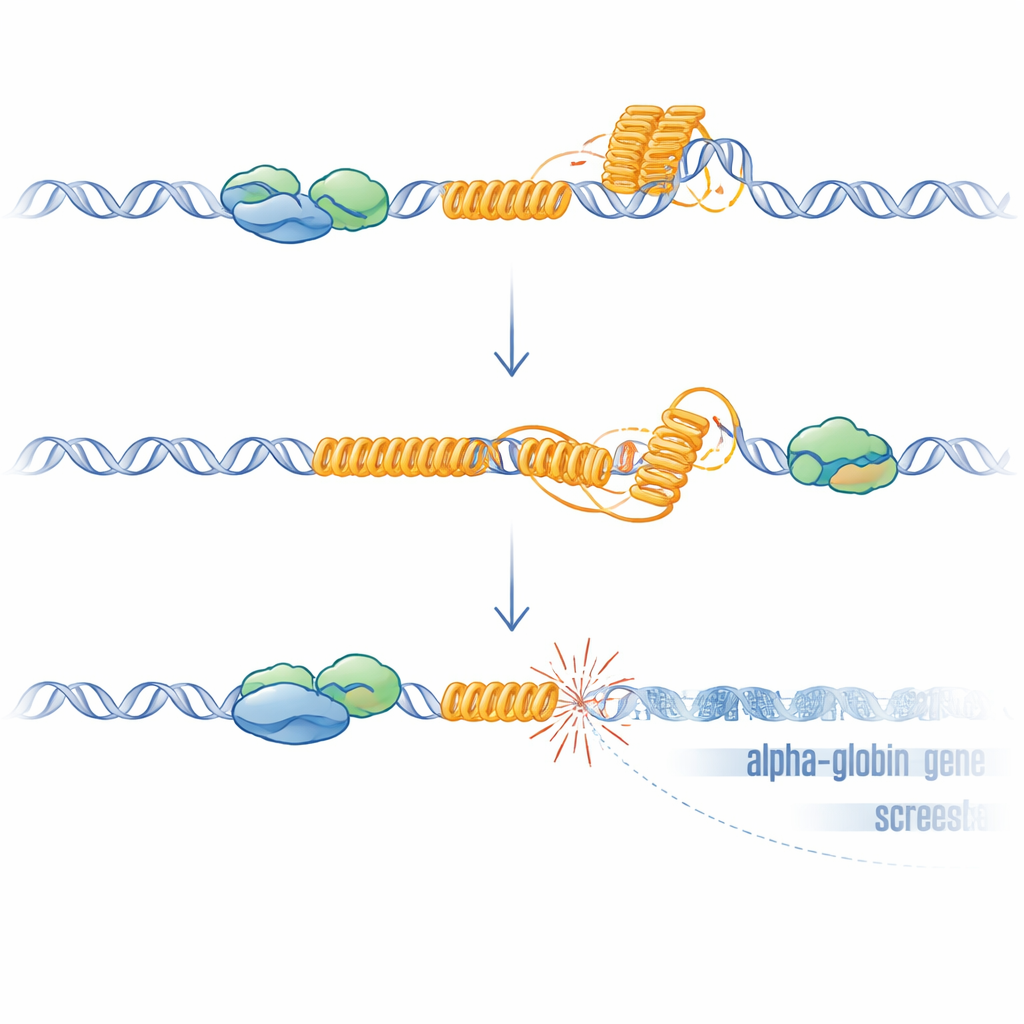
De formas extrañas del ADN a genes rotos
Los repetidos ricos en G como este VNTR pueden plegarse en G-cuádruplexes y favorecer la formación de R-loops, estructuras híbridas donde el ARN recién sintetizado queda adherido a la plantilla de ADN. Ambas estructuras pueden ralentizar o detener la maquinaria que copia y lee el ADN, provocando estrés y roturas. Los investigadores demostraron que, sin ATRX, los R-loops aumentaron en todo el genoma y se elevaron de forma particular en el VNTR. Cuando sobreexpresaron RNasa H, una enzima que elimina R-loops, la expresión de HBM se recuperó parcialmente, lo que respalda un papel causal de estas estructuras. Para probar si el daño en el ADN por sí solo era suficiente para silenciar los genes cercanos, usaron CRISPR para crear roturas dirigidas justo río arriba de HBM en células donde se había eliminado el VNTR. Estas roturas artificiales, incluso en ausencia del repetido, volvieron a reducir HBM y, de forma más débil, los genes de alfa-globina, afectando más al gen más cercano. Este efecto dependiente de la distancia coincide con lo observado en pacientes y es coherente con la propagación conocida de represión transcripcional a partir de sitios de roturas de doble hebra.
Qué implica esto para la enfermedad y más allá
En conjunto, el trabajo describe un modelo claro: en células sanas, ATRX se une a un repetido rico en G cerca de los genes de alfa-globina mientras se transcribe, ayudando a prevenir o disolver G-cuádruplexes y R-loops y protegiendo así la región del daño en el ADN. Cuando falta ATRX, estas estructuras inusuales de ADN y ARN se acumulan en el repetido, conduciendo a roturas locales del ADN, activación de la respuesta al daño y un entorno de cromatina represivo que atenúa la expresión de genes vecinos de forma dependiente de la distancia, con HBM siendo el más afectado. Este mecanismo explica por qué el síndrome ATR-X causa una alfa-talassemia leve y parcheada, por qué la gravedad varía con la longitud del repetido y por qué los modelos de ratón que carecen de este repetido específico humano no muestran el mismo defecto sanguíneo. Más en general, sugiere que las secuencias repetitivas ricas en G dispersas por nuestro genoma pueden actuar como fallas ocultas: si factores protectores como ATRX fallan, pueden convertirse en puntos calientes de inestabilidad que silenciosamente reconfiguran la actividad génica durante el desarrollo, el envejecimiento y el cáncer.
Cita: Shen, Y., Gupta, K., Tan-Wong, S.M. et al. ATRX loss couples genome instability at a G-rich repeat to dysregulation of human alpha-globin expression. Nat Commun 17, 2749 (2026). https://doi.org/10.1038/s41467-026-69169-7
Palabras clave: ATRX, alfa-globina, daño en el ADN, G-cuádruplex, R-loops