Clear Sky Science · sv
Samleverans av Programmed Death 1-ligander förbättrar och förlänger rAAV-medierad genuttryck i förimmuniserade möss
Göra genterapi effektivt för fler människor
Genterapier som använder ofarliga virus för att leverera hjälpsamma gener börjar förändra hur vi behandlar ärftliga sjukdomar. Men många människors immunsystem känner redan igen dessa virus, vilket kan göra att behandlingen avtar eller misslyckas. Denna studie undersöker ett sätt att "lugna" immunsvaret just där genterapin verkar, så att behandlingen kan bli mer bestående och hjälpa patienter som tidigare exponerats för dessa virus.
Varför immunsystemet bekämpar hjälpsamma virus
Genterapiverktygen i denna studie bygger på adenoassocierat virus (AAV), ett litet virus som ofta används för att skjutsa in nya gener i celler. AAV är generellt säkert och kan ge långvarig verkan, men det finns en hake: många människor har redan stött på naturligt förekommande AAV. Deras immunsystem minns virusets kapsel och kan snabbt angripa behandlade celler som visar upp delar av den, vilket avbryter genuttrycket. Detta är ett särskilt problem vid muskelbehandlingar, som ofta kräver höga doser och inte är naturligt skyddade mot immunangrepp. Nuvarande lösningar—som att utesluta patienter med redan befintliga antikroppar eller att ge bred immunosuppression—kan lämna patienter sårbara för infektioner och är inte idealiska långsiktiga strategier.
Låna en naturlig broms på immuniteten
Forskarna vände sig till en naturlig "broms" i immunsystemet kallad PD-1-vägen. I friska vävnader hjälper PD-1 och dess partners, PD-L1 och PD-L2, till att förhindra överaktiva immunsvar som kan skada kroppen själv. Tumörer utnyttjar ibland denna väg för att gömma sig från immunceller, men samma mekanism kan i princip användas för att skydda friska celler som modifierats med genterapi. Teamet designade AAV-vektorer som bär både en rapportörgen (ett ofarligt sekretoriskt enzym kallat muSEAP, som lätt kan mätas i blod) och antingen PD-L1 eller PD-L2, kopplade med ett kort självklippt peptid som gör att celler kan producera båda proteinerna separat från en enda genetisk kasset. De bekräftade först i cellkulturer att "två-i-ett"-designen fungerade: både den terapeutiska representanten och PD-1-liganderna producerades korrekt, var biologiskt aktiva och kunde binda PD-1.
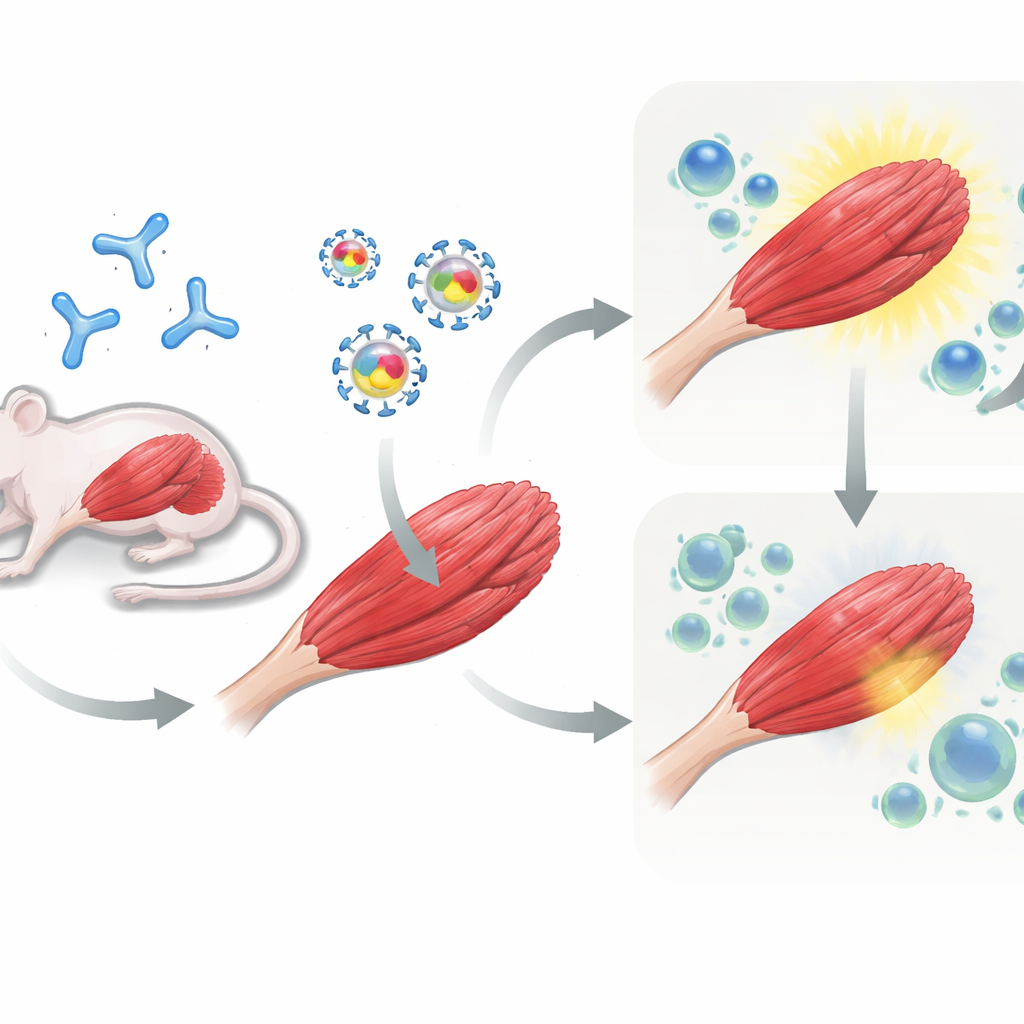
Testa strategin i förexponerade möss
Nästa steg förde teamet till möss. Vissa djur gavs först en dos AAV för att efterlikna patienter som redan bär på immunitet mot vektorn, medan andra förblev naiva. Alla möss fick sedan genterapi injicerad i benmuskulaturen: antingen AAV som bar muSEAP ensam, eller AAV som bar muSEAP plus PD-L1 eller PD-L2. Under flera veckor mätte forskarna muSEAP-nivåer i blodet som ett mått på hur väl den införda genen fungerade. I möss som förhandsimmuniserats mot AAV var samleverans av PD-L1 särskilt effektiv: muSEAP-nivåerna var mycket högre och förblev förhöjda upp till 12 veckor jämfört med kontrollvektorn. PD-L2 förbättrade också uttrycket, om än i mindre grad och med större variation. I kontrast gav tillsats av PD-L1 eller PD-L2 i naiva möss som aldrig tidigare mött AAV ingen bestående fördel och i vissa fall avtog eventuella tidiga vinster över tid.
Vad som händer inne i behandlad muskel
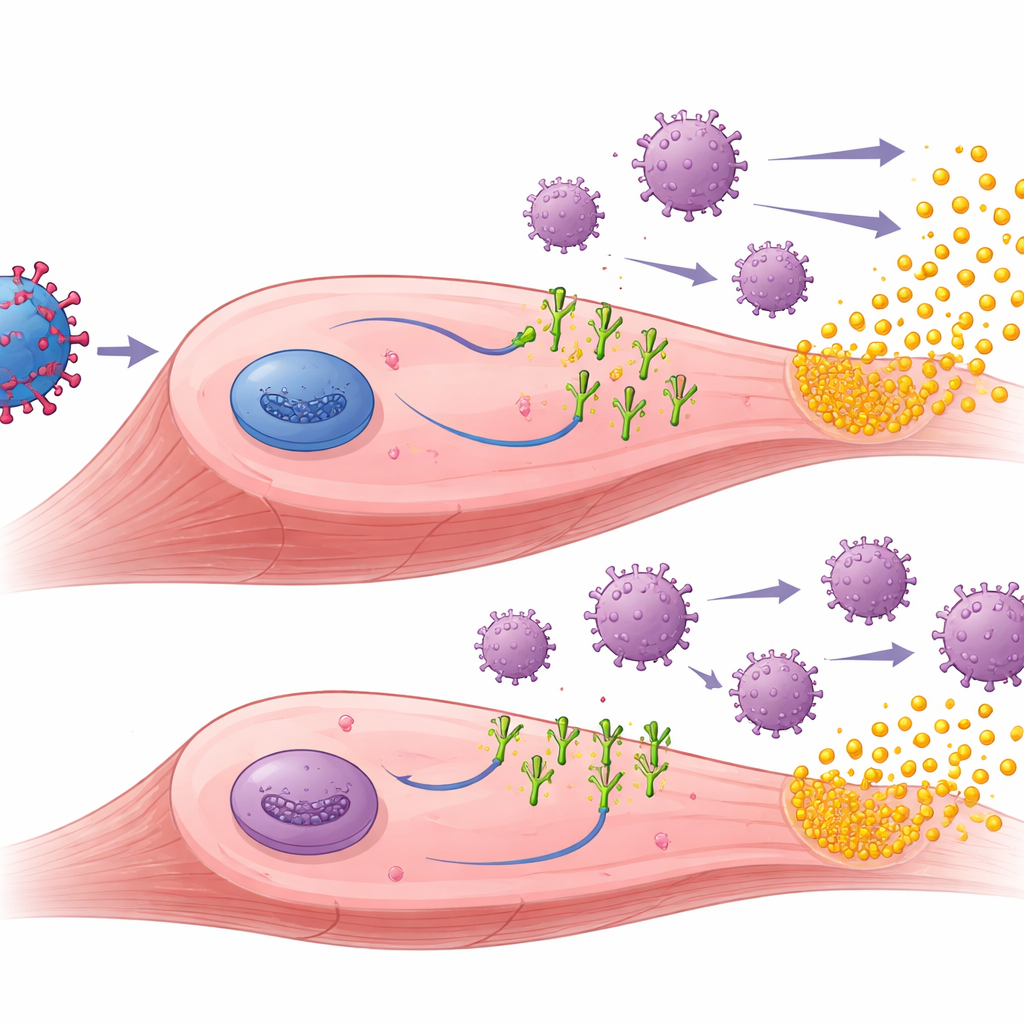
För att förstå varför PD-1-liganderna hjälpte undersökte forskarna de behandlade musklerna. De fann att genterapin framgångsrikt drev produktion av både muSEAP och PD-1-liganderna i muskelvävnad. I de förimmuniserade djuren visade muskler som fick PD-L1- eller PD-L2-vektorerna generellt färre invaderande T-celler och andra tecken på inflammation än muskler behandlade med muSEAP ensam. I dessa förexponerade möss gick högre muSEAP-nivåer ofta hand i hand med lägre antal immunceller, vilket tyder på att lokal immunnedsättning tillät de behandlade cellerna att överleva och fortsätta producera det terapeutiska proteinet längre. Teamet mätte också antikroppar mot AAV och mot de humana PD-1-liganderna själva. Som förväntat steg AAV-antikropparna efter förimmunisering och förblev höga, men PD-1-liganderna minskade inte dessa anti-vektorantikroppar. Intressant nog framkallade endast PD-L1 detekterbara anti-ligand-antikroppar, främst i naiva möss, vilket antyder subtila skillnader i hur främmande varje ligand uppfattas av immunsystemet.
Vad detta kan innebära för framtida behandlingar
Enkelt uttryckt visar denna studie att paketera en lokal immun"fredsmäklare" tillsammans med en terapeutisk gen kan hjälpa genterapi att fungera bättre hos individer vars immunsystem redan är uppmärt mot leveransviruset. Genom att samleverera PD-L1 eller PD-L2 direkt med transgenen i en enda AAV-vektor uppnådde författarna starkare och mer långvarigt genuttryck i förimmuniserade möss, samtidigt som färre immunceller attackerade den behandlade muskeln. Även om många frågor kvarstår—som hur man bäst väger nytta mot potentiella risker med att dämpa immunitet, och hur dessa fynd kommer att översättas till människor—pekar arbetet mot en strategi som skulle kunna öppna genterapi för en bredare patientgrupp som annars kan bli utesluten på grund av tidigare exponering för AAV.
Citering: Käyhty, P., Nieminen, T., Eriksson, R.A.E. et al. The co-delivery of Programmed Death 1 ligands enhances and prolongs rAAV-mediated gene expression in pre-immunized mice. Gene Ther 33, 127–137 (2026). https://doi.org/10.1038/s41434-025-00588-9
Nyckelord: genterapi, AAV-vektorer, immunologisk tolerans, PD-1 kontrollpunkt, skelettmuskulatur