Clear Sky Science · de
Die Kofraktion von Programmed Death‑1‑Liganden verstärkt und verlängert rAAV‑vermittelte Genexpression in vorimmunisierten Mäusen
Gentherapie für mehr Menschen wirksam machen
Gentherapien, die harmlose Viren nutzen, um nützliche Gene zu liefern, beginnen, die Behandlung erblicher Erkrankungen zu verändern. Doch die Immunsysteme vieler Menschen erkennen diese Viren bereits, was dazu führen kann, dass die Therapie nachlässt oder versagt. In dieser Studie wird ein Ansatz untersucht, um die Immunantwort direkt dort zu „beruhigen“, wo die Gentherapie wirkt, damit die Behandlung länger anhält und auch Patienten hilft, die zuvor mit diesen Viren in Kontakt gekommen sind.
Warum das Immunsystem nützliche Viren bekämpft
Die in dieser Studie verwendeten Gentherapie‑Werkzeuge basieren auf dem adeno‑assoziierten Virus (AAV), einem winzigen Virus, das häufig genutzt wird, um neue Gene in Zellen zu schleusen. AAV ist im Allgemeinen sicher und kann über Jahre wirken, doch es gibt einen Haken: Viele Menschen haben in der Natur bereits Kontakt mit AAV gehabt. Ihr Immunsystem erinnert sich an die Virushülle und kann behandelte Zellen, die Teile dieser Hülle präsentieren, schnell angreifen und so die Genexpression unterbrechen. Dies ist besonders bei Muskelbehandlungen problematisch, die oft hohe Dosen erfordern und nicht natürlich vor Immunangriffen geschützt sind. Aktuelle Umgehungsstrategien — wie der Ausschluss von Patienten mit vorbestehenden Antikörpern oder die Gabe breit wirkender Immunsuppressiva — können Patienten gegenüber Infektionen ungeschützt lassen und sind auf lange Sicht keine ideale Lösung.
Sich einer natürlichen Bremse der Immunreaktion bedienen
Die Forschenden griffen auf eine natürliche „Bremse“ des Immunsystems zurück, den PD‑1‑Signalweg. In gesundem Gewebe helfen PD‑1 und seine Partner PD‑L1 und PD‑L2, übermäßige Immunangriffe zu verhindern, die dem Körper selbst schaden könnten. Tumoren nutzen diesen Mechanismus gelegentlich, um sich vor Immunzellen zu verbergen, aber derselbe Mechanismus kann prinzipiell dazu verwendet werden, gesunde, durch Gentherapie veränderte Zellen zu schützen. Das Team entwarf AAV‑Vektoren, die sowohl ein Reportergen (ein harmloses, sekretiertes Enzym namens muSEAP, das leicht im Blut gemessen werden kann) als auch entweder PD‑L1 oder PD‑L2 tragen, verbunden durch ein kurzes selbstspaltendes Peptid, das es den Zellen ermöglicht, beide Proteine getrennt aus einer einzigen Gensequenz herzustellen. Zunächst bestätigten sie in Zellkulturen, dass das „Zwei‑in‑Einem“‑Design funktionierte: Sowohl der therapeutische Stellvertreter als auch die PD‑1‑Liganden wurden korrekt produziert, waren biologisch aktiv und konnten an PD‑1 binden.
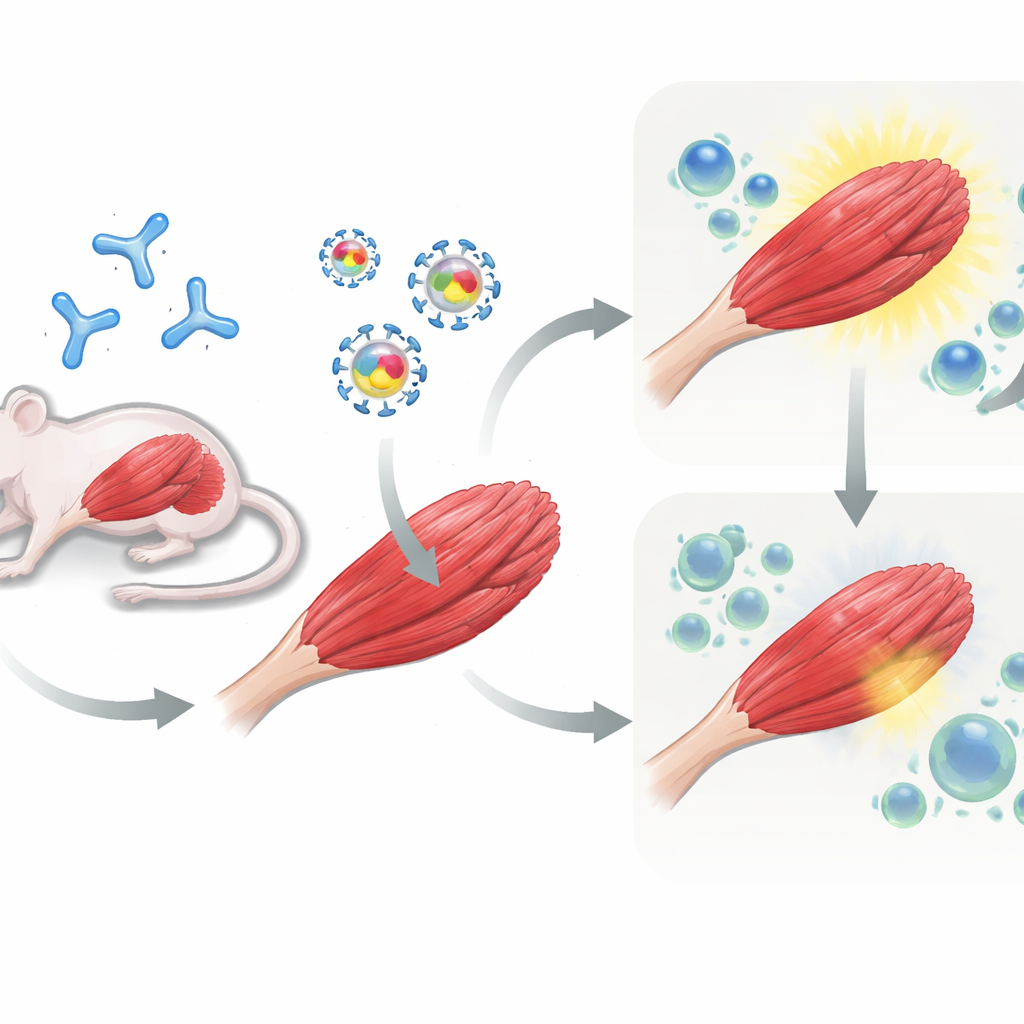
Test des Ansatzes in vorexponierten Mäusen
Als Nächstes gingen die Forschenden an Mäuse. Einige Tiere erhielten zunächst eine AAV‑Dosis, um Patienten zu simulieren, die bereits Immunität gegen den Vektor besitzen, während andere naiv blieben. Alle Mäuse bekamen danach die Gentherapie in die Beinmuskulatur injiziert: entweder AAV mit muSEAP allein oder AAV mit muSEAP plus PD‑L1 bzw. PD‑L2. Über mehrere Wochen maßen die Forschenden muSEAP‑Spiegel im Blut als Indikator dafür, wie gut das eingebrachte Gen funktionierte. Bei Mäusen, die gegen AAV vorimmunisiert waren, war die Kofraktion mit PD‑L1 besonders effektiv: Die muSEAP‑Werte waren deutlich höher und blieben im Vergleich zum Kontrollvektor bis zu 12 Wochen erhöht. PD‑L2 verbesserte die Expression ebenfalls, wenn auch in geringerem und variablerem Umfang. Im Gegensatz dazu brachte das Hinzufügen von PD‑L1 oder PD‑L2 bei naiven Mäusen, die AAV nie zuvor gesehen hatten, keinen anhaltenden Vorteil; in einigen Fällen schwanden frühe Zugewinne mit der Zeit.
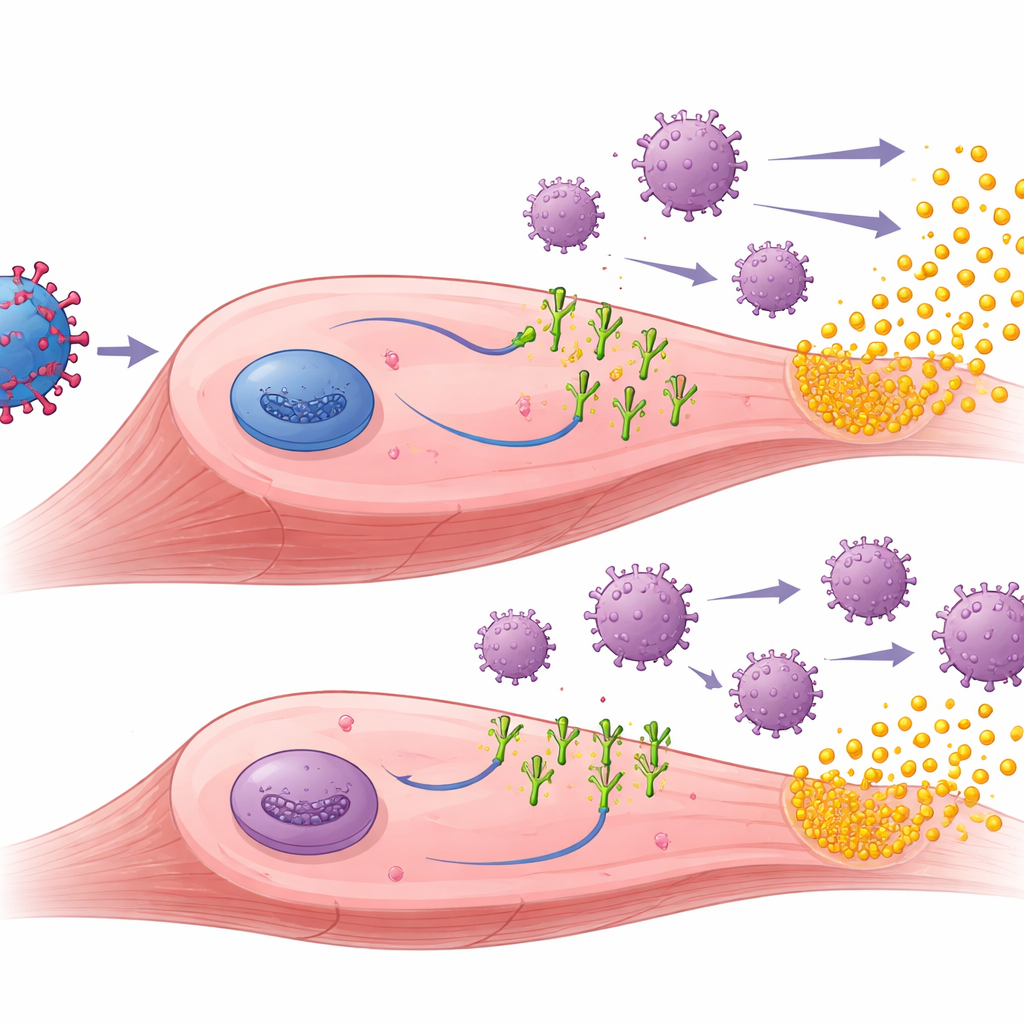
Was im behandelten Muskel geschieht
Um zu verstehen, warum die PD‑1‑Liganden halfen, untersuchten die Forschenden die behandelten Muskeln. Sie fanden heraus, dass die Gentherapie sowohl muSEAP als auch die PD‑1‑Liganden erfolgreich im Muskelgewebe produzierte. In den vorimmunisierten Tieren zeigten Muskeln, die PD‑L1‑ oder PD‑L2‑Vektoren erhielten, im Allgemeinen weniger eindringende T‑Zellen und geringere Entzündungszeichen als Muskeln, die nur muSEAP erhalten hatten. Bei diesen vorexponierten Mäusen gingen höhere muSEAP‑Spiegel häufig mit niedrigeren Zahlen an Immunzellen einher, was darauf hindeutet, dass die lokale Dämpfung der Immunantwort den behandelten Zellen erlaubte, zu überleben und länger das therapeutische Protein zu produzieren. Das Team maß außerdem Antikörper gegen AAV und gegen die menschlichen PD‑1‑Liganden selbst. Wie erwartet stiegen die AAV‑Antikörper nach der Vorimmunisierung und blieben hoch, doch die PD‑1‑Liganden reduzierten diese Anti‑Vektor‑Antikörper nicht. Interessanterweise löste nur PD‑L1 nachweisbare Anti‑Liganden‑Antikörper aus, und zwar hauptsächlich bei naiven Mäusen, was auf subtile Unterschiede hindeutet, wie fremd jeder Ligand für das Immunsystem erscheint.
Was das für künftige Behandlungen bedeuten könnte
Vereinfacht gesagt zeigt diese Studie, dass das Verpacken eines lokalen immunologischen „Friedenswächters“ zusammen mit einem therapeutischen Gen die Wirksamkeit von Gentherapien bei Patienten verbessern kann, deren Immunsystem bereits gegen das Transportvirus sensibilisiert ist. Durch die Kofraktion von PD‑L1 oder PD‑L2 direkt mit dem Transgen in einem einzigen AAV‑Vektor erzielten die Autorinnen und Autoren stärkere und länger anhaltende Genexpression in vorimmunisierten Mäusen und beobachteten zugleich weniger Immunzellangriffe auf den behandelten Muskel. Obwohl viele Fragen offenbleiben — etwa wie Nutzen und potenzielle Risiken der Immunsuppression am besten austariert werden und wie sich die Befunde auf den Menschen übertragen lassen — deutet die Arbeit auf eine Strategie hin, die Gentherapie für eine breitere Patientengruppe öffnen könnte, die andernfalls aufgrund früherer AAV‑Exposition ausgeschlossen wäre.
Zitation: Käyhty, P., Nieminen, T., Eriksson, R.A.E. et al. The co-delivery of Programmed Death 1 ligands enhances and prolongs rAAV-mediated gene expression in pre-immunized mice. Gene Ther 33, 127–137 (2026). https://doi.org/10.1038/s41434-025-00588-9
Schlüsselwörter: Gentherapie, AAV‑Vektoren, Immunologische Toleranz, PD‑1‑Checkpoint, Skelettmuskulatur