Clear Sky Science · ru
Совместная доставка лигандов программируемой смерти 1 усиливает и продлевает экспрессию генов, медиируемую rAAV, у предварительно иммунизированных мышей
Как сделать генную терапию доступной для большего числа людей
Генные терапии с использованием безвредных вирусов для доставки полезных генов начинают менять подход к лечению наследственных заболеваний. Но у многих людей иммунная система уже узнает эти вирусы, что может привести к ослаблению или неудаче лечения. В этом исследовании изучают способ «успокоить» иммунный ответ там, где действует генная терапия, чтобы лечение сохранялось дольше и помогало пациентам, ранее контактировавшим с этими вирусами.
Почему иммунная система атакует полезные вирусы
Инструменты генной терапии в этом исследовании основаны на аденоассоциированном вирусе (AAV) — крошечном вирусе, часто используемом для доставки новых генов в клетки. AAV обычно безопасен и может функционировать годами, но есть один нюанс: многие люди уже встречались с природным AAV. Их иммунная система запоминает капсид вируса и может быстро атаковать обработанные клетки, которые демонстрируют фрагменты этого капсида, что прекращает экспрессию введённого гена. Это особенно важно для терапий мышц, которые часто требуют высоких доз и не защищены естественным образом от иммунной атаки. Текущие обходные решения — например, исключение пациентов с предсуществующими антителами или назначение широкого иммунодепрессантного лечения — оставляют пациентов без защиты от инфекций и не являются идеальным долгосрочным решением.
Заимствование природного тормоза иммунитета
Исследователи обратились к природному «тормозу» иммунной системы, известному как путь PD-1. В здоровых тканях PD-1 и его партнёры, PD-L1 и PD-L2, помогают предотвратить чрезмерные иммунные атаки, которые могли бы повредить собственные клетки организма. Опухоли иногда используют этот путь, чтобы скрываться от иммунных клеток, но тот же механизм, в принципе, можно использовать для защиты здоровых клеток, модифицированных генной терапией. Команда разработала векторы AAV, несущие как отчетный ген (безвредный секретируемый фермент muSEAP, который легко измерить в крови), так и PD-L1 или PD-L2, связанные коротким саморазрезающимся пептидом, позволяющим клеткам продуцировать оба белка отдельно из одной генетической кассеты. Сначала они подтвердили в культурах клеток, что «два в одном» работают: и терапевтический маркер, и лиганды PD-1 правильно образуются, биологически активны и способны связываться с PD-1.
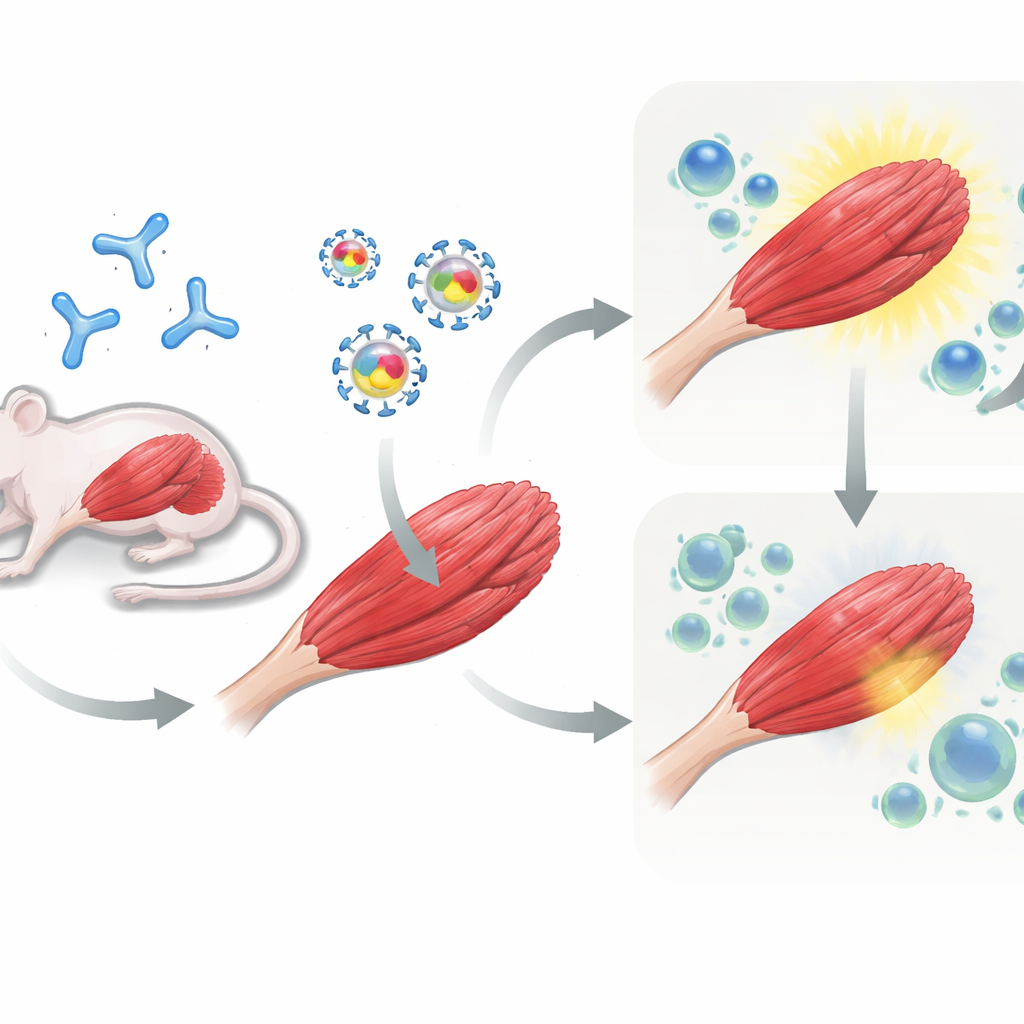
Испытание стратегии на предварительно экспонированных мышах
Далее команда перешла к опытам на мышах. Часть животных сначала получила дозу AAV, чтобы смоделировать пациентов с уже сформированным иммунитетом к вектору, а остальные оставались наивными. Всем мышам затем ввели генную терапию в мышцы ноги: либо AAV, несущий только muSEAP, либо AAV с muSEAP вместе с PD-L1 или PD-L2. В течение нескольких недель исследователи измеряли уровни muSEAP в крови как показатель активности введённого гена. У мышей, предварительно иммунизированных против AAV, сопутствующая доставка PD-L1 оказалась особенно эффективной: уровни muSEAP были значительно выше и оставались повышенными до 12 недель по сравнению с контрольным вектором. PD-L2 также улучшала экспрессию, хотя в меньшей и более изменчивой степени. Напротив, у наивных мышей, никогда ранее не встречавшихся с AAV, добавление PD-L1 или PD-L2 не давало длительного преимущества и в некоторых случаях любое раннее повышение со временем исчезало.
Что происходит внутри обработанной мышцы
Чтобы понять, почему лиганды PD-1 помогали, исследователи изучили обработанные мышцы. Они обнаружили, что генная терапия успешно индуцировала продукцию и muSEAP, и лигандов PD-1 в мышечной ткани. У предварительно иммунизированных животных мышцы, получившие векторы с PD-L1 или PD-L2, как правило, показывали меньше вторгшихся Т-клеток и других признаков воспаления по сравнению с мышцами, обработанными только muSEAP. У этих предварительно экспонированных мышей более высокие уровни muSEAP обычно коррелировали с меньшим количеством иммунных клеток, что указывает на то, что локальное подавление иммунитета позволило обработанным клеткам выжить и дольше синтезировать терапевтический белок. Команда также измерила антитела против AAV и против самих человеческих лигандов PD-1. Как и ожидалось, антитела к AAV повышались после предварительной иммунизации и оставались высокими, но лиганды PD-1 не снижали эти антитела к вектору. Интересно, что только PD-L1 вызывал обнаруживаемые антитела против лиганда, и в основном у наивных мышей, что намекает на тонкие различия в том, насколько чужеродным каждый лиганд воспринимается иммунной системой.
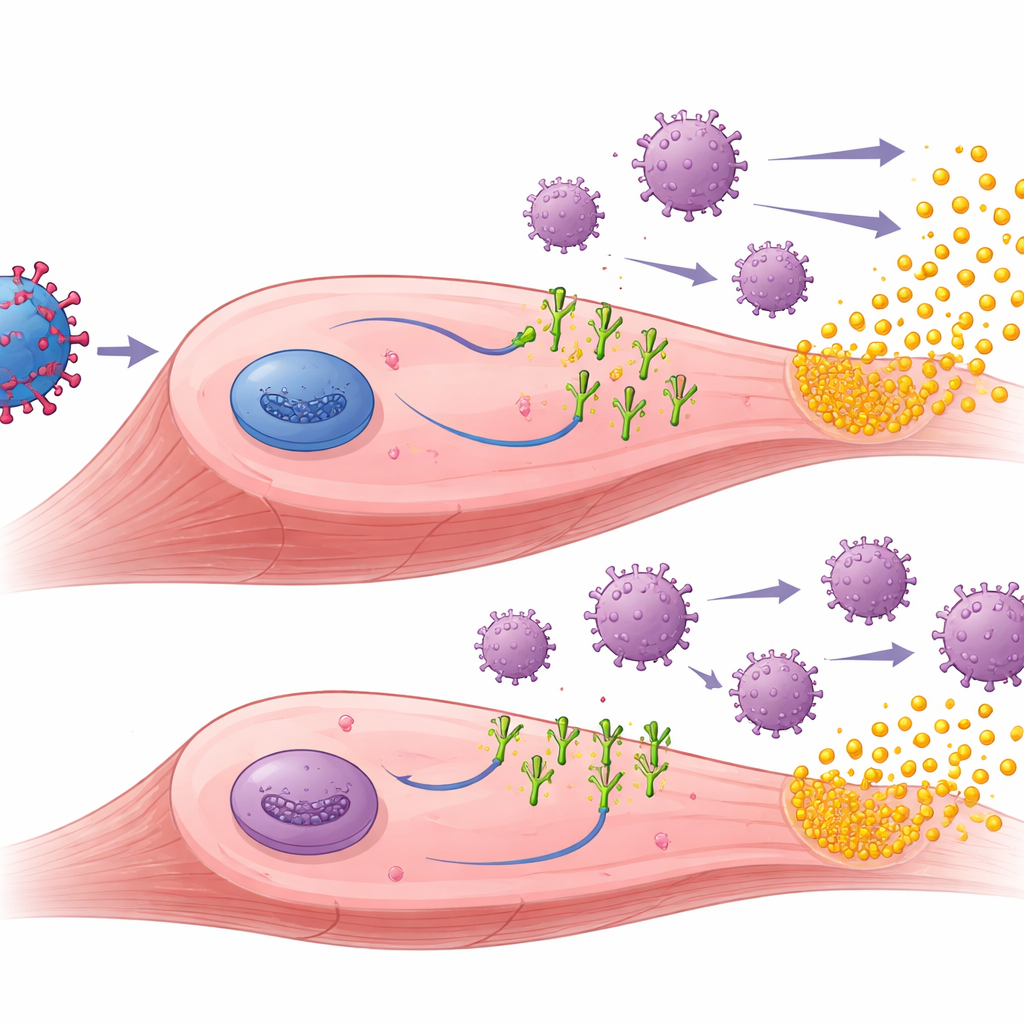
Что это может значить для будущих терапий
Проще говоря, это исследование показывает, что упаковка локального иммунного «миротворца» вместе с терапевтическим геном может помочь генной терапии работать лучше у субъектов, чья иммунная система уже подготовлена против векторного вируса. При совместной доставке PD-L1 или PD-L2 прямо с трансгеном в одном векторе AAV авторы добились более сильной и продолжительной экспрессии гена у предварительно иммунизированных мышей, одновременно наблюдая меньше атак иммунных клеток на обработанную мышцу. Хотя остаётся много вопросов — например, как лучше сбалансировать пользу и потенциальные риски подавления иммунитета и как эти результаты перенесутся на людей — работа указывает на стратегию, которая могла бы расширить круг пациентов, доступных для генной терапии, и которые в противном случае могли бы быть исключены из-за предыдущего контакта с AAV.
Цитирование: Käyhty, P., Nieminen, T., Eriksson, R.A.E. et al. The co-delivery of Programmed Death 1 ligands enhances and prolongs rAAV-mediated gene expression in pre-immunized mice. Gene Ther 33, 127–137 (2026). https://doi.org/10.1038/s41434-025-00588-9
Ключевые слова: генная терапия, векторы AAV, иммунная толерантность, контрольный пункт PD-1, скелетная мышца