Clear Sky Science · ar
التوصيل المشترك لريباطات الموت المبرمج 1 يعزز ويطيل التعبير الجيني المتوسط rAAV في الفئران المكشوفة مسبقًا للمناعة
جعل العلاج الجيني فعالاً لشريحة أوسع من الناس
العلاجات الجينية التي تستخدم فيروسات غير ضارة لإيصال جينات مفيدة بدأت تُغيّر طريقة علاج الأمراض الوراثية. لكن جهاز المناعة لدى كثيرين يتعرف بالفعل على هذه الفيروسات، مما قد يؤدي إلى تلاشي العلاج أو فشله. تستكشف هذه الدراسة وسيلة لـ "تهدئة" الاستجابة المناعية في المكان نفسه الذي يعمل فيه العلاج الجيني، بحيث يمكن أن يستمر تأثير العلاج لفترة أطول ويستفيد منه المرضى الذين تعرّضوا لهذه الفيروسات سابقًا.
لماذا يقاوم جهاز المناعة فيروسات مفيدة
أدوات العلاج الجيني في هذه الدراسة مبنية على فيروس مترافق مع الأدينو (AAV)، وهو فيروس صغير يُستخدم على نطاق واسع لنقل جينات جديدة إلى الخلايا. AAV آمن عمومًا ويمكن أن يبقى فعالًا لسنوات، لكن هناك مشكلة: كثير من الناس سبق أن تعرضوا لـ AAV الطبيعي في البيئة. يتذكر جهاز المناعة الغلاف الفيروسي ويمكنه بسرعة مهاجمة الخلايا المعالجة التي تعرض أجزاء من هذا الغلاف، ما يقطع التعبير الجيني. هذا يُعدّ مصدر قلق خاص لعلاجات العضلات، التي غالبًا ما تتطلب جرعات عالية وليست محمية طبيعيًا من هجوم المناعة. الحلول الحالية—مثل استبعاد المرضى ذوي الأجسام المضادة المسبقة أو إعطاء عقاقير مهيمنة لتثبيط المناعة—قد تترك المرضى عرضة للعدوى وليست حلولًا مثالية على المدى الطويل.
الاستعانة بمكبح طبيعي للمناعة
اتجه الباحثون إلى "مكبح" طبيعي في جهاز المناعة يُعرف بمسار PD-1. في الأنسجة الصحية، يساعد PD-1 وشريكاها PD-L1 وPD-L2 على منع هجمات مناعية مفرطة قد تضر بالجسم نفسه. تستغل بعض الأورام أحيانًا هذا المسار للاختباء من الخلايا المناعية، لكن يمكن، من حيث المبدأ، استخدام الآلية نفسها لحماية الخلايا الصحية المعدلة بواسطة العلاج الجيني. صمّم الفريق نواقل AAV تحمل كلًا من جين مؤشرات (إنزيم سري مُفرَز غير مؤذٍ يُدعى muSEAP يمكن قياسه بسهولة في الدم) وأحد ربطيّ PD-L1 أو PD-L2، مرتبطان بواسطة ببتيد قصير يفصل ذاتيًا يسمح للخلايا بإنتاج البروتينين بشكل منفصل من كاسيت جيني واحد. أكدوا أولًا في مزروعات خلوية أن تصميم "اثنان في واحد" يعمل: فقد تم إنتاج كلٍ من العنصر التعويضي العلاجي ورباطي PD-1 بشكل سليم، وكانا نشيطين بيولوجيًا وقادرين على الارتباط بـ PD-1.
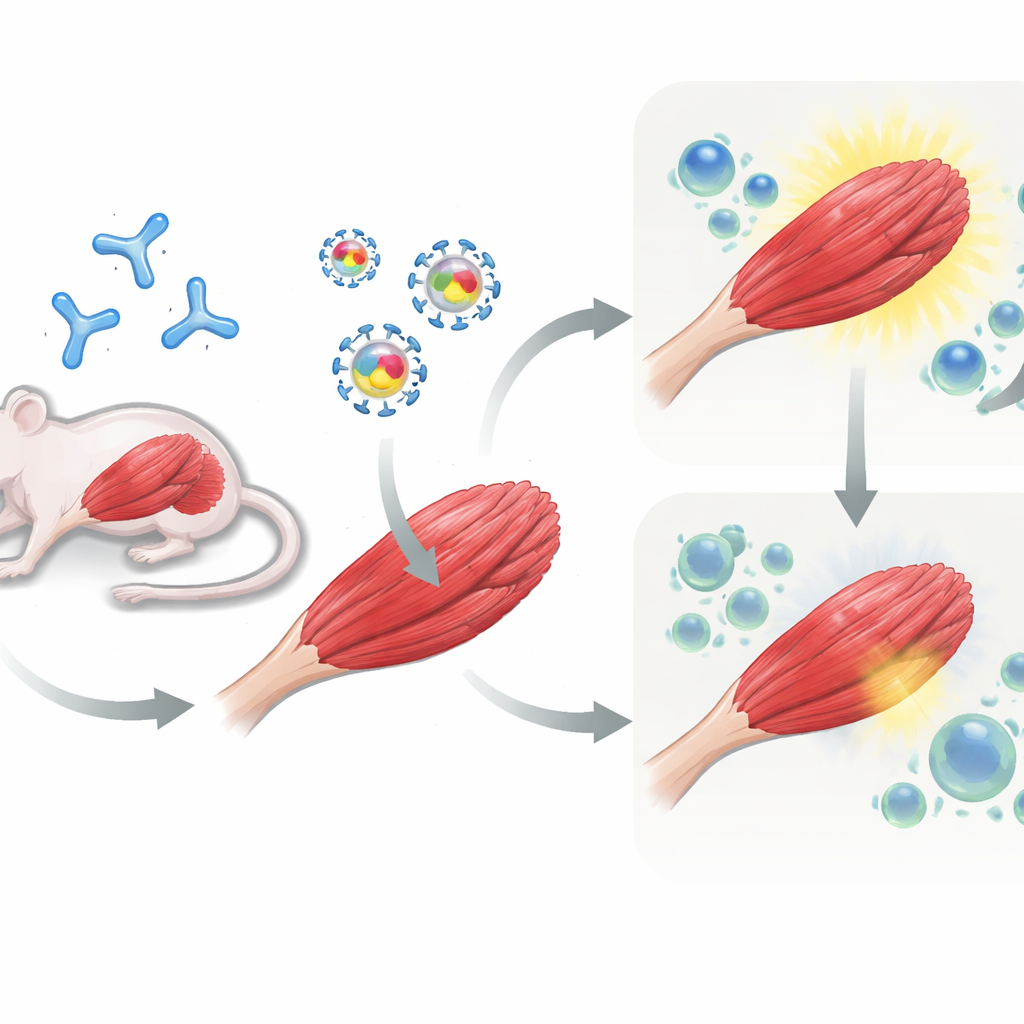
اختبار الاستراتيجية في فئران معرضة مسبقًا
بعد ذلك، انتقل الفريق إلى التجارب في الفئران. أُعطيت بعض الحيوانات جرعة AAV أولية لمحاكاة المرضى الذين لديهم مناعة سابقة ضد الناقل، بينما بقيت أخرى ساذجة. ثم تلقت جميع الفئران العلاج الجيني المحقون في عضلات الساق: إما AAV يحمل muSEAP فقط، أو AAV يحمل muSEAP مع PD-L1 أو PD-L2. على مدار عدة أسابيع، قاس الباحثون مستويات muSEAP في الدم كمؤشر على كفاءة الجين المُدخل. في الفئران التي كانت مُسبَقًا مُناعَة ضد AAV، كان التوصيل المشترك لـ PD-L1 ذا تأثير كبير: كانت مستويات muSEAP أعلى بكثير وبقيت مرتفعة لمدة تصل إلى 12 أسبوعًا مقارنة بالناقلة الضابطة. كما حسّن PD-L2 التعبير أيضًا، وإن بدرجة أقل وأكثر تفاوتًا. بالمقابل، في الفئران الساذجة التي لم تسبق رؤيتها لـ AAV، لم يمنح إرفاق PD-L1 أو PD-L2 ميزة دائمة، وفي بعض الحالات تلاشت أي مكاسب مبكرة مع مرور الوقت.
ما الذي يحدث داخل العضلة المعالجة
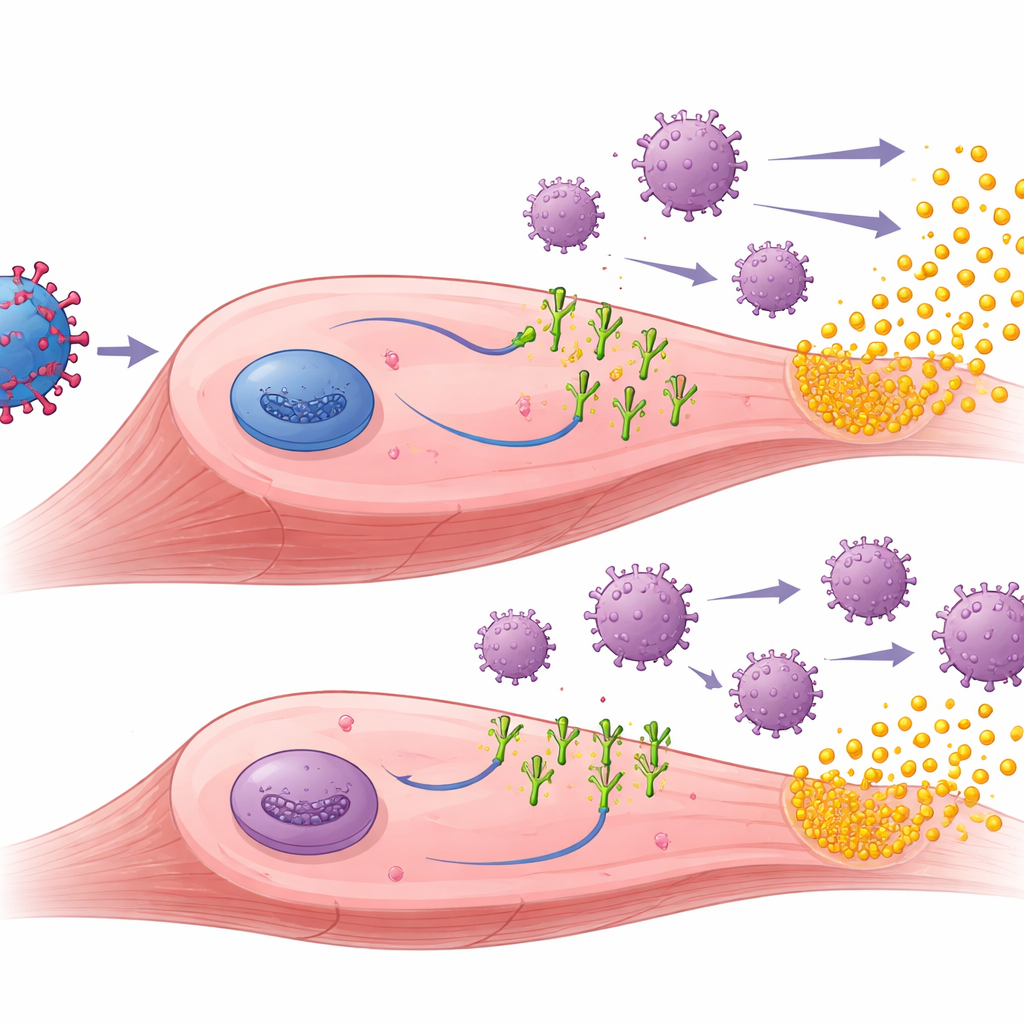
لفهم سبب استفادة الرابِطات PD-1، فحص الباحثون العضلات المعالجة. وجدوا أن العلاج الجيني دفع بنجاح إنتاج كلٍ من muSEAP ورباطي PD-1 في نسيج العضلات. في الحيوانات المعرضة مسبقًا للمناعة، أظهرت العضلات التي تلقت ناقلات PD-L1 أو PD-L2 عموماً خلايا T مُهاجمة أقل وعلامات التهاب أقل مقارنةً بالعضلات المعالجة بـ muSEAP وحده. في هذه الفئران المعرضة سابقًا، ارتبطت المستويات الأعلى من muSEAP غالبًا بانخفاض أعداد الخلايا المناعية، ما يوحي بأن التهدئة المناعية الموضعية سمحت للخلايا المعالجة بالبقاء والاستمرار في إنتاج البروتين العلاجي لفترة أطول. كما قاس الفريق الأجسام المضادة ضد AAV وضد روابط PD-1 البشرية نفسها. كما كان متوقعًا، ارتفعت أجسام AAV المضادة بعد التعرض المسبق وبقيت مرتفعة، لكن روابط PD-1 لم تقلل هذه الأجسام المضادة المضادة للناقلة. ومن المثير للاهتمام أن PD-L1 فقط هو الذي أثار تكوّن أجسام مضادة قابلة للكشف ضد الرابط، وخصوصًا في الفئران الساذجة، مما يلمح إلى فروق دقيقة في مدى غريبة كل رابط أمام جهاز المناعة.
ما الذي قد يعنيه هذا للعلاجات المستقبلية
بعبارات بسيطة، تُظهر هذه الدراسة أن تعبئة "حاجب" مناعي موضعي جنبًا إلى جنب مع جين علاجي يمكن أن تساعد العلاج الجيني على العمل بشكل أفضل في الأفراد الذين جهاز مناعهم مُهيأ بالفعل ضد فيروس الإيصال. من خلال التوصيل المشترك لـ PD-L1 أو PD-L2 مباشرة مع النسخة الجينية في ناقل AAV واحد، حقق المؤلفون تعبيرًا جينيًا أقوى وأكثر دوامًا في الفئران المعرضة مسبقًا، مع رؤية أيضًا خلايا مناعية أقل تهاجم العضلة المعالجة. وبالرغم من بقاء العديد من الأسئلة—مثل كيفية موازنة الفوائد مع المخاطر المحتملة لتثبيط المناعة، وكيفية ترجمة هذه النتائج إلى البشر—تشير النتائج إلى استراتيجية قد تفتح العلاج الجيني لشريحة أوسع من المرضى الذين قد يُستبعدون بخلاف ذلك بسبب تعرضهم السابق لـ AAV.
الاستشهاد: Käyhty, P., Nieminen, T., Eriksson, R.A.E. et al. The co-delivery of Programmed Death 1 ligands enhances and prolongs rAAV-mediated gene expression in pre-immunized mice. Gene Ther 33, 127–137 (2026). https://doi.org/10.1038/s41434-025-00588-9
الكلمات المفتاحية: العلاج الجيني, نواقل AAV, تسامح مناعي, نقطة تفتيش PD-1, العضلات الهيكلية