Clear Sky Science · ja
Programmed Death 1 リガンドの同時デリバリーは、免疫既往のあるマウスにおけるrAAV媒介遺伝子発現を増強し持続させる
より多くの人に遺伝子治療を効かせるために
無害なウイルスを用いて有益な遺伝子を届ける遺伝子治療は、遺伝性疾患の治療法を変えつつあります。しかし、多くの人の免疫系は既にこれらのウイルスを認識しており、その結果として治療効果が消失したり失敗したりすることがあります。本研究は、遺伝子治療が作用する局所で免疫反応を「鎮める」方法を検討し、治療効果を長く持続させ、過去にこれらのウイルスに曝露した患者にも効果を及ぼせる可能性を探ります。
なぜ免疫系は有用なウイルスに反応するのか
本研究で用いられる遺伝子治療ツールは、アデノ随伴ウイルス(AAV)に基づいています。AAVは新しい遺伝子を細胞に運ぶために広く用いられる小さなウイルスで、通常は安全であり数年間作用し続けることができます。しかし問題があります。多くの人が自然環境でAAVに既に出会っており、免疫系がウイルスの殻を記憶しているため、治療後にその殻の断片を提示する細胞を迅速に攻撃し、遺伝子発現を止めてしまうのです。これは、高用量が必要になりがちで免疫攻撃から自然に守られない筋肉治療で特に問題となります。現在の対処法(既存の抗体を持つ患者を除外する、あるいは広範な免疫抑制薬を投与するなど)は、感染に対する防御を弱めたり、長期的な解決策として理想的でなかったりします。
自然の免疫ブレーキを借りる
研究者たちはPD-1 経路と呼ばれる自然の免疫ブレーキに着目しました。健康な組織では、PD-1 とそのパートナーである PD-L1、PD-L2 が過剰な免疫攻撃を防ぎ、自己組織の損傷を抑えています。腫瘍はしばしばこの経路を利用して免疫細胞から隠れますが、同じ仕組みは遺伝子治療で改変された健常細胞を保護するためにも原理上利用できます。研究チームは、レポーター遺伝子(血中で簡便に測定できる無害な分泌酵素である muSEAP)と、PD-L1 または PD-L2 を同一の AAV カセットに短い自己切断ペプチドで連結して同時に運ぶベクターを設計しました。この設計により、単一の遺伝子カセットから両方のタンパク質が別々に産生されます。まず培養細胞で「二者同時」デザインが機能することを確認しました:治療代替物とPD-1リガンドの両方が適切に産生され、生物学的に活性をもち、PD-1 に結合できました。
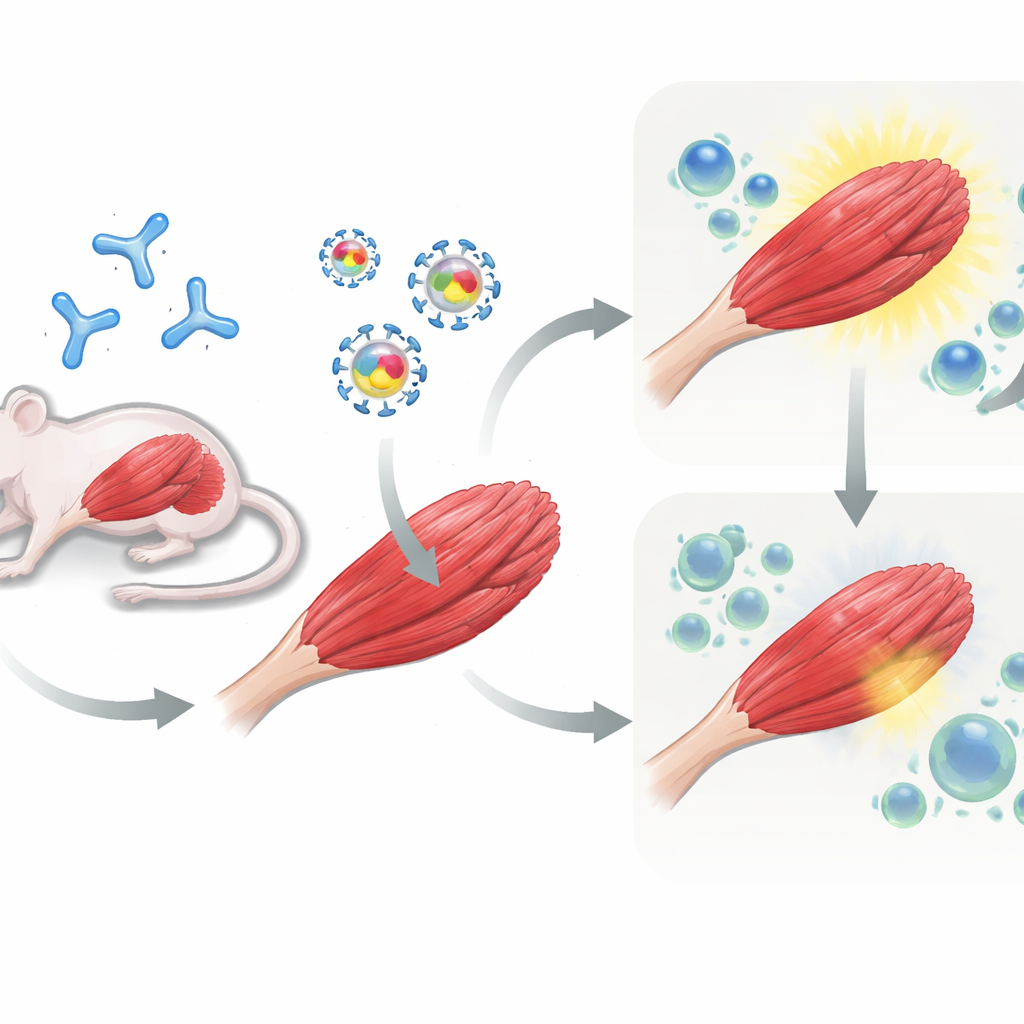
既往曝露マウスで戦略を検証する
次にチームはマウスで試験を行いました。まず一部の動物にAAVを投与して、ベクターに対する既往免疫を模倣し、他方はナイーブなままにしました。すべてのマウスにその後、脚の筋肉へ遺伝子治療を注射しました:muSEAP 単独を運ぶ AAV、または muSEAP と PD-L1 あるいは PD-L2 を同時に運ぶ AAV です。数週間にわたり、導入遺伝子の働きを示す指標として血中の muSEAP レベルを測定しました。AAV に対して事前免疫化されたマウスでは、PD-L1 の同時デリバリーが特に有効で、muSEAP レベルは対照ベクターと比べてはるかに高く、最大12週間にわたり高値が維持されました。PD-L2 も発現を改善しましたが、効果はより小さく変動がありました。対照的に、AAV をこれまで見たことのないナイーブマウスでは、PD-L1 や PD-L2 を加えても持続的な利点は得られず、初期の上昇も時間とともに消える場合がありました。
治療部位の筋肉内で何が起きているか
PD-1 リガンドが効果を示した理由を理解するために、研究者たちは処置した筋肉を詳しく調べました。遺伝子治療は筋組織内でmuSEAPとPD-1リガンドの両方の産生を確実に駆動していました。既往免疫のある動物では、PD-L1 または PD-L2 ベクターを受け取った筋肉は、muSEAP 単独で処置した筋肉に比べて浸潤するT細胞やその他の炎症の兆候が一般に少ないことが分かりました。これらの既往曝露マウスでは、高い muSEAP レベルは一般に免疫細胞数の低下と相関しており、局所的な免疫抑制が処置された細胞の生存を許容し、治療タンパク質の長期的な産生を可能にしたことを示唆しています。チームはまた、AAV に対する抗体とヒトPD-1リガンド自体に対する抗体も測定しました。予想どおり、AAV 抗体は事前免疫化後に上昇して高値が持続しましたが、PD-1 リガンドはこれらの対ベクター抗体を低下させませんでした。興味深いことに、検出可能な対リガンド抗体を誘導したのは主にPD-L1で、しかも主にナイーブマウスに見られました。これは各リガンドが免疫系にとってどの程度「異物」に見えるかに微妙な違いがあることを示唆します。
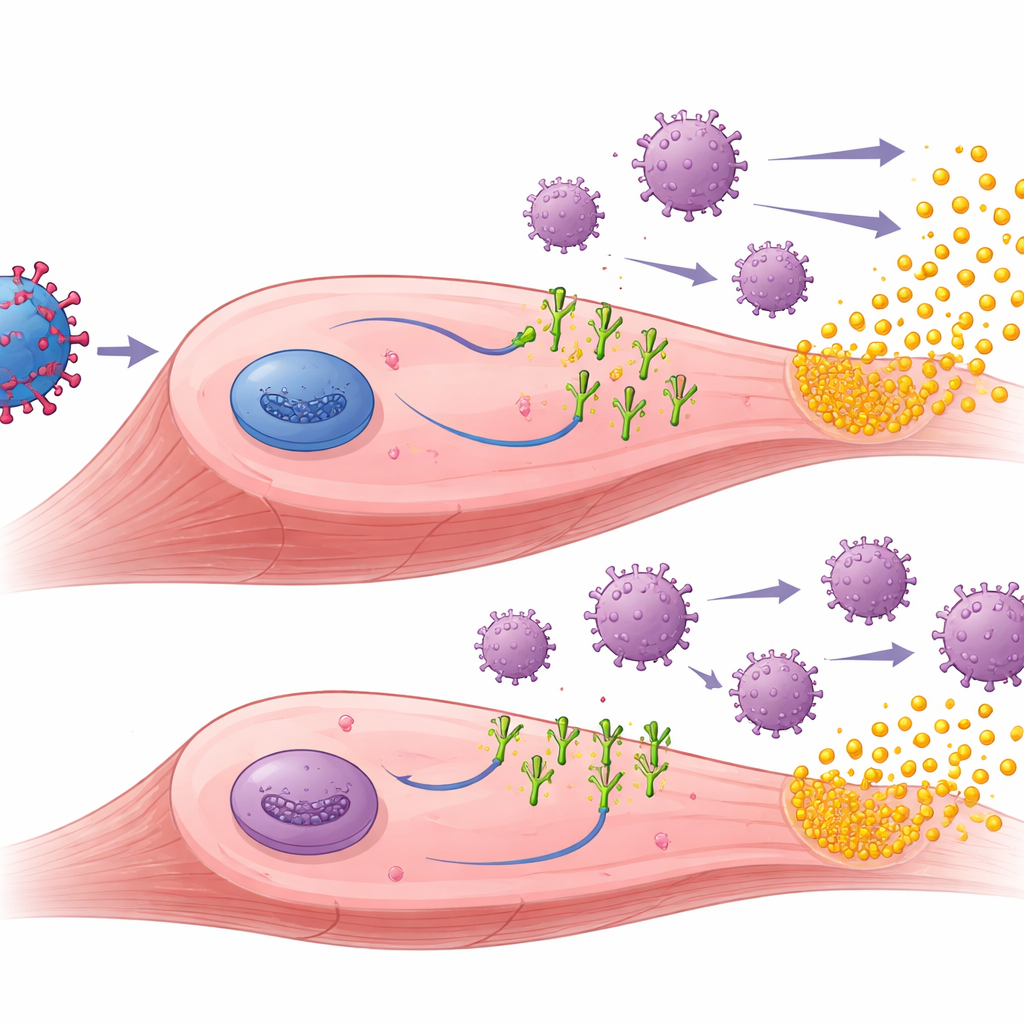
将来の治療にとって何を意味するか
簡潔に言えば、この研究は、治療遺伝子とともに局所的な免疫の「平和維持因子」を同梱することで、既にデリバリーベクターに対して免疫が賦活化されている被験体において遺伝子治療の効果を高め得ることを示しています。トランスジーンとともに PD-L1 または PD-L2 を単一の AAV ベクターで共送達することで、研究者らは既往免疫のあるマウスにおいてより強く長期の遺伝子発現を達成し、かつ処置した筋肉への免疫細胞の攻撃も減らしました。利益と免疫抑制に伴う潜在的リスクの最良のバランスの取り方や、これらの発見がヒトにどのように翻訳されるかなど、多くの疑問が残りますが、本研究はAAVへの過去の曝露のために除外される可能性のあるより広い患者層に遺伝子治療を開く戦略を示唆しています。
引用: Käyhty, P., Nieminen, T., Eriksson, R.A.E. et al. The co-delivery of Programmed Death 1 ligands enhances and prolongs rAAV-mediated gene expression in pre-immunized mice. Gene Ther 33, 127–137 (2026). https://doi.org/10.1038/s41434-025-00588-9
キーワード: 遺伝子治療, AAV ベクター, 免疫寛容, PD-1 チェックポイント, 骨格筋