Clear Sky Science · pl
Wspólne dostarczenie ligandów Programmed Death 1 wzmacnia i przedłuża ekspresję genów zależną od rAAV u myszy z wcześniejszą immunizacją
Uczynienie terapii genowej skuteczniejszą dla większej liczby osób
Terapie genowe wykorzystujące bezpieczne wirusy do dostarczania pomocnych genów zaczynają zmieniać sposób leczenia chorób dziedzicznych. Jednak układy odpornościowe wielu osób już wcześniej rozpoznały te wirusy, co może spowodować osłabienie lub niepowodzenie terapii. W tym badaniu zbadano sposób na „uspokojenie” odpowiedzi immunologicznej dokładnie tam, gdzie działa terapia genowa, tak aby leczenie mogło działać dłużej i pomagać pacjentom, którzy wcześniej zetknęli się z tymi wirusami.
Dlaczego układ odpornościowy atakuje pomocne wirusy
Narzędzia terapii genowej użyte w tym badaniu opierają się na wirusie adeno-zależnym (AAV), maleńkim wirusie powszechnie wykorzystywanym do transportu nowych genów do komórek. AAV jest zwykle bezpieczny i może działać przez lata, ale jest jedno zastrzeżenie: wiele osób już wcześniej zetknęło się z naturalnym AAV w środowisku. Ich układy odpornościowe pamiętają otoczkę wirusa i mogą szybko zaatakować leczone komórki prezentujące fragmenty tej otoczki, przerywając ekspresję wprowadzonego genu. Jest to szczególnie problematyczne w terapii mięśni, które często wymagają wysokich dawek i nie są naturalnie chronione przed atakiem immunologicznym. Obecne obejścia — takie jak wykluczanie pacjentów z istniejącymi przeciwciałami lub stosowanie szerokiego tłumienia odporności — mogą pozostawiać pacjentów bez ochrony przed infekcjami i nie są idealnym rozwiązaniem długoterminowym.
Zap借czenie naturalnego hamulca odporności
Naukowcy sięgnęli po naturalny „hamulec” układu odpornościowego zwany szlakiem PD-1. W zdrowych tkankach PD-1 i jego partnerzy, PD-L1 i PD-L2, pomagają zapobiegać nadmiernym atakom odpornościowym, które mogłyby uszkodzić własne tkanki organizmu. Guzy nowotworowe czasem wykorzystują ten szlak, aby ukryć się przed komórkami odpornościowymi, ale ten sam mechanizm można w zasadzie użyć, by chronić zdrowe komórki zmodyfikowane terapią genową. Zespół zaprojektował wektory AAV przenoszące zarówno gen raportowy (niegroźny sekrecyjny enzym muSEAP, łatwy do oznaczenia we krwi), jak i PD-L1 lub PD-L2, połączone krótkim peptydem samoczynnie rozszczepialnym, który pozwala komórkom produkować oba białka oddzielnie z jednej kasety genowej. Najpierw potwierdzili w hodowlach komórkowych, że konstrukcja „dwa w jednym” działa: zarówno zastępca terapeutyczny, jak i ligandy PD-1 były prawidłowo produkowane, biologicznie aktywne i zdolne do wiązania PD-1.
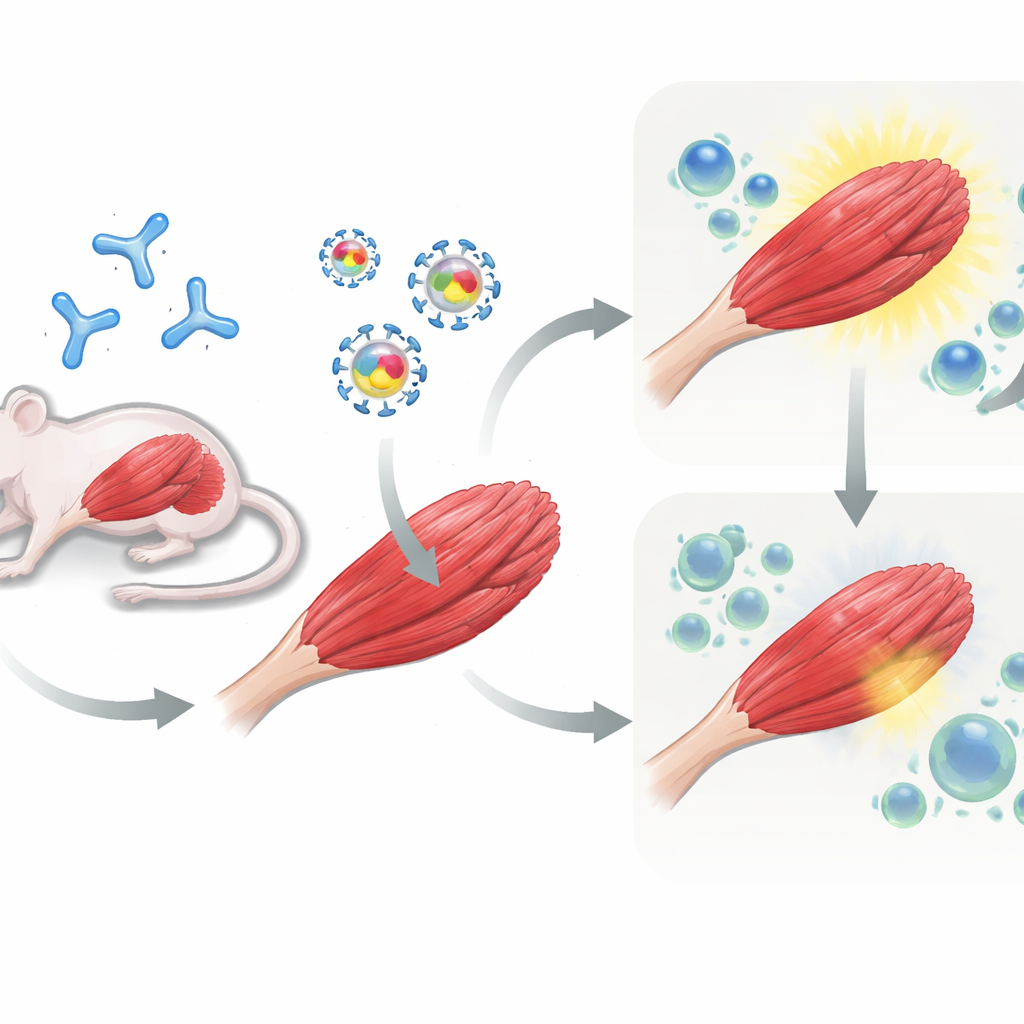
Testowanie strategii u myszy wcześniej narażonych na AAV
Następnie zespół przystąpił do badań na myszach. Niektóre zwierzęta najpierw otrzymały dawkę AAV, aby naśladować pacjentów, którzy już mają odporność na wektor, podczas gdy inne pozostały nieuodpornione. Wszystkie myszy następnie otrzymały terapię genową wstrzykniętą do mięśni uda: albo AAV przenoszące tylko muSEAP, albo AAV przenoszące muSEAP wraz z PD-L1 lub PD-L2. Przez kilka tygodni badacze mierzyli poziomy muSEAP we krwi jako wskaźnik działania wprowadzonego genu. U myszy, które były wcześniej uodpornione przeciwko AAV, współdostarczanie PD-L1 było szczególnie skuteczne: poziomy muSEAP były znacznie wyższe i utrzymywały się do 12 tygodni w porównaniu z wektorem kontrolnym. PD-L2 także poprawiło ekspresję, choć w mniejszym i bardziej zmiennym stopniu. Natomiast u myszy nieuodpornionych, które nigdy wcześniej nie widziały AAV, dodanie PD-L1 lub PD-L2 nie dawało trwałej przewagi i w niektórych przypadkach wczesne korzyści zanikały z czasem.
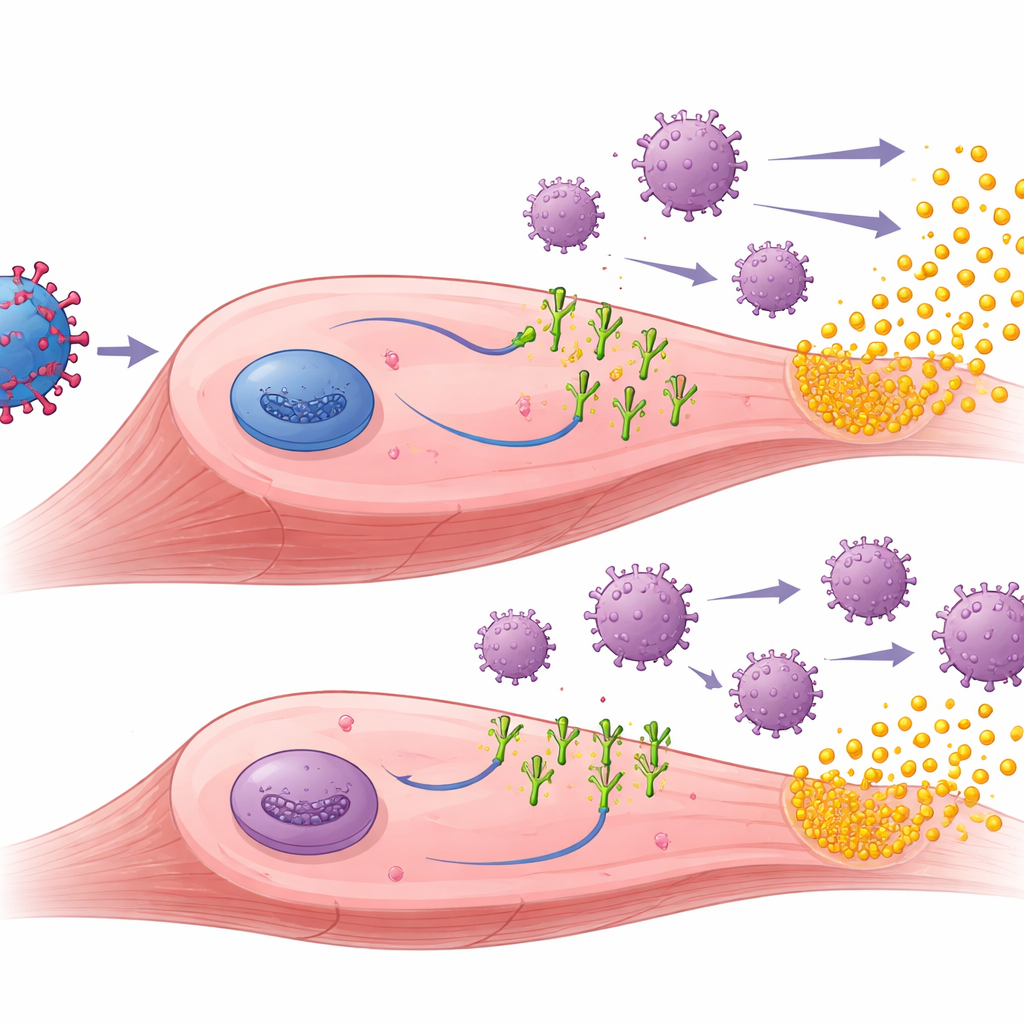
Co dzieje się w leczonym mięśniu
Aby zrozumieć, dlaczego ligandy PD-1 pomagały, badacze zbadali leczone mięśnie. Stwierdzili, że terapia genowa skutecznie powodowała produkcję zarówno muSEAP, jak i ligandów PD-1 w tkance mięśniowej. U zwierząt wcześniej uodpornionych mięśnie, które otrzymały wektory z PD-L1 lub PD-L2, wykazywały zazwyczaj mniej naciekających limfocytów T i innych oznak zapalenia niż mięśnie leczone tylko muSEAP. U tych myszy z wcześniejszą ekspozycją wyższe poziomy muSEAP zwykle szły w parze z mniejszą liczbą komórek odpornościowych, co sugeruje, że miejscowe stłumienie odpowiedzi immunologicznej pozwala leczonym komórkom przetrwać i dłużej produkować terapeutyczne białko. Zespół mierzył także przeciwciała przeciwko AAV i przeciwko samym ludzkim ligandom PD-1. Jak można się było spodziewać, przeciwciała przeciw AAV wzrosły po wstępnej immunizacji i pozostały wysokie, ale ligandy PD-1 nie zmniejszyły tych przeciwciał przeciw wektorowi. Co ciekawe, wykrywalne przeciwciała przeciw ligandowi wywołał jedynie PD-L1, głównie u myszy nieuodpornionych, co sugeruje subtelne różnice w tym, jak obce każdy z ligandów wydaje się układowi odpornościowemu.
Co to może znaczyć dla przyszłych terapii
W prostych słowach, badanie pokazuje, że zapakowanie lokalnego „rozejmowego” elementu immunologicznego razem z genem terapeutycznym może pomóc terapii genowej działać lepiej u osobników, których układy odpornościowe są już nastawione przeciwko wektorowi dostarczającemu. Poprzez współdostarczenie PD-L1 lub PD-L2 bezpośrednio z transgenem w jednym wektorze AAV, autorzy osiągnęli silniejszą i dłużej utrzymującą się ekspresję genu u myszy z wcześniejszą immunizacją, obserwując jednocześnie mniejszy napór komórek odpornościowych na leczone mięśnie. Chociaż pozostaje wiele pytań — na przykład jak najlepiej zrównoważyć korzyści z potencjalnymi ryzykami tłumienia odporności oraz jak wyniki te przełożą się na ludzi — prace te wskazują strategię, która mogłaby otworzyć terapię genową na szerszą grupę pacjentów, którzy w przeciwnym razie mogliby być wykluczeni z powodu wcześniejszego kontaktu z AAV.
Cytowanie: Käyhty, P., Nieminen, T., Eriksson, R.A.E. et al. The co-delivery of Programmed Death 1 ligands enhances and prolongs rAAV-mediated gene expression in pre-immunized mice. Gene Ther 33, 127–137 (2026). https://doi.org/10.1038/s41434-025-00588-9
Słowa kluczowe: terapia genowa, wektory AAV, tolerancja immunologiczna, punkt kontrolny PD-1, mięsień szkieletowy