Clear Sky Science · es
La coadministración de ligandos de PD-1 mejora y prolonga la expresión génica mediada por rAAV en ratones preinmunizados
Hacer que la terapia génica funcione para más personas
Las terapias génicas que usan virus inofensivos para transportar genes beneficiosos están empezando a cambiar el tratamiento de las enfermedades hereditarias. Pero los sistemas inmunitarios de muchas personas ya reconocen estos virus, lo que puede hacer que el tratamiento se desvanezca o fracase. Este estudio explora una forma de "calmar" la respuesta inmune justo donde actúa la terapia génica, de modo que el tratamiento pueda durar más y ayudar a pacientes que han estado expuestos a estos virus con anterioridad.
Por qué el sistema inmune combate virus útiles
Las herramientas de terapia génica en este estudio se basan en el virus adenoasociado (AAV), un virus diminuto ampliamente utilizado para introducir nuevos genes en las células. El AAV es generalmente seguro y puede mantener su efecto durante años, pero hay un inconveniente: muchas personas ya han encontrado AAV natural en el entorno. Sus sistemas inmunitarios recuerdan la cápside viral y pueden atacar rápidamente las células tratadas que presentan fragmentos de esa cápside, interrumpiendo la expresión génica. Esto es especialmente preocupante en tratamientos musculares, que a menudo requieren dosis altas y no están naturalmente protegidos frente al ataque inmunitario. Las soluciones actuales—como excluir a pacientes con anticuerpos preexistentes o administrar fármacos inmunosupresores de amplio espectro—pueden dejar a los pacientes sin protección frente a infecciones y no son soluciones ideales a largo plazo.
Tomando prestado un freno natural de la inmunidad
Los investigadores se dirigieron a un "freno" natural del sistema inmune llamado vía PD-1. En tejidos sanos, PD-1 y sus asociados, PD-L1 y PD-L2, ayudan a prevenir ataques inmunitarios excesivos que podrían dañar el propio organismo. Los tumores a veces explotan esta vía para ocultarse de las células inmunitarias, pero el mismo mecanismo puede, en principio, usarse para proteger células sanas modificadas por terapia génica. El equipo diseñó vectores AAV que llevan tanto un gen reportero (una enzima secretada inofensiva llamada muSEAP, que puede medirse fácilmente en sangre) como PD-L1 o PD-L2, unidos por un péptido autocleavable corto que permite a las células producir ambas proteínas por separado desde un mismo cassette genético. Primero confirmaron en cultivos celulares que el diseño "dos en uno" funcionaba: tanto el marcador terapéutico como los ligandos de PD-1 se producían correctamente, eran biológicamente activos y podían unirse a PD-1.
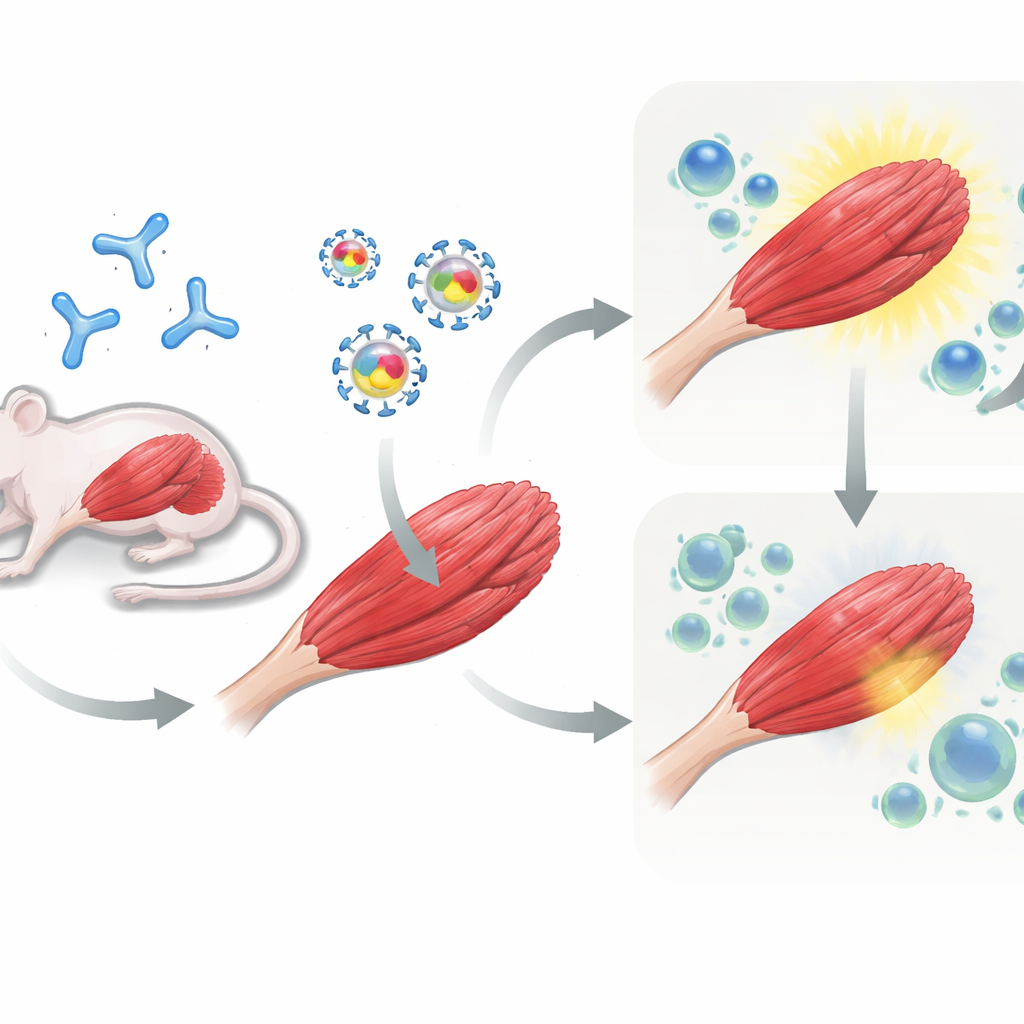
Probando la estrategia en ratones preexpuestos
A continuación, el equipo pasó a ensayos en ratones. A algunos animales se les administró primero una dosis de AAV para imitar a pacientes que ya albergan inmunidad frente al vector, mientras que otros permanecieron vírgenes frente al virus. Todos los ratones recibieron después la terapia génica inyectada en los músculos de la pierna: bien AAV portador de muSEAP solo, bien AAV portador de muSEAP más PD-L1 o PD-L2. Durante varias semanas, los investigadores midieron los niveles de muSEAP en sangre como indicador de cuánto funcionaba el gen introducido. En los ratones que habían sido preinmunizados contra AAV, la coadministración de PD-L1 fue especialmente eficaz: los niveles de muSEAP fueron mucho mayores y se mantuvieron elevados hasta 12 semanas en comparación con el vector de control. PD-L2 también mejoró la expresión, aunque en menor medida y con más variabilidad. En contraste, en ratones vírgenes que nunca habían visto AAV, añadir PD-L1 o PD-L2 no produjo una ventaja duradera y, en algunos casos, cualquier ganancia inicial se perdió con el tiempo.
Qué ocurre dentro del músculo tratado
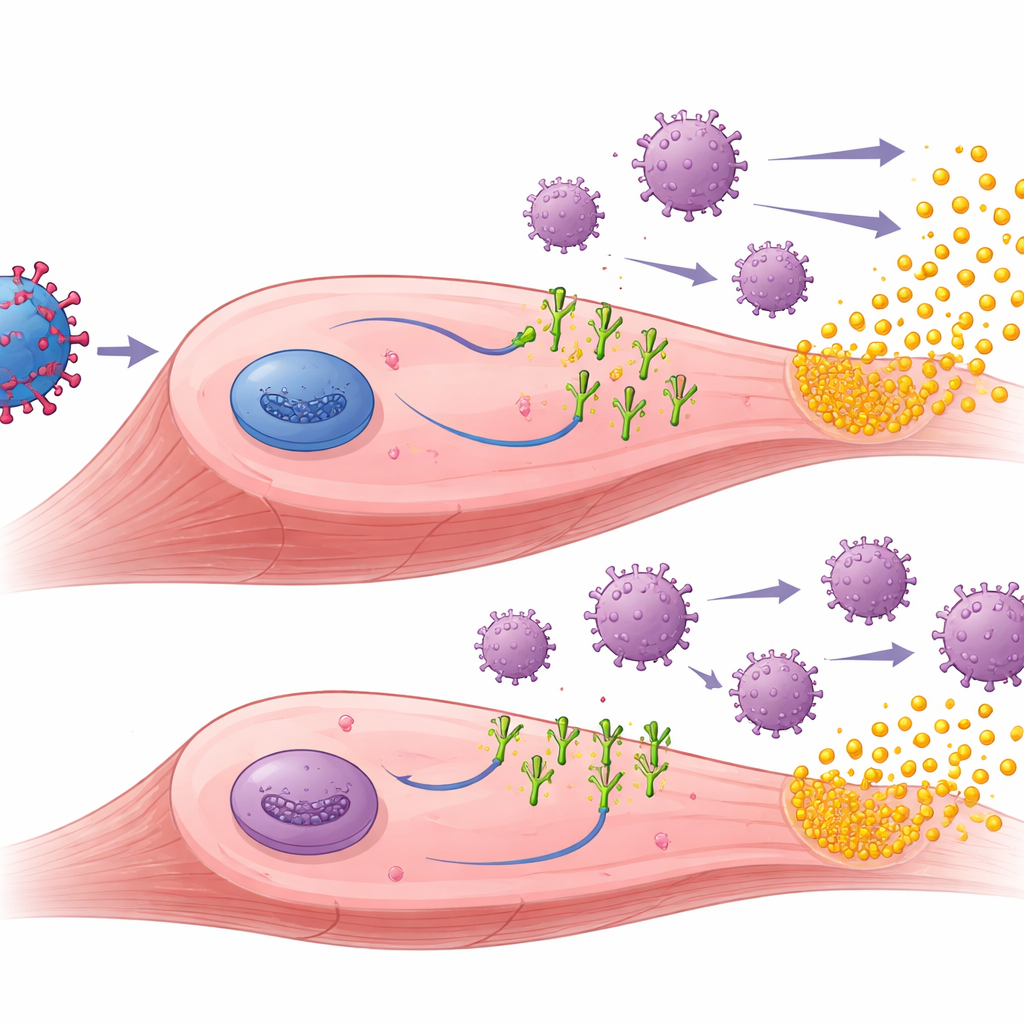
Para entender por qué los ligandos de PD-1 ayudaron, los investigadores examinaron los músculos tratados. Encontraron que la terapia génica impulsó con éxito la producción tanto de muSEAP como de los ligandos de PD-1 en el tejido muscular. En los animales preinmunizados, los músculos que recibieron los vectores con PD-L1 o PD-L2 mostraron generalmente menos linfocitos T invasores y otros signos de inflamación que los músculos tratados solo con muSEAP. En estos ratones preexpuestos, los niveles más altos de muSEAP tendían a ir acompañados de un menor número de células inmunitarias, lo que sugiere que la atenuación inmune local permitía que las células tratadas sobrevivieran y siguieran produciendo la proteína terapéutica durante más tiempo. El equipo también midió anticuerpos contra AAV y contra los propios ligandos humanos de PD-1. Como era de esperar, los anticuerpos contra AAV aumentaron tras la preinmunización y se mantuvieron altos, pero los ligandos de PD-1 no redujeron estos anticuerpos anti-vector. Curiosamente, solo PD-L1 desencadenó anticuerpos detectables contra el ligando, y principalmente en ratones vírgenes, lo que apunta a sutiles diferencias en la percepción de cada ligando como elemento extraño por el sistema inmune.
Qué podría significar esto para tratamientos futuros
En términos sencillos, este estudio muestra que empaquetar un "pacificador" inmune local junto con un gen terapéutico puede ayudar a que la terapia génica funcione mejor en sujetos cuyos sistemas inmunitarios ya están sensibilizados frente al virus de entrega. Al coadministrar PD-L1 o PD-L2 directamente con el transgén en un único vector AAV, los autores lograron una expresión génica más fuerte y duradera en ratones preinmunizados, al tiempo que observaron menos células inmunitarias atacando el músculo tratado. Aunque quedan muchas preguntas por resolver—como cómo equilibrar mejor los beneficios con los posibles riesgos de atenuar la inmunidad y cómo se traducirán estos hallazgos a humanos—el trabajo apunta a una estrategia que podría abrir la terapia génica a un grupo más amplio de pacientes que de otro modo podrían quedar excluidos por una exposición previa al AAV.
Cita: Käyhty, P., Nieminen, T., Eriksson, R.A.E. et al. The co-delivery of Programmed Death 1 ligands enhances and prolongs rAAV-mediated gene expression in pre-immunized mice. Gene Ther 33, 127–137 (2026). https://doi.org/10.1038/s41434-025-00588-9
Palabras clave: terapia génica, vectores AAV, tolerancia inmune, punto de control PD-1, músculo esquelético