Clear Sky Science · pt
A coentrega dos ligantes de Programmed Death 1 melhora e prolonga a expressão gênica mediada por rAAV em camundongos pré-imunizados
Tornando a terapia gênica eficaz para mais pessoas
Terapias gênicas que usam vírus inofensivos para entregar genes úteis começam a transformar o tratamento de doenças hereditárias. Mas o sistema imunológico de muitas pessoas já reconhece esses vírus, o que pode fazer o tratamento desaparecer ou falhar. Este estudo explora uma forma de “acalmar” a resposta imune justamente no local onde a terapia gênica atua, para que o tratamento dure mais e beneficie pacientes que já foram expostos a esses vírus.
Por que o sistema imune ataca vírus úteis
As ferramentas de terapia gênica deste estudo baseiam-se no vírus adeno-associado (AAV), um vírus pequeno amplamente usado para transportar novos genes a células. AAV é geralmente seguro e pode permanecer ativo por anos, mas há um problema: muitas pessoas já encontraram o AAV natural no ambiente. Seus sistemas imunes lembram a cápside viral e podem atacar rapidamente células tratadas que exibem pedaços dessa cápside, interrompendo a expressão gênica. Isso é particularmente preocupante em tratamentos musculares, que frequentemente exigem doses altas e não têm proteção natural contra ataques imunes. Soluções atuais — como excluir pacientes com anticorpos pré-existentes ou administrar drogas imunossupressoras gerais — podem deixar os pacientes desprotegidos contra infecções e não são ideais a longo prazo.
Emprestando um freio natural da imunidade
Os pesquisadores recorreram a um “freio” natural do sistema imune chamado via PD-1. Em tecidos saudáveis, o PD-1 e seus parceiros, PD-L1 e PD-L2, ajudam a prevenir ataques imunológicos excessivos que poderiam danificar o próprio organismo. Tumores às vezes exploram essa via para se esconder das células imunes, mas o mesmo mecanismo pode, em princípio, ser usado para proteger células saudáveis modificadas por terapia gênica. A equipe projetou vetores AAV que carregam tanto um gene repórter (uma enzima secretada inofensiva chamada muSEAP, facilmente mensurável no sangue) quanto PD-L1 ou PD-L2, ligados por um pequeno peptídeo autoclastic que permite às células produzir ambas as proteínas separadamente a partir de um único cassete genético. Eles primeiro confirmaram em culturas celulares que o design “dois em um” funcionou: tanto o substituto terapêutico quanto os ligantes PD-1 foram produzidos corretamente, estavam biologicamente ativos e eram capazes de se ligar ao PD-1.
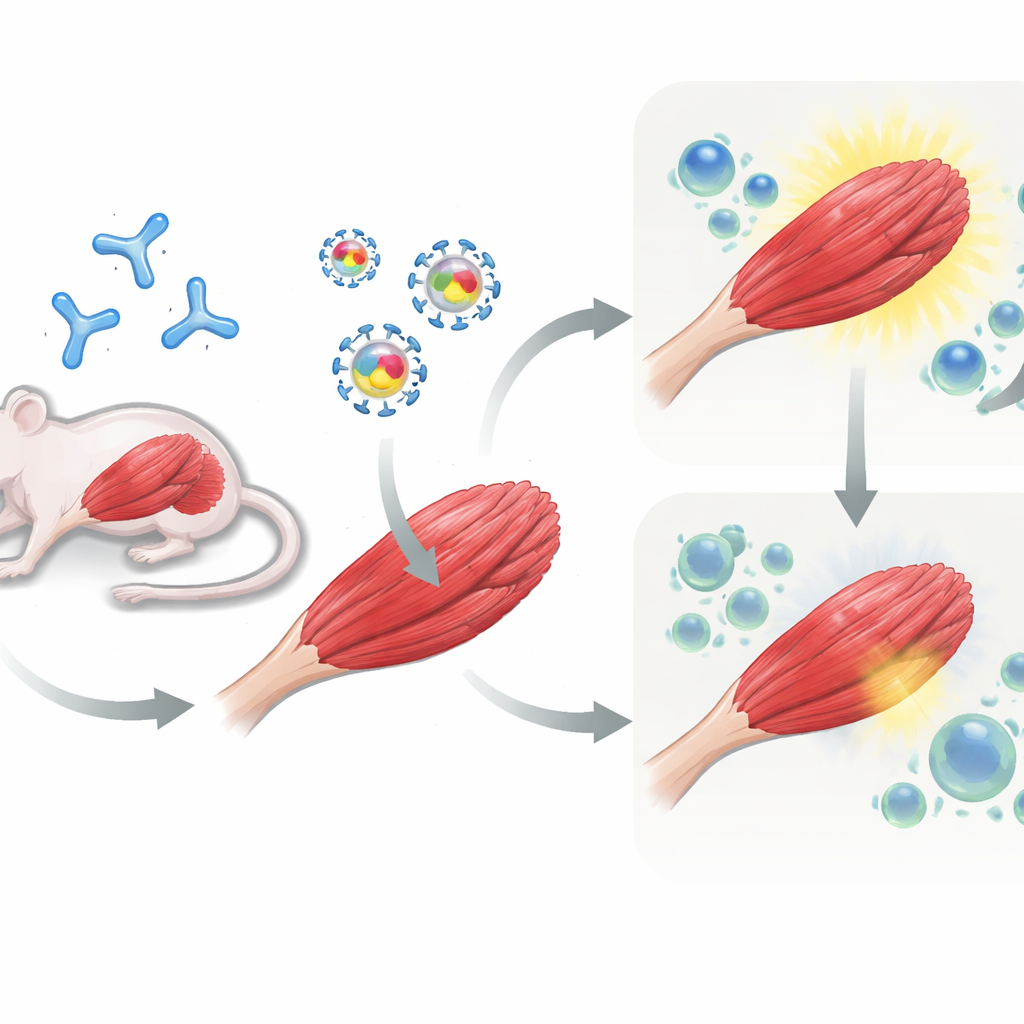
Testando a estratégia em camundongos pré-expostos
Em seguida, a equipe passou para experimentos em camundongos. Alguns animais receberam primeiro uma dose de AAV para imitar pacientes que já possuem imunidade contra o vetor, enquanto outros permaneceram ingênuos. Todos os camundongos então receberam a terapia gênica injetada nos músculos da perna: ou AAV carregando apenas muSEAP, ou AAV carregando muSEAP junto com PD-L1 ou PD-L2. Ao longo de várias semanas, os pesquisadores mediram os níveis de muSEAP no sangue como indicador de quão bem o gene introduzido estava funcionando. Em camundongos pré-imunizados contra AAV, a coentrega de PD-L1 foi especialmente eficaz: os níveis de muSEAP foram muito mais altos e permaneceram elevados por até 12 semanas comparado ao vetor controle. PD-L2 também melhorou a expressão, embora em menor grau e com maior variabilidade. Em contraste, em camundongos ingênuos que nunca haviam visto AAV antes, adicionar PD-L1 ou PD-L2 não produziu uma vantagem duradoura e, em alguns casos, qualquer ganho inicial desapareceu com o tempo.
O que acontece dentro do músculo tratado
Para entender por que os ligantes PD-1 ajudaram, os pesquisadores examinaram os músculos tratados. Eles descobriram que a terapia gênica impulsionou com sucesso a produção tanto de muSEAP quanto dos ligantes PD-1 no tecido muscular. Nos animais pré-imunizados, músculos que receberam os vetores com PD-L1 ou PD-L2 geralmente mostraram menos infiltração de células T e outros sinais de inflamação do que músculos tratados apenas com muSEAP. Nesses camundongos pré-expostos, níveis mais altos de muSEAP tendiam a andar de mãos dadas com menor número de células imunes, sugerindo que a atenuação imune local permitiu que as células tratadas sobrevivessem e continuassem produzindo a proteína terapêutica por mais tempo. A equipe também mediu anticorpos contra AAV e contra os próprios ligantes humanos de PD-1. Como esperado, os anticorpos anti-AAV aumentaram após a pré-imunização e permaneceram altos, mas os ligantes PD-1 não reduziram esses anticorpos anti-vetor. Curiosamente, somente PD-L1 desencadeou anticorpos detectáveis contra o ligante, principalmente em camundongos ingênuos, sugerindo diferenças sutis em quão estranho cada ligante parece ao sistema imune.
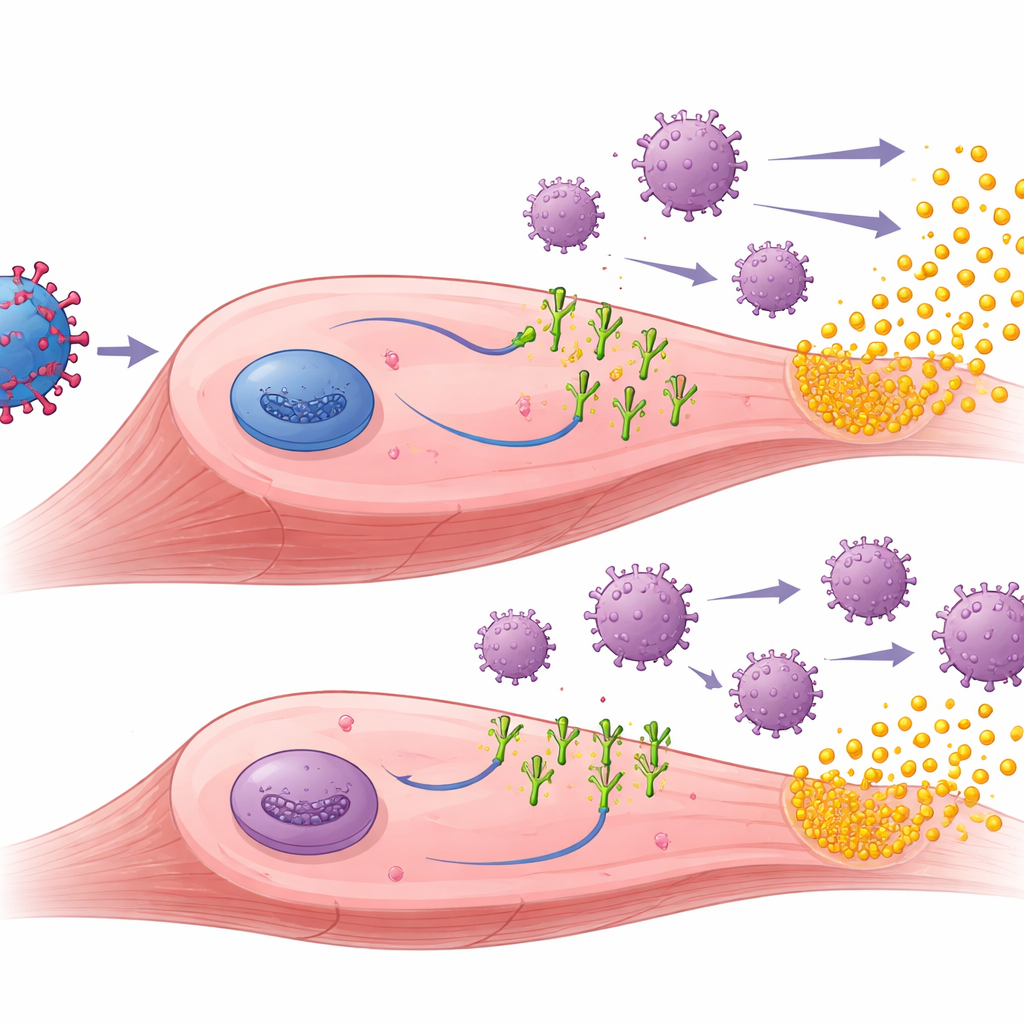
O que isso pode significar para tratamentos futuros
Em termos simples, este estudo mostra que empacotar um “pacificador” imune local junto com um gene terapêutico pode ajudar a terapia gênica a funcionar melhor em indivíduos cujos sistemas imunes já estão sensibilizados contra o vírus de entrega. Ao coentregar PD-L1 ou PD-L2 diretamente com o transgene em um único vetor AAV, os autores alcançaram expressão gênica mais forte e duradoura em camundongos pré-imunizados, além de observar menos células imunes atacando o músculo tratado. Embora muitas questões permaneçam — como a melhor forma de equilibrar benefícios com riscos potenciais de suprimir a imunidade, e como esses achados se traduzirão em humanos — o trabalho aponta para uma estratégia que pode abrir a terapia gênica a um grupo mais amplo de pacientes que, de outra forma, poderiam ser excluídos por exposição prévia ao AAV.
Citação: Käyhty, P., Nieminen, T., Eriksson, R.A.E. et al. The co-delivery of Programmed Death 1 ligands enhances and prolongs rAAV-mediated gene expression in pre-immunized mice. Gene Ther 33, 127–137 (2026). https://doi.org/10.1038/s41434-025-00588-9
Palavras-chave: terapia gênica, vetores AAV, tolerância imune, checkpoint PD-1, músculo esquelético