Clear Sky Science · it
La co-somministrazione dei ligandi di Programmed Death 1 potenzia e prolunga l’espressione genica mediata da rAAV in topi pre-immunizzati
Rendere la terapia genica efficace per più persone
Le terapie geniche che utilizzano virus innocui per consegnare geni utili stanno iniziando a cambiare il trattamento delle malattie ereditarie. Ma il sistema immunitario di molte persone riconosce già questi virus, il che può far svanire o fallire la terapia. Questo studio esplora un modo per “calmare” la risposta immunitaria proprio dove la terapia genica agisce, in modo che il trattamento possa durare più a lungo e aiutare pazienti già esposti a questi virus.
Perché il sistema immunitario attacca virus utili
Gli strumenti di terapia genica in questo studio si basano sul virus adeno-associato (AAV), un minuscolo virus ampiamente usato per trasferire nuovi geni nelle cellule. L’AAV è generalmente sicuro e può continuare a funzionare per anni, ma c’è un problema: molte persone hanno già incontrato l’AAV naturale nell’ambiente. I loro sistemi immunitari ricordano il capsidio virale e possono attaccare rapidamente le cellule trattate che mostrano pezzi di quel rivestimento, interrompendo l’espressione genica. Questo è particolarmente rilevante per i trattamenti muscolari, che spesso richiedono dosi elevate e non sono naturalmente protetti dagli attacchi immunitari. Le soluzioni attuali — come escludere pazienti con anticorpi preesistenti o somministrare farmaci immunosoppressivi generalizzati — possono lasciare i pazienti vulnerabili alle infezioni e non sono ideali nel lungo termine.
Prendere in prestito un freno naturale dell’immunità
I ricercatori si sono rivolti a un “freno” naturale del sistema immunitario chiamato via PD-1. Nei tessuti sani, PD-1 e i suoi partner, PD-L1 e PD-L2, aiutano a prevenire attacchi immunitari eccessivi che potrebbero danneggiare l’organismo. I tumori talvolta sfruttano questa via per nascondersi dalle cellule immunitarie, ma lo stesso meccanismo può, in linea di principio, essere usato per proteggere le cellule sane modificate dalla terapia genica. Il team ha progettato vettori AAV che trasportano sia un gene reporter (un enzima secreto innocuo chiamato muSEAP, facilmente misurabile nel sangue) sia PD-L1 o PD-L2, collegati da un breve peptide auto-cleavante che permette alle cellule di produrre entrambi le proteine separatamente da un unico cassette genica. Hanno prima confermato in colture cellulari che il design “due-in-uno” funzionava: sia il sostituto terapeutico sia i ligandi PD-1 venivano prodotti correttamente, risultavano biologicamente attivi e in grado di legarsi a PD-1.
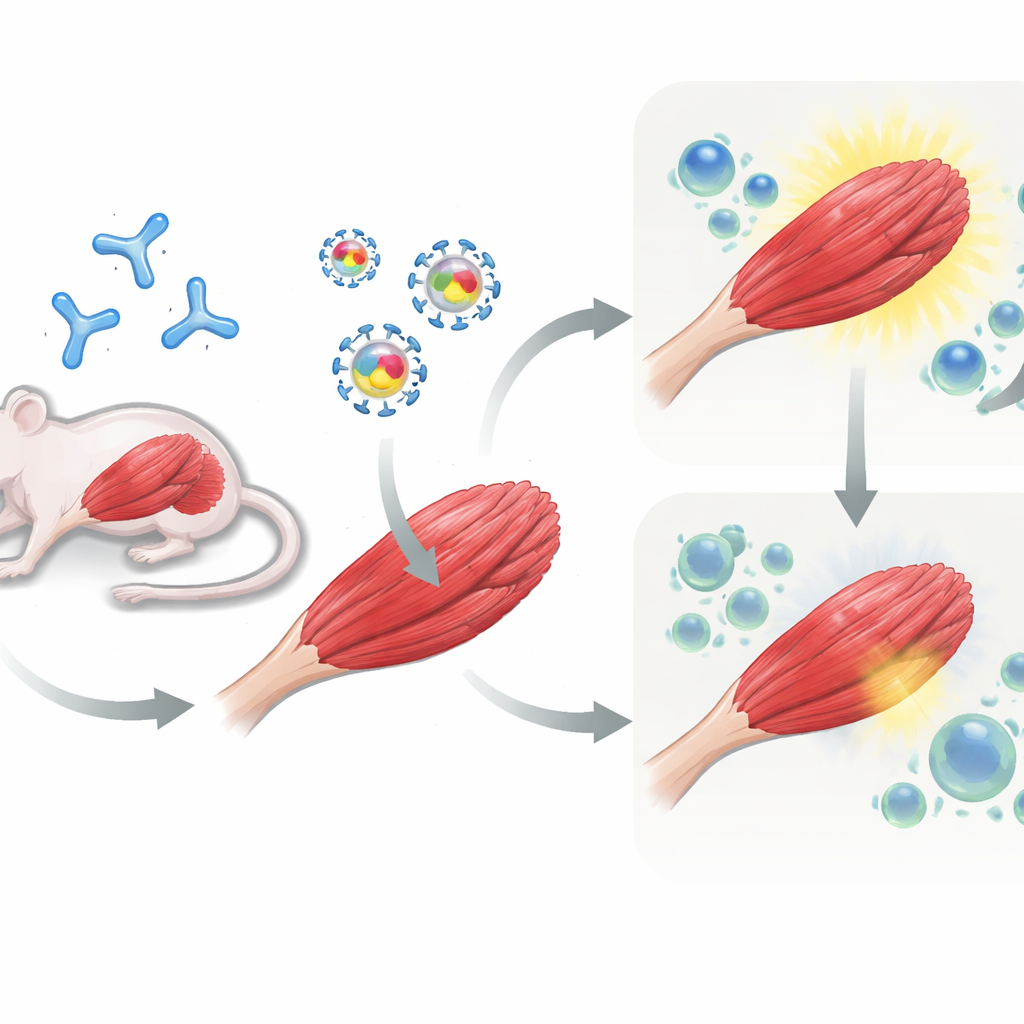
Testare la strategia in topi pre-esposti
Successivamente, il team è passato ai topi. Alcuni animali hanno ricevuto prima una dose di AAV per simulare pazienti che già possiedono immunità verso il vettore, mentre altri sono rimasti naïve. Tutti i topi hanno poi ricevuto la terapia genica iniettata nei muscoli della zampa: AAV contenente solo muSEAP oppure AAV contenente muSEAP più PD-L1 o PD-L2. Per diverse settimane i ricercatori hanno misurato i livelli di muSEAP nel sangue come indicatore di quanto bene funzionasse il gene introdotto. Nei topi pre-immunizzati contro AAV, la co-somministrazione di PD-L1 è risultata particolarmente efficace: i livelli di muSEAP erano molto più alti e rimanevano elevati fino a 12 settimane rispetto al vettore di controllo. Anche PD-L2 ha migliorato l’espressione, sebbene in misura minore e più variabile. Al contrario, nei topi naïve che non avevano mai incontrato l’AAV, l’aggiunta di PD-L1 o PD-L2 non ha prodotto un vantaggio duraturo e, in alcuni casi, qualsiasi guadagno iniziale è svanito nel tempo.
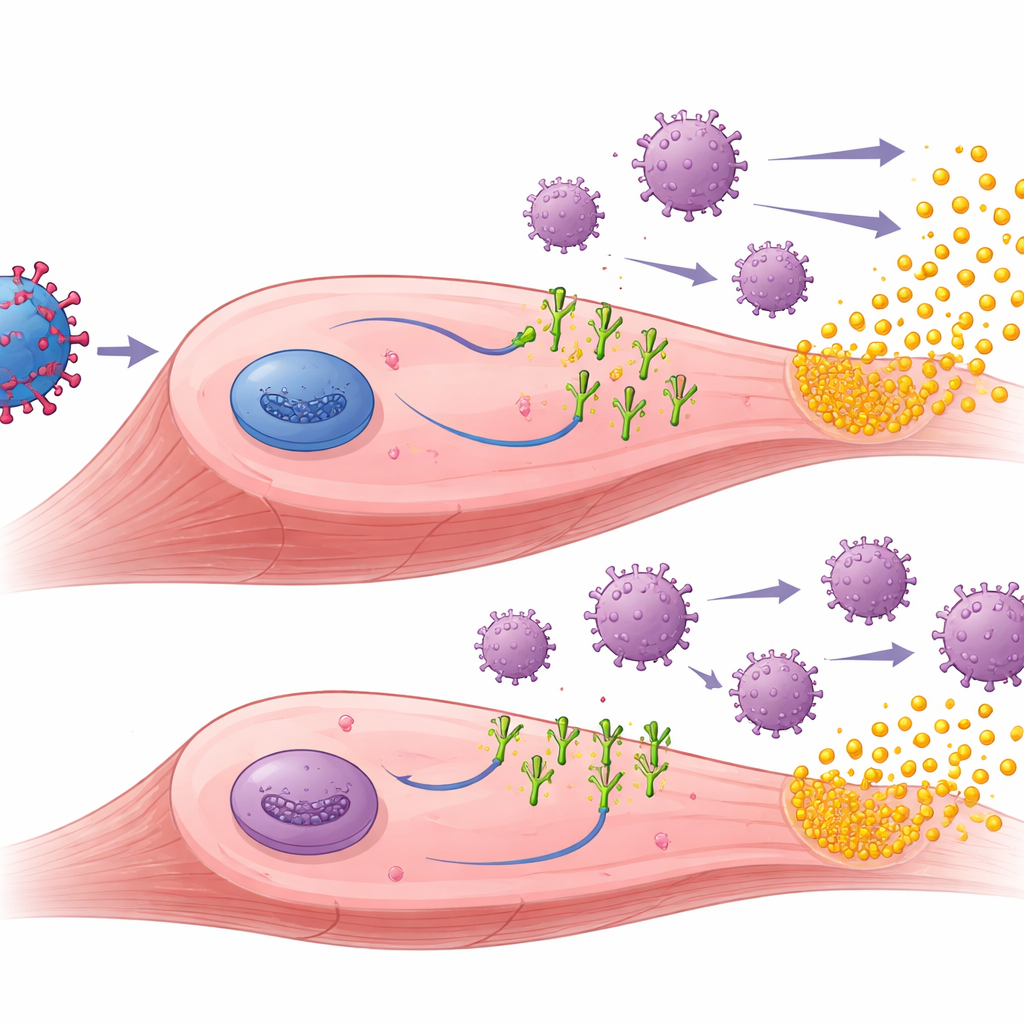
Cosa succede all’interno del muscolo trattato
Per capire perché i ligandi PD-1 fossero d’aiuto, i ricercatori hanno esaminato i muscoli trattati. Hanno riscontrato che la terapia genica induceva con successo la produzione sia di muSEAP sia dei ligandi PD-1 nel tessuto muscolare. Negli animali pre-immunizzati, i muscoli che avevano ricevuto i vettori PD-L1 o PD-L2 mostravano generalmente meno cellule T infiltranti e altri segni di infiammazione rispetto ai muscoli trattati con solo muSEAP. In questi topi pre-esposti, livelli più alti di muSEAP tendevano a corrispondere a numeri inferiori di cellule immunitarie, suggerendo che l’attenuazione immunitaria locale permetteva alle cellule trattate di sopravvivere e continuare a produrre la proteina terapeutica più a lungo. Il team ha anche misurato gli anticorpi contro l’AAV e contro gli stessi ligandi PD-1 umani. Come previsto, gli anticorpi anti-AAV aumentavano dopo la pre-immunizzazione e rimanevano elevati, ma i ligandi PD-1 non riducevano questi anticorpi anti-vettore. Interessante notare che solo PD-L1 ha scatenato anticorpi anti-ligando rilevabili, soprattutto nei topi naïve, suggerendo sottili differenze nella percezione di “estraneità” di ciascun ligando da parte del sistema immunitario.
Cosa potrebbe significare per trattamenti futuri
In termini semplici, questo studio mostra che impacchettare un “pacificatore” immunitario locale insieme a un gene terapeutico può migliorare l’efficacia della terapia genica in soggetti i cui sistemi immunitari sono già pronti contro il virus vettore. Co-somministrando PD-L1 o PD-L2 direttamente con il transgene in un singolo vettore AAV, gli autori hanno ottenuto un’espressione genica più forte e duratura nei topi pre-immunizzati, osservando al contempo meno cellule immunitarie che attaccavano il muscolo trattato. Sebbene restino molte questioni — come bilanciare al meglio i benefici con i potenziali rischi di attenuare l’immunità e come questi risultati si tradurranno negli esseri umani — il lavoro indica una strategia che potrebbe aprire la terapia genica a un gruppo più ampio di pazienti altrimenti esclusi a causa dell’esposizione pregressa all’AAV.
Citazione: Käyhty, P., Nieminen, T., Eriksson, R.A.E. et al. The co-delivery of Programmed Death 1 ligands enhances and prolongs rAAV-mediated gene expression in pre-immunized mice. Gene Ther 33, 127–137 (2026). https://doi.org/10.1038/s41434-025-00588-9
Parole chiave: terapia genica, vettori AAV, tolleranza immunitaria, checkpoint PD-1, muscolo scheletrico