Clear Sky Science · fr
La co-administration des ligands de la protéine de mort programmée 1 améliore et prolonge l'expression génique médiée par rAAV chez des souris pré-immunisées
Rendre la thérapie génique efficace pour davantage de personnes
Les thérapies géniques qui utilisent des virus inoffensifs pour délivrer des gènes utiles commencent à transformer la prise en charge des maladies héréditaires. Mais le système immunitaire de nombreuses personnes reconnaît déjà ces virus, ce qui peut entraîner l'affaiblissement ou l'échec du traitement. Cette étude explore une méthode pour « apaiser » la réponse immunitaire là où la thérapie génique agit, afin que le traitement dure plus longtemps et soit efficace chez des patients déjà exposés à ces virus.
Pourquoi le système immunitaire combat des virus utiles
Les outils de thérapie génique de cette étude reposent sur le virus adéno-associé (AAV), un petit virus largement utilisé pour introduire de nouveaux gènes dans les cellules. L'AAV est généralement sûr et peut rester actif pendant des années, mais il y a un bémol : beaucoup de personnes ont déjà rencontré l'AAV naturel. Leur système immunitaire se souvient de la capside virale et peut attaquer rapidement les cellules traitées qui présentent des fragments de cette capside, interrompant l'expression génique. C'est particulièrement préoccupant pour les traitements musculaires, qui requièrent souvent des doses élevées et ne sont pas naturellement protégés contre l'attaque immunitaire. Les solutions actuelles — comme exclure les patients ayant des anticorps préexistants ou administrer des immunosuppresseurs larges — peuvent laisser les patients vulnérables aux infections et ne constituent pas des solutions idéales à long terme.
Emprunter un frein naturel de l'immunité
Les chercheurs se sont tournés vers un « frein » naturel du système immunitaire appelé voie PD-1. Dans les tissus sains, PD-1 et ses partenaires PD-L1 et PD-L2 contribuent à prévenir des attaques immunitaires excessives qui pourraient endommager l'organisme. Les tumeurs exploitent parfois cette voie pour se cacher des cellules immunitaires, mais le même mécanisme peut, en principe, protéger des cellules saines modifiées par thérapie génique. L'équipe a conçu des vecteurs AAV qui transportent à la fois un gène rapporteur (une enzyme sécrétée inoffensive appelée muSEAP, facile à mesurer dans le sang) et soit PD-L1 soit PD-L2, reliés par un court peptide auto-clivable permettant aux cellules de produire les deux protéines séparément à partir d'une seule cassette génétique. Ils ont d'abord confirmé en cultures cellulaires que la conception « deux-en-un » fonctionnait : à la fois le substitut thérapeutique et les ligands PD-1 étaient correctement produits, biologiquement actifs et capables de se lier à PD-1.
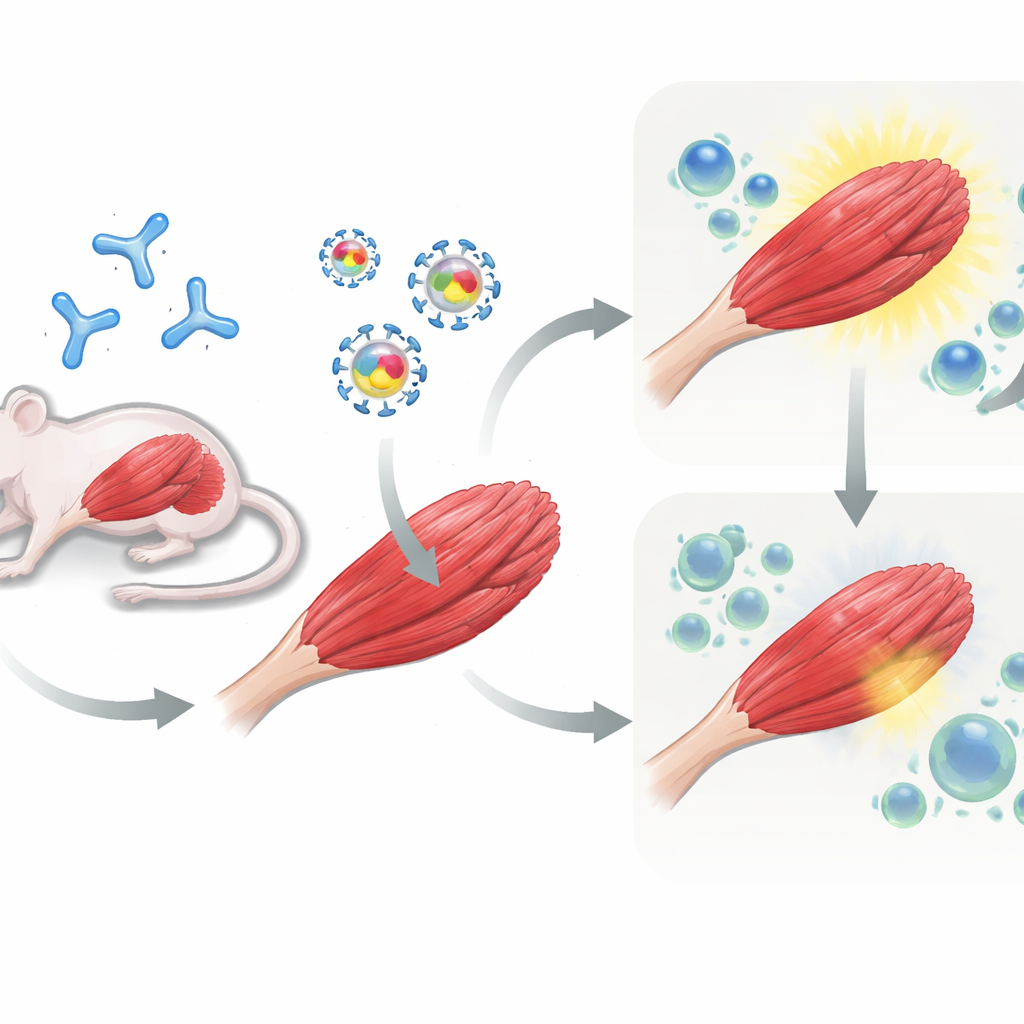
Tester la stratégie chez des souris pré-exposées
Ensuite, l'équipe est passée aux expériences chez la souris. Certains animaux ont d'abord reçu une dose d'AAV pour mimer des patients déjà immunisés contre le vecteur, tandis que d'autres sont restés naïfs. Tous les oiseaux ont ensuite reçu la thérapie génique injectée dans les muscles des pattes : soit l'AAV portant muSEAP seul, soit l'AAV portant muSEAP plus PD-L1 ou PD-L2. Sur plusieurs semaines, les chercheurs ont mesuré les niveaux de muSEAP dans le sang comme indicateur du fonctionnement du gène introduit. Chez les souris pré-immunisées contre l'AAV, la co-administration de PD-L1 s'est montrée particulièrement efficace : les niveaux de muSEAP étaient bien plus élevés et restaient élevés jusqu'à 12 semaines par rapport au vecteur témoin. PD-L2 a également amélioré l'expression, quoique dans une moindre mesure et avec plus de variabilité. En revanche, chez les souris naïves n'ayant jamais rencontré l'AAV, l'ajout de PD-L1 ou PD-L2 n'apportait pas d'avantage durable et, dans certains cas, tout gain initial s'est estompé avec le temps.
Ce qui se passe à l'intérieur du muscle traité
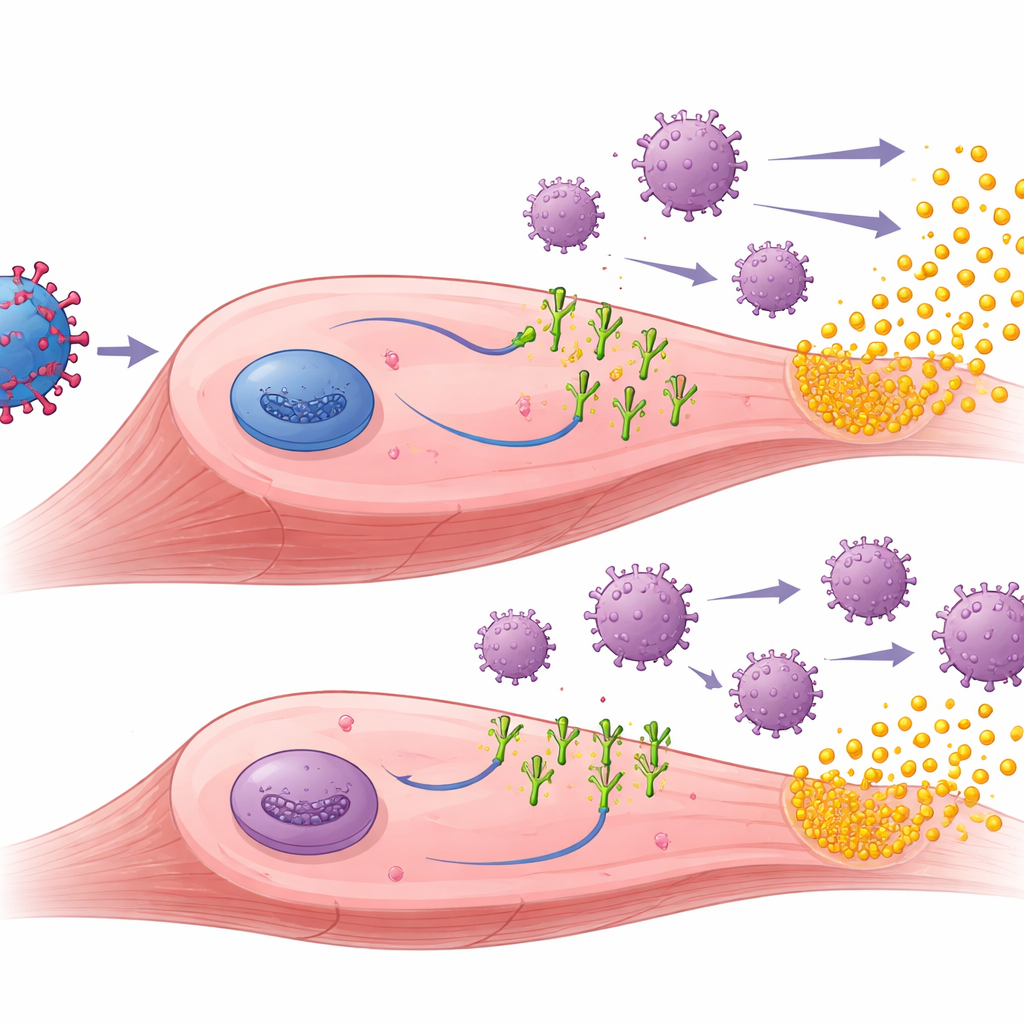
Pour comprendre pourquoi les ligands PD-1 ont aidé, les chercheurs ont examiné les muscles traités. Ils ont constaté que la thérapie génique induisait avec succès la production à la fois de muSEAP et des ligands PD-1 dans le tissu musculaire. Chez les animaux pré-immunisés, les muscles ayant reçu les vecteurs PD-L1 ou PD-L2 présentaient généralement moins de cellules T infiltrantes et moins de signes d'inflammation que les muscles traités par muSEAP seul. Chez ces souris pré-exposées, des niveaux plus élevés de muSEAP allaient généralement de pair avec un nombre réduit de cellules immunitaires, suggérant qu'une atténuation locale de la réponse immunitaire permettait aux cellules traitées de survivre et de continuer à produire la protéine thérapeutique plus longtemps. L'équipe a également mesuré les anticorps dirigés contre l'AAV et contre les ligands PD-1 humains eux-mêmes. Comme prévu, les anticorps anti-AAV ont augmenté après la pré-immunisation et sont restés élevés, mais les ligands PD-1 n'ont pas réduit ces anticorps anti-vecteur. Fait intéressant, seul PD-L1 a déclenché des anticorps anti-ligand détectables, et principalement chez les souris naïves, ce qui suggère de subtiles différences dans la perception de l'étrangeté de chaque ligand par le système immunitaire.
Ce que cela pourrait signifier pour les traitements futurs
Concrètement, cette étude montre qu'emballer un « pacificateur » immunitaire local avec un gène thérapeutique peut améliorer l'efficacité de la thérapie génique chez des sujets dont le système immunitaire est déjà sensibilisé au virus de délivrance. En co-administrant PD-L1 ou PD-L2 directement avec le transgène dans un seul vecteur AAV, les auteurs ont obtenu une expression génique plus forte et plus durable chez des souris pré-immunisées, tout en observant moins d'attaques immunitaires du muscle traité. Bien que de nombreuses questions demeurent — notamment comment équilibrer au mieux les bénéfices et les risques potentiels d'une atténuation de l'immunité, et comment ces résultats se traduiront chez l'humain — ce travail indique une stratégie susceptible d'ouvrir la thérapie génique à un plus grand nombre de patients qui seraient autrement exclus en raison d'une exposition antérieure à l'AAV.
Citation: Käyhty, P., Nieminen, T., Eriksson, R.A.E. et al. The co-delivery of Programmed Death 1 ligands enhances and prolongs rAAV-mediated gene expression in pre-immunized mice. Gene Ther 33, 127–137 (2026). https://doi.org/10.1038/s41434-025-00588-9
Mots-clés: thérapie génique, vecteurs AAV, tolérance immunitaire, point de contrôle PD-1, muscle squelettique