Clear Sky Science · nl
Het gelijktijdig toedienen van Programmed Death 1-liganden versterkt en verlengt rAAV-gemedieerde genexpressie in voorgeïmmuniseerde muizen
Gentherapie werkbaar maken voor meer mensen
Gentherapieën die onschuldige virussen gebruiken om nuttige genen af te leveren, veranderen langzaam de behandeling van erfelijke aandoeningen. Maar bij veel mensen herkent het immuunsysteem deze virussen al, wat ervoor kan zorgen dat de behandeling vervliegt of faalt. Deze studie onderzoekt een manier om de immuunreactie ter plaatse, waar de gentherapie actief is, te "kalmeren", zodat de behandeling langer kan werken en ook patiënten kan helpen die eerder aan deze virussen zijn blootgesteld.
Waarom het immuunsysteem behulpzame virussen aanvalt
De gereedschappen voor gentherapie in deze studie zijn gebaseerd op adeno-geassocieerd virus (AAV), een klein virus dat veel wordt gebruikt om nieuwe genen in cellen te brengen. AAV is over het algemeen veilig en kan jarenlang werkzaam blijven, maar er is een probleem: veel mensen hebben natuurlijke AAV eerder ontmoet. Hun immuunsysteem herinnert zich de viruscapside en kan snel behandelde cellen aanvallen die stukjes van die capsid tonen, waardoor genexpressie stopt. Dit is een specifiek probleem bij spierbehandelingen, die vaak hoge doses vereisen en niet van nature beschermd zijn tegen immuunaanval. Huidige oplossingen — zoals het uitsluiten van patiënten met bestaande antilichamen of het toedienen van brede immunosuppressiva — kunnen patiënten kwetsbaar maken voor infecties en zijn geen ideale langetermijnoplossing.
Een natuurlijke rem op de immuniteit lenen
De onderzoekers richtten zich op een natuurlijke "rem" van het immuunsysteem, het PD-1-pad. In gezonde weefsels helpen PD-1 en zijn partners, PD-L1 en PD-L2, overactieve immuunreacties te voorkomen die het eigen lichaam kunnen beschadigen. Tumoren maken soms gebruik van dit pad om zich te verbergen voor immuuncellen, maar hetzelfde mechanisme kan in principe worden ingezet om gezonde cellen die door gentherapie zijn aangepast te beschermen. Het team ontwierp AAV-vectoren die zowel een rapportergen (een onschadelijk, uitgescheiden enzym genaamd muSEAP, dat gemakkelijk in bloed kan worden gemeten) als PD-L1 of PD-L2 dragen, gekoppeld door een korte zelfknappend peptide waardoor cellen beide eiwitten afzonderlijk uit één genetische cassette kunnen produceren. Ze bevestigden eerst in celculturen dat het "twee-in-één"-ontwerp werkte: zowel het therapeutische schaalmodel als de PD-1-liganden werden correct geproduceerd, biologisch actief en in staat PD-1 te binden.
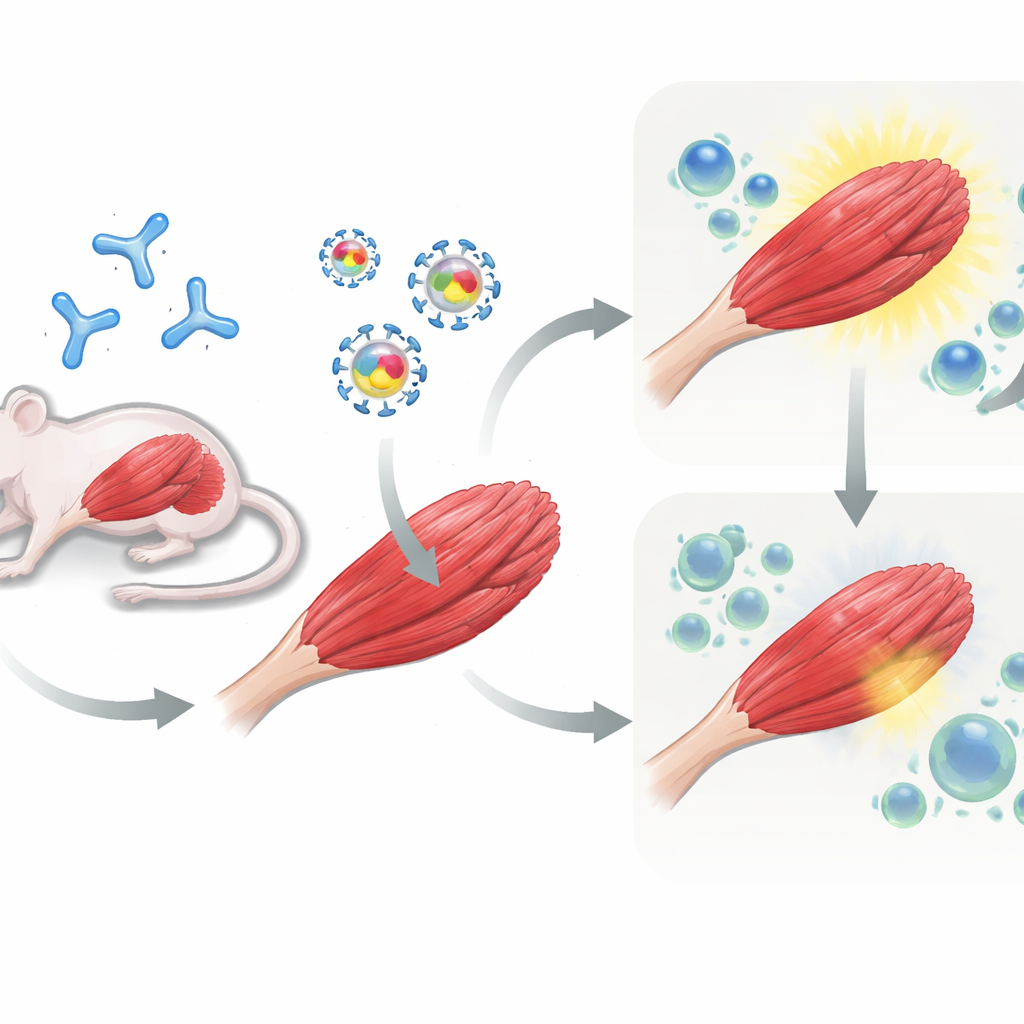
Het testen van de strategie in voorgeïmmuniseerde muizen
Vervolgens ging het team naar muizen. Sommige dieren kregen eerst een AAV-dosis om patiënten na te bootsen die al immuniteit tegen de vector hebben, terwijl andere dieren naïef bleven. Alle muizen kregen daarna gentherapie in hun beenspieren geïnjecteerd: ofwel AAV met alleen muSEAP, of AAV met muSEAP plus PD-L1 of PD-L2. Gedurende enkele weken maten de onderzoekers muSEAP-niveaus in het bloed als maat voor hoe goed het ingevoerde gen werkte. Bij muizen die voorgeïmmuniseerd waren tegen AAV was co-toediening van PD-L1 bijzonder krachtig: muSEAP-niveaus waren veel hoger en bleven tot 12 weken verhoogd vergeleken met de controlevector. PD-L2 verbeterde de expressie ook, zij het in mindere mate en met meer variatie. Daarentegen gaf het toevoegen van PD-L1 of PD-L2 bij naïeve muizen, die AAV nog nooit hadden gezien, geen blijvend voordeel en in sommige gevallen verdwenen vroege winsten in de loop van de tijd.
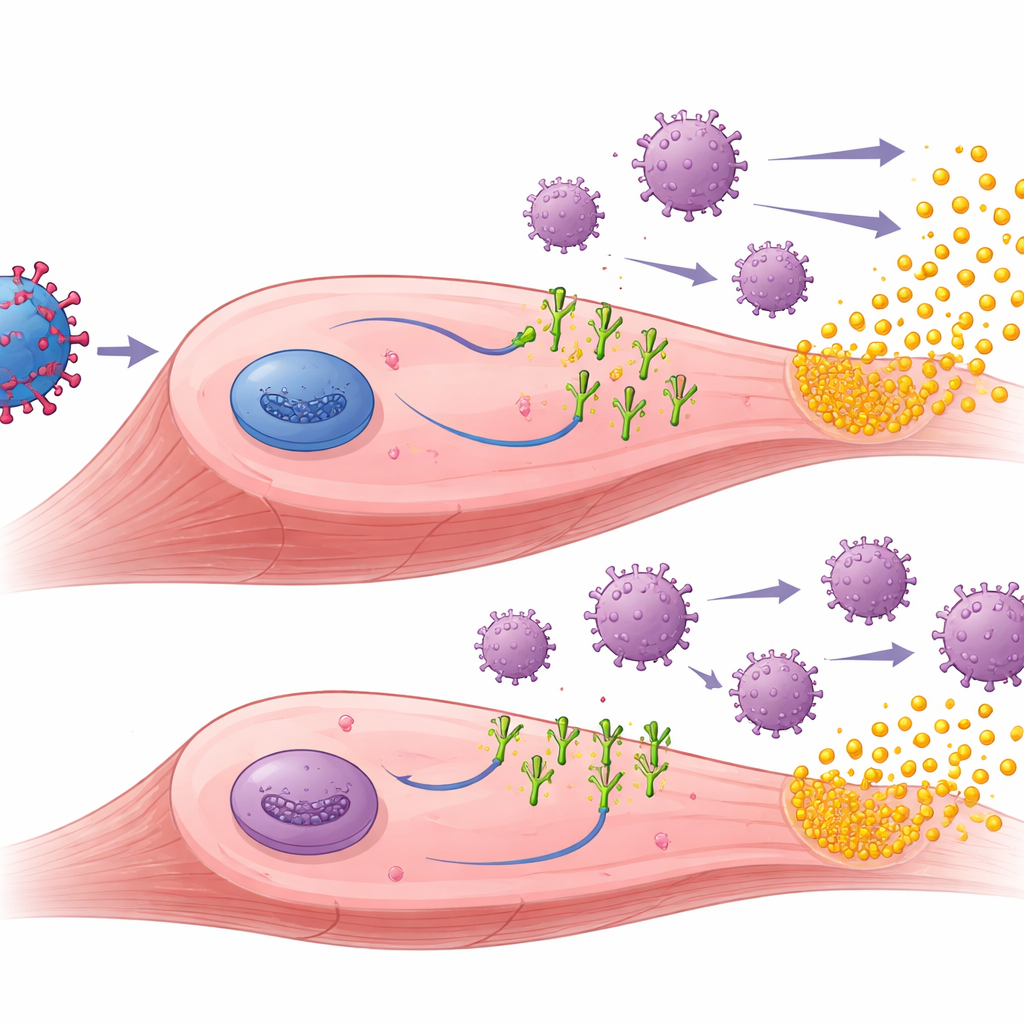
Wat er gebeurt in de behandelde spier
Om te begrijpen waarom de PD-1-liganden hielpen, onderzochten de onderzoekers de behandelde spieren. Ze vonden dat de gentherapie zowel de productie van muSEAP als van de PD-1-liganden in spierweefsel effectief aandreef. In de voorgeïmmuniseerde dieren vertoonden spieren die de PD-L1- of PD-L2-vectoren ontvingen over het algemeen minder binnendringende T-cellen en andere tekenen van ontsteking dan spieren behandeld met alleen muSEAP. Bij deze voorblootgestelde muizen gingen hogere muSEAP-niveaus vaak samen met lagere aantallen immuuncellen, wat suggereert dat lokale inmunsuppressie de behandelde cellen in staat stelde te overleven en langer het therapeutische eiwit te blijven produceren. Het team meet ook antilichamen tegen AAV en tegen de humane PD-1-liganden zelf. Zoals verwacht stegen de AAV-antilichamen na voorimmu¬nisatie en bleven hoog, maar de PD-1-liganden verminderden deze anti-vectorantilichamen niet. Interessant genoeg veroorzaakte alleen PD-L1 detecteerbare anti-ligandantilichamen, en vooral in naïeve muizen, wat wijst op subtiele verschillen in hoe vreemd elk ligand door het immuunsysteem wordt gezien.
Wat dit kan betekenen voor toekomstige behandelingen
In eenvoudige bewoordingen laat deze studie zien dat het verpakken van een lokale immuun-"vredestichter" samen met een therapeutisch gen kan helpen dat gentherapie beter werkt bij proefpersonen waarvan het immuunsysteem al was voorbereid op het bezorgingsvirus. Door PD-L1 of PD-L2 direct samen met het transgen in één AAV-vector mee te leveren, bereikten de auteurs sterkere en langdurigere genexpressie in voorgeïmmuniseerde muizen, terwijl ze ook minder immuuncellen zagen die de behandelde spier aanvielen. Hoewel veel vragen blijven — zoals hoe voordelen het beste kunnen worden afgewogen tegen potentiële risico’s van het dempen van immuniteit, en hoe deze bevindingen naar mensen te vertalen zijn — wijst het werk op een strategie die gentherapie voor een bredere groep patiënten zou kunnen openen die anders uitgesloten zouden worden vanwege eerdere blootstelling aan AAV.
Bronvermelding: Käyhty, P., Nieminen, T., Eriksson, R.A.E. et al. The co-delivery of Programmed Death 1 ligands enhances and prolongs rAAV-mediated gene expression in pre-immunized mice. Gene Ther 33, 127–137 (2026). https://doi.org/10.1038/s41434-025-00588-9
Trefwoorden: gentherapie, AAV-vectoren, immuuntolerantie, PD-1-checkpoint, skelettspier