Clear Sky Science · he
מתן משותף של ליגנדים של PD-1 משפר ומאריך את הביטוי הגנטי המתווך על-ידי rAAV בעכברים עם חיסון מוקדם
להפוך את הטיפול הגנטי לזמין ליותר אנשים
טיפולים גנטיים המשתמשים בווירוסים לא מזיקים כדי להעביר גנים מועילים מתחילים לשנות את אופן הטיפול במחלות תורשתיות. עם זאת, מערכות החיסון של רבים כבר מזהות את הווירוסים הללו, מה שעלול לגרום להיעלמות או לכישלון של הטיפול. מחקר זה בוחן דרך "לרכך" את תגובת המערכת החיסונית במקום שבו הטיפול הגנטי פועל, כך שהטיפול יוכל להמשיך לתקופה ארוכה יותר ולעזור לחולים שנחשפו לווירוסים הללו בעבר.
מדוע המערכת החיסונית תוקפת וירוסים מועילים
כלי הטיפול הגנטי בעבודה זו מבוססים על וירוס adeno-associated (AAV), וירוס קטן הנפוץ לשימוש בהעברתם של גנים לתאים. AAV בדרך כלל בטוח ויכול לפעול למשך שנים, אך יש הסתייגות: רבים כבר נתקלו ב-AAV בטבע. מערכות החיסון שלהם זוכרות את מעטפת הווירוס ועלולות לתקוף במהירות תאים שטופלו ומציגים חלקים מהדגם, ובכך לחתוך את הביטוי הגנטי. זוהי דאגה מיוחדת לטיפולים בשרירים, שלרוב מצריכים מינונים גבוהים ואינם מוגנים באופן טבעי מפני התקפה חיסונית. פתרונות זמניים קיימים — כמו לשלול מטופלים עם נוגדנים קיימים או לתת תרופות מדכאות חיסון רחבות היקף — עלולים להשאיר את המטופלים ללא הגנה מפני זיהומים ואינם אידיאליים לטווח הארוך.
הלוואת בלם טבעי למערכת החיסון
החוקרים פנו ל"בלם" טבעי של המערכת החיסונית שנקרא מסלול PD-1. ברקמות בריאות, PD-1 ושותפיו, PD-L1 ו-PD-L2, מסייעים למנוע התקפות חיסוניות יתר שעלולות לפגוע ברקמה עצמה. גידולים ממאירים מנצלים לעיתים קרובות מסלול זה כדי להתחבא מתאי חיסון, אך מנגנון זה ניתן, בעקרון, לשימוש להגנה על תאים בריאים ששונו על ידי טיפול גנטי. הצוות תיכנן וקטורים של AAV שנושאים גם גן מדווח (אנזים מופרש חסר-פגיעה בשם muSEAP, שניתן למדוד בקלות בדם) וגם PD-L1 או PD-L2, מקושרים על-ידי פפטיד קצר המתנתק בעצמו ומאפשר לתאים לייצר את שני החלבונים בנפרד מקסטת גנים יחידה. הם אימתו תחילה בתרביות תאים שעיצוב ה"שניים-ב-אחד" עבד: גם הסטנד-אין הטיפולי וגם ליגנדי PD-1 יוצרו כראוי, פעילים ביולוגית ובעלי יכולת להיקשר ל-PD-1.
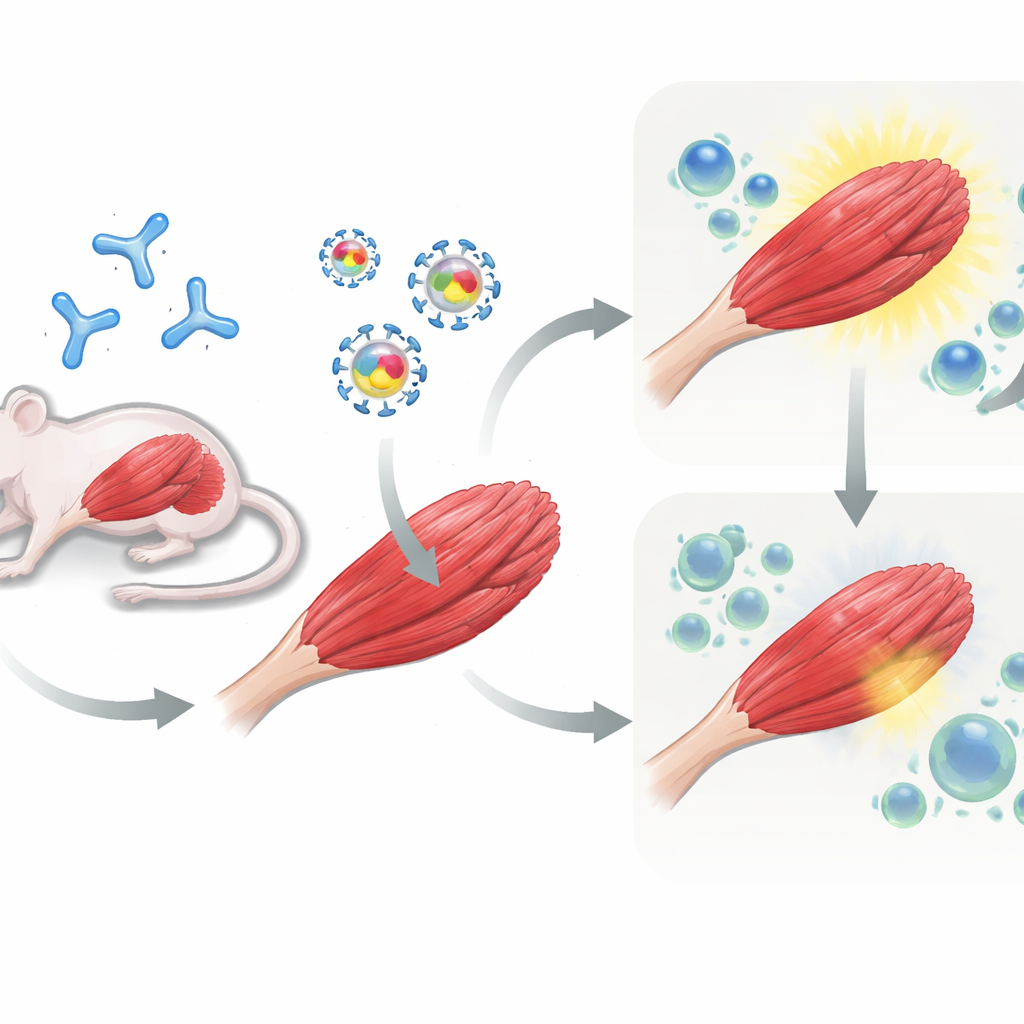
בדיקת האסטרטגיה בעכברים שנחשפו מראש
בהמשך העבירו את המחקר לעכברים. חלק מהחיות קיבלו קודם מנה של AAV כדי לדמות מטופלים שכבר נושאים חיסוניות כלפי הווקטור, בעוד שאחרות נשארו נאיביות. לאחר מכן כל העכברים קיבלו טיפול גנטי שהוזרק לשרירי הרגל: או AAV הנושא muSEAP בלבד, או AAV הנושא muSEAP יחד עם PD-L1 או PD-L2. במשך מספר שבועות מדדו החוקרים את רמות muSEAP בדם כקריאה כמה טוב הגן המוכנס פועל. בעכברים שחוסנו מראש נגד AAV, מתן משותף של PD-L1 היה בעל השפעה מיוחדת: רמות muSEAP היו גבוהות בהרבה ונשמרו גבוהות עד 12 שבועות לעומת הווקטור הביקורת. PD-L2 גם שיפרה את הביטוי, אך במידה פחותה ומשתנה יותר. לעומת זאת, בעכברים נאיביים שמעולם לא נתקלו ב-AAV קודם לכן, הוספת PD-L1 או PD-L2 לא הניבה יתרון מתמשך ובמקרים מסוימים כל רווח מוקדם דעך עם הזמן.
מה קורה בתוך השריר המטופל
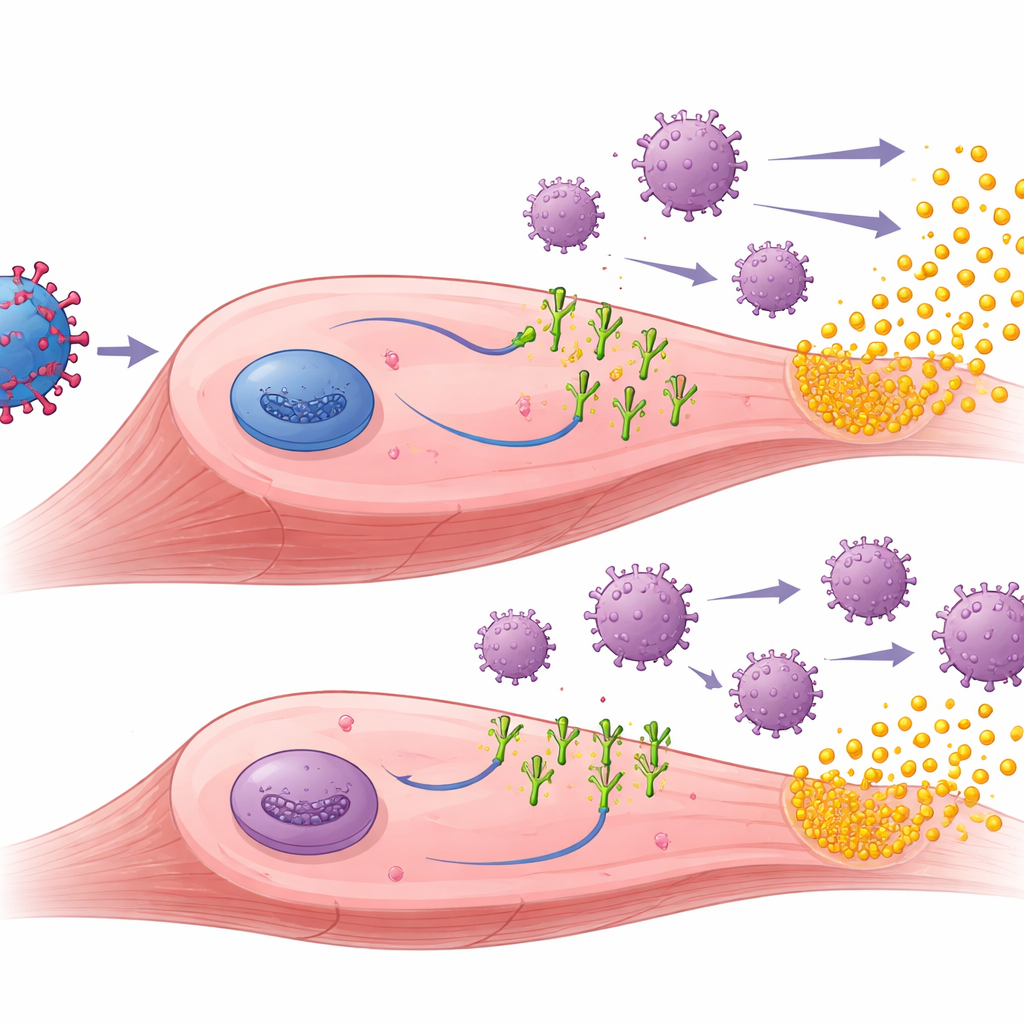
כדי להבין מדוע ליגנדי PD-1 עזרו, החוקרים בחנו את השרירים שטופלו. הם מצאו שטיפול הגנים הוביל בהצלחה לייצור גם של muSEAP וגם של ליגנדי PD-1 ברקמת השריר. בחיות שחוסנו מראש, שרירים שקיבלו את הווקטורים של PD-L1 או PD-L2 הציגו בדרך כלל פחות תאי T פולשים וסימנים אחרים של דלקת לעומת שרירים שטופלו ב-muSEAP בלבד. בעכברים שנחשפו מראש, רמות גבוהות יותר של muSEAP נטו להיברע לצד מספרים נמוכים יותר של תאים חיסוניים, מה שמרמז שהדיכוי החיסוני המקומי אפשר לתאים המטופלים לשרוד ולהמשיך לייצר את החלבון הטיפולי לאורך זמן רב יותר. הצוות גם מדד נוגדנים כנגד AAV ונגד ליגנדי PD-1 האנושיים עצמם. כמצופה, נוגדני AAV עלו לאחר החיסון המוקדם ונשארו גבוהים, אך הליגנדים של PD-1 לא הורידו את נוגדני הנגד-ווקטור הללו. במעניין, רק PD-L1 עורר נוגדני אנטי-ליגנד מדידים, ובמיעוטם בקרב עכברים נאיביים, מרמז על הבדלים עדינים באיך כל ליגנד נתפס כזר על ידי המערכת החיסונית.
מה המשמעות של זה לטיפולים עתידיים
באופן פשוט, מחקר זה מראה שאריזה של "שומר שלום" חיסוני מקומי יחד עם גן טיפולי יכולה לשפר את יעילות הטיפול הגנטי בנבדקים שמערכת החיסון שלהם כבר מוכנה נגד וירוס ההעברה. על-ידי מתן משותף של PD-L1 או PD-L2 ישירות עם הטרנסגן בוקטור AAV יחיד, המחברים השיגו ביטוי גנטי חזק וארוך יותר בעכברים שחוסנו מראש, ובמקביל ראו פחות תאי חיסון תוקפים את השריר המטופל. למרות שעדיין נותרו שאלות רבות — כגון כיצד לאזן בצורה מיטבית את היתרונות עם הסיכונים הפוטנציאליים של דיכוי חיסוני, וכיצד ממצאים אלה יתורגמו לבני אדם — העבודה מצביעה על אסטרטגיה שעשויה לפתוח את הטיפולים הגנטיים לקבוצת מטופלים רחבה יותר שאחרת היו עשויים להיזנח בשל חשיפה מוקדמת ל-AAV.
ציטוט: Käyhty, P., Nieminen, T., Eriksson, R.A.E. et al. The co-delivery of Programmed Death 1 ligands enhances and prolongs rAAV-mediated gene expression in pre-immunized mice. Gene Ther 33, 127–137 (2026). https://doi.org/10.1038/s41434-025-00588-9
מילות מפתח: טיפול גנטי, וקטורי AAV, סבילות חיסונית, צ'קפוינט PD-1, שריר השלד