Clear Sky Science · sv
Ubiquitin‑specifik proteas 26 underlättar endokondral ossifikation genom att driva kondrocyt‑hypertrofi och mineralisering
Hur ben växer och reparerar sig själva
Vårt skelett förändras ständigt. Långa ben i armar och ben bildas först som mjuk brosk som senare omvandlas till hårt ben i en process som kallas endokondral ossifikation. Samma program hjälper brutna ben att läka — men när det går för långt i leder kan det också driva på artros. Denna studie avslöjar en nyckelpassare på molekylär nivå, ett protein kallat USP26, som hjälper broskceller att växa, förkalkas och svara på mekaniska krafter som kroppsvikt och rörelse. Att förstå denna brytpunkt kan öppna nya sätt att främja benläkning samtidigt som ledskador bromsas.
Resan från mjukt brosk till hårt ben
I växande embryon och vid frakturläkning förökar sig specialiserade broskceller, så kallade kondrocyter, först, blir sedan större och hjälper till att avsätta mineral som bildar ben. Forskarna fann att USP26 blir mer rikligt när och där denna övergång sker: i mitten av utvecklande muslemsben, i broskcallus som bygger en läkningsfraktur, och i överväxta broskområden i artrosdrabbade leder. När kondrocyter uppmuntras att mogna i laboratoriet ökar nivåerna av USP26 i takt med klassiska markörer för hypertrofi (cellförstoring) och mineralisering. Dessa mönster tyder på att USP26 fungerar som en accelerator för övergången från brosk till ben. 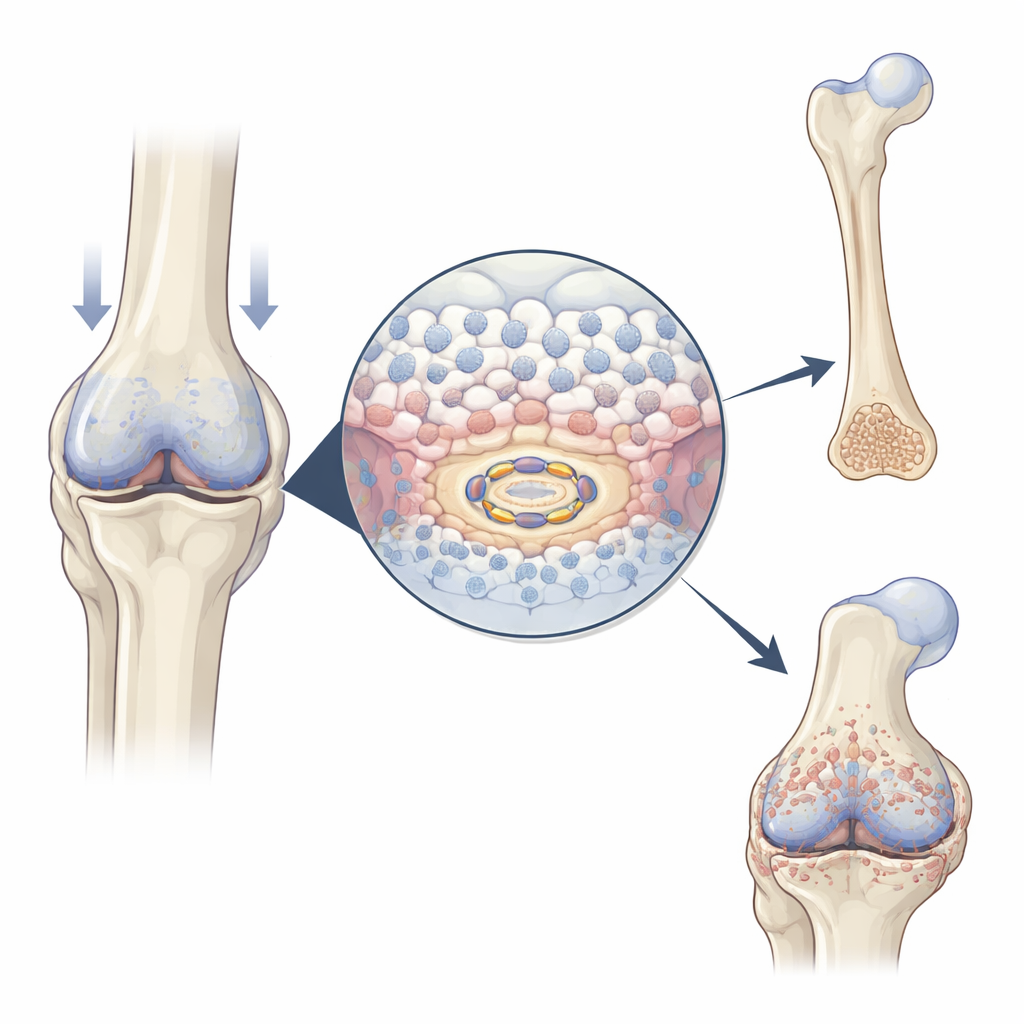
Vad händer när USP26 saknas
För att pröva USP26:s roll konstruerade teamet möss där proteinet tagits bort enbart i kondrocyter. Dessa djur utvecklade kortare lemmar och kotor, vilket speglar hämmad skelettillväxt. Deras tillväxtplattor — zonerna där nytt ben normalt bildas — visade färre förstorade kondrocyter, mindre mineraliserat brosk och minskad uttrycksnivå av nyckelgener som driver benbildning och blodkärlinsväxt. När dessa knock-out‑möss drabbades av lårbensfrakturer innehöll deras callusar mindre brosk och ben, och skanningar visade svagare, mindre mineraliserad reparationsvävnad. Samtidigt skyddade borttagning av USP26 i ledbrosk mot experimentellt framkallad artros: det fanns färre beniga utskott, slätare broskyta och lägre poäng för sjukdomens svårighetsgrad. Tillsammans visar fynden att USP26 är tvåeggad — det behövs för normal tillväxt och reparation, men bidrar också till skadlig benöverväxt i sjuka leder.
Att driva benbildning via cellernas kraftverk
Kondrocyt‑förstoring och mineralisering kräver stora mängder energi. Forskarna upptäckte att USP26 bidrar till att möta detta behov genom att upprätthålla friska mitokondrier, cellens kraftverk. Utan USP26 tog kondrocyter upp mindre glukos, tillverkade mindre ATP (cellens energivaluta) och producerade mindre laktat. Deras mitokondrier var färre, mer fragmenterade och fungerade dåligt, med minskad andningsaktivitet och lägre uttryck av gener inblandade i oxidativ fosforylering. Ett protein kallat FBP2 framträdde som en avgörande länk: i frånvaro av USP26 steg FBP2‑nivåerna kraftigt. FBP2 är känt för att styra celler bort från glukosförbränning och för att hämma mitokondriell biogenes. Här återställde blockering av FBP2 i USP26‑defekta kondrocyter glukosanvändning, mitokondriell massa och energiproduktion, och återupplivade deras förmåga att förstoras och mineraliseras. I artrosmodeller förstärkte också hämning av FBP2 broskets ossifikation, vilket understryker hur balansen mellan USP26 och FBP2 formar benrelaterade utfall. 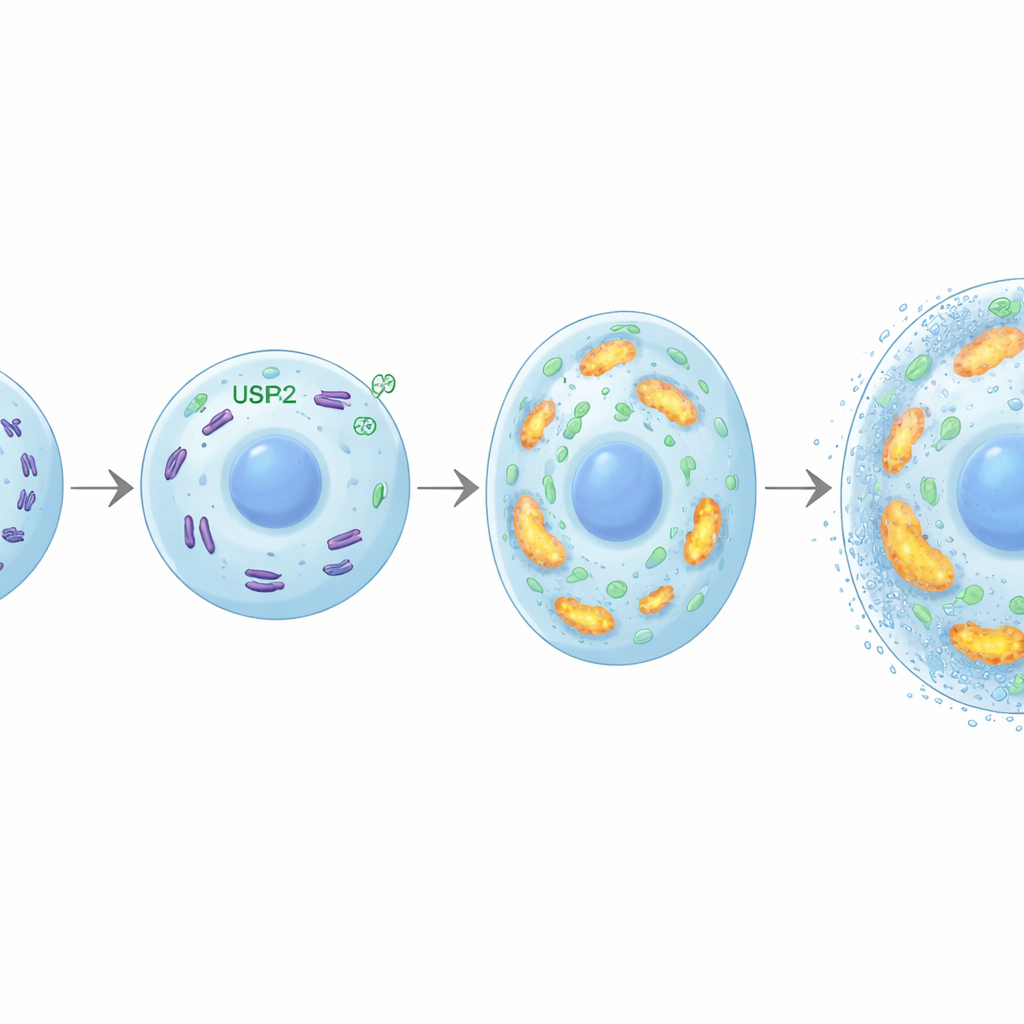
Hur mekaniska krafter slår på USP26
Skelettet känner ständigt av och anpassar sig till mekaniska krafter. Teamet fann att broskzoner under tung belastning — såsom viktbärande områden i artrosdrabbade knän — visar högre nivåer av USP26. I odlade kondrocyter ökade kontrollerad kompression USP26 och samtidigt aktiverade gener som driver hypertrofi och mineralisering. Denna mekaniska signal gick via östrogenreceptor‑α (ER‑α), en hormonkänslig transkriptionsfaktor. Under kompression aktiverades ER‑α genom fosforylering vid en specifik plats (serin 118) och band direkt till en kort DNA‑sekvens i USP26‑genens kontrollregion. Mutera antingen denna DNA‑plats eller fosforyleringsstället på ER‑α dämpade ökningen av USP26, höll kvar högre FBP2‑nivåer och försvagade den metabola och utvecklingsmässiga förskjutningen mot benbildning. Hos möss som tvingades löpa och överbelasta sina knäleder minskade återigen borttagning av USP26 i kondrocyter benöverväxt och broskskada, vilket bekräftar dess roll som en mekanisk ”sensor‑effektor” in vivo.
Varför detta spelar roll för ben och leder
Enkelt uttryckt hjälper USP26 broskceller att omvandla mekanisk belastning och bränsletillgång till benbildande aktivitet. Det gör det genom att sänka FBP2, bevara robusta, energiproducerande mitokondrier och driva kondrocyter mot förstoring och mineralisering. Det gör USP26 avgörande för normal skelettillväxt och effektiv frakturläkning. Men i åldrande eller skadade leder utsatta för kronisk överbelastning tycks samma vägdrift främja förhårdnad och överväxt av brosk som kännetecknar artros. Genom att rikta in sig på USP26 självt eller dess nedströms‑partner FBP2 skulle framtida terapier möjligen kunna selektivt förstärka endokondral ossifikation när vi behöver mer ben — efter trauma eller vid tillväxtrubbningar — samtidigt som man dämpar den i leder i riskzonen för degenerativ sjukdom.
Citering: Li, C., Xu, Y., Zhou, L. et al. Ubiquitin-specific protease 26 facilitates endochondral ossification by driving chondrocyte hypertrophy and mineralization. Bone Res 14, 41 (2026). https://doi.org/10.1038/s41413-026-00517-5
Nyckelord: endokondral ossifikation, kondrocyt‑hypertrofi, mitokondriell metabolism, mekanotransduktion, artros