Clear Sky Science · fr
La protéase spécifique de l’ubiquitine 26 facilite l’ossification endochondrale en stimulant l’hypertrophie et la minéralisation des chondrocytes
Comment les os croissent et se réparent
Notre squelette est en perpétuel changement. Les os longs des bras et des jambes se forment d’abord en cartilage mou, qui se transforme ensuite en os dur dans un processus appelé ossification endochondrale. Le même programme participe à la réparation des fractures — mais quand il s’emballe dans les articulations, il peut aussi alimenter l’arthrose. Cette étude met au jour un commutateur moléculaire clé, une protéine nommée USP26, qui aide les cellules cartilagineuses à croître, se rigidifier et répondre aux forces mécaniques telles que le poids du corps et le mouvement. Comprendre ce commutateur pourrait ouvrir de nouvelles voies pour favoriser la réparation osseuse tout en ralentissant les lésions articulaires.
Le passage du cartilage mou à l’os dur
Chez les embryons en croissance et lors de la cicatrisation des fractures, des cellules cartilagineuses spécialisées appelées chondrocytes se multiplient d’abord, puis s’agrandissent, et enfin participent au dépôt de minéraux pour former de l’os. Les auteurs ont observé que USP26 devient plus abondant précisément quand et où cette transition a lieu : au centre des os des membres en développement chez la souris, dans le cal cartilagineux qui comble une fracture en cours de guérison, et dans les zones de cartilage excédentaire des articulations arthrosiques. Lorsque l’on encourage la maturation des chondrocytes en culture, les niveaux d’USP26 augmentent en parallèle des marqueurs classiques d’hypertrophie (augmentation cellulaire) et de minéralisation. Ces profils suggèrent qu’USP26 agit comme un accélérateur de la transition cartilage→os. 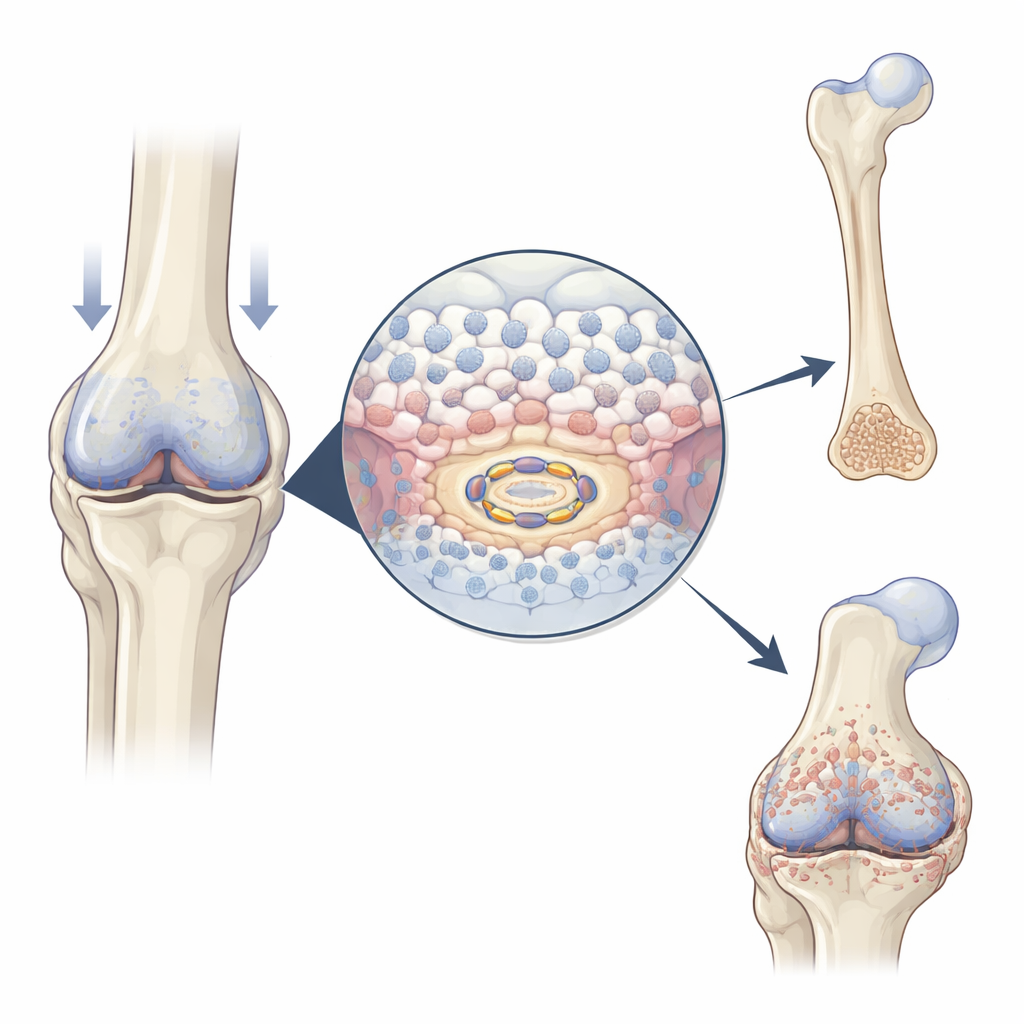
Que se passe-t-il lorsqu’USP26 manque
Pour tester le rôle d’USP26, l’équipe a conçu des souris chez lesquelles cette protéine était supprimée uniquement dans les chondrocytes. Ces animaux ont développé des membres et des vertèbres plus courts, reflétant une croissance squelettique retardée. Leurs plaques de croissance — les zones où l’os neuf est normalement produit — présentaient moins de chondrocytes hypertrophiés, un cartilage moins minéralisé, et une expression réduite de gènes clés qui stimulent la formation osseuse et l’invasion vasculaire. Lorsque ces souris knock-out ont subi des fractures du fémur, leurs cals contenaient moins de cartilage et d’os, et les analyses ont révélé un tissu de réparation plus faible et moins minéralisé. Parallèlement, la suppression d’USP26 dans le cartilage articulaire protégeait contre une arthrose induite expérimentalement : il y avait moins d’excroissances osseuses, des surfaces cartilagineuses plus lisses et des scores de sévérité réduits. Ensemble, ces résultats montrent qu’USP26 est à double tranchant : nécessaire à la croissance et à la réparation normales, mais contribuant aussi à la croissance osseuse néfaste dans les articulations malades.
Alimenter la formation osseuse via les centrales énergétiques cellulaires
L’agrandissement et la minéralisation des chondrocytes exigent de grandes quantités d’énergie. Les chercheurs ont découvert qu’USP26 aide à satisfaire cette demande en maintenant des mitochondries saines, les centrales énergétiques de la cellule. En l’absence d’USP26, les chondrocytes captaient moins de glucose, produisaient moins d’ATP (la monnaie énergétique de la cellule) et généraient moins de lactate. Leurs mitochondries étaient moins nombreuses, plus fragmentées et fonctionnaient mal, avec une activité respiratoire réduite et une expression abaissée des gènes impliqués dans la phosphorylation oxydative. Une protéine nommée FBP2 est apparue comme un maillon crucial : sans USP26, les niveaux de FBP2 augmentaient fortement. FBP2 est connue pour orienter les cellules loin de la consommation de glucose et pour supprimer la biogenèse mitochondriale. Ici, bloquer FBP2 dans des chondrocytes déficients en USP26 a restauré l’utilisation du glucose, la masse mitochondriale et la production d’énergie, et a ravivé leur capacité à s’agrandir et à se minéraliser. Dans des modèles d’arthrose, l’inhibition de FBP2 a également intensifié l’ossification du cartilage, soulignant comment l’équilibre USP26–FBP2 façonne les résultats liés à l’os. 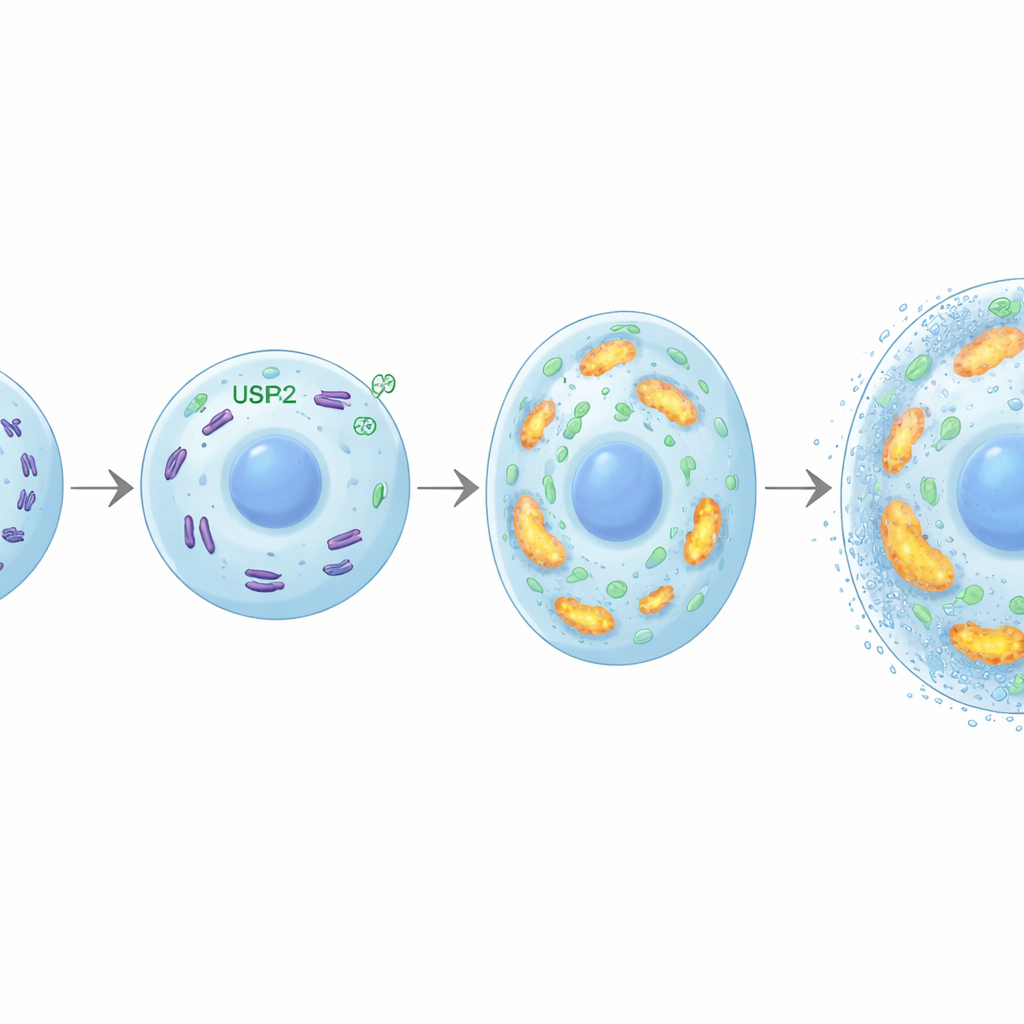
Comment les forces mécaniques activent USP26
Le squelette perçoit et s’adapte en permanence aux forces mécaniques. L’équipe a constaté que les zones de cartilage soumises à de fortes contraintes — comme les régions portantes des genoux arthrosiques — présentent des niveaux plus élevés d’USP26. Dans des chondrocytes en culture, l’application d’une compression contrôlée augmentait USP26 et activait en même temps des gènes promouvant l’hypertrophie et la minéralisation. Ce signal mécanique transitait par le récepteur aux œstrogènes α (ER‑α), un facteur de transcription sensible aux hormones. Sous compression, ER‑α était activé par phosphorylation en un site spécifique (sérine 118) et se liait directement à une courte séquence d’ADN dans la région régulatrice du gène USP26. La mutation de ce site d’ADN ou du site de phosphorylation sur ER‑α atténuait la montée d’USP26, préservait des niveaux plus élevés de FBP2 et affaiblissait la bascule métabolique et développementale vers la formation osseuse. Chez des souris forcées à courir et à surcharger leurs articulations du genou, la suppression d’USP26 dans les chondrocytes réduisait de nouveau la croissance osseuse excessive et les lésions cartilagineuses, confirmant son rôle de « capteur‑effecteur » mécanique in vivo.
Pourquoi cela compte pour les os et les articulations
En résumé, USP26 aide les cellules cartilagineuses à convertir la charge mécanique et l’approvisionnement en carburant en activité constructrice d’os. Il le fait en abaissant FBP2, en préservant des mitochondries robustes et productrices d’énergie, et en poussant les chondrocytes vers l’hypertrophie et la minéralisation. Cela rend USP26 essentiel à la croissance squelettique normale et à une bonne guérison des fractures. Mais dans les articulations vieillissantes ou blessées exposées à une surcharge chronique, la même voie semble entraîner le durcissement et la croissance excessive du cartilage caractéristiques de l’arthrose. En ciblant USP26 lui‑même, ou son partenaire en aval FBP2, des thérapies futures pourraient un jour amplifier sélectivement l’ossification endochondrale quand nous avons besoin de plus d’os — après un traumatisme ou pour des troubles de croissance — tout en la réduisant dans les articulations à risque de maladie dégénérative.
Citation: Li, C., Xu, Y., Zhou, L. et al. Ubiquitin-specific protease 26 facilitates endochondral ossification by driving chondrocyte hypertrophy and mineralization. Bone Res 14, 41 (2026). https://doi.org/10.1038/s41413-026-00517-5
Mots-clés: ossification endochondrale, hypertrophie des chondrocytes, métabolisme mitochondrial, <keyword>arthrose