Clear Sky Science · de
Ubiquitin-spezifische Protease 26 fördert die enchondrale Ossifikation, indem sie Chondrozytenhypertrophie und Mineralisierung antreibt
Wie Knochen wachsen und sich selbst reparieren
Unser Skelett verändert sich ständig. Lange Knochen in Armen und Beinen entstehen zunächst als weicher Knorpel, der später in einem Prozess namens enchondrale Ossifikation zu hartem Knochen umgebaut wird. Dasselbe Programm hilft auch bei der Heilung von Knochenbrüchen – läuft es in Gelenken jedoch zu stark ab, kann es zur Entstehung von Arthrose beitragen. Diese Studie deckt einen wichtigen molekularen Schalter auf, ein Protein namens USP26, das Knorpelzellen dabei unterstützt, zu wachsen, zu verhärten und auf mechanische Kräfte wie Körpergewicht und Bewegung zu reagieren. Das Verständnis dieses Schalters könnte neue Wege eröffnen, die Knochenreparatur zu fördern und gleichzeitig Gelenkschäden zu verlangsamen.
Der Weg vom weichen Knorpel zum harten Knochen
In wachsenden Embryonen und bei der Heilung von Frakturen vermehren sich spezialisierte Knorpelzellen, die Chondrozyten genannt werden, zunächst, vergrößern sich dann und tragen schließlich durch Mineralablagerung zur Knochenbildung bei. Die Autoren fanden heraus, dass USP26 genau dann und dort stärker vorhanden ist, wo dieser Übergang stattfindet: in der Mitte sich entwickelnder Mäuse-Gliedmaßenknochen, im knorpeligen Kallus, der eine heilende Fraktur überbrückt, und in überwucherten Knorpelbereichen bei arthrotischen Gelenken. Wenn Chondrozyten im Labor zur Reifung angeregt wurden, stiegen die USP26-Spiegel parallel zu klassischen Markern der Hypertrophie (Zellvergrößerung) und Mineralisierung an. Diese Muster deuten darauf hin, dass USP26 als Beschleuniger des Knorpel-zu-Knochen-Übergangs wirkt. 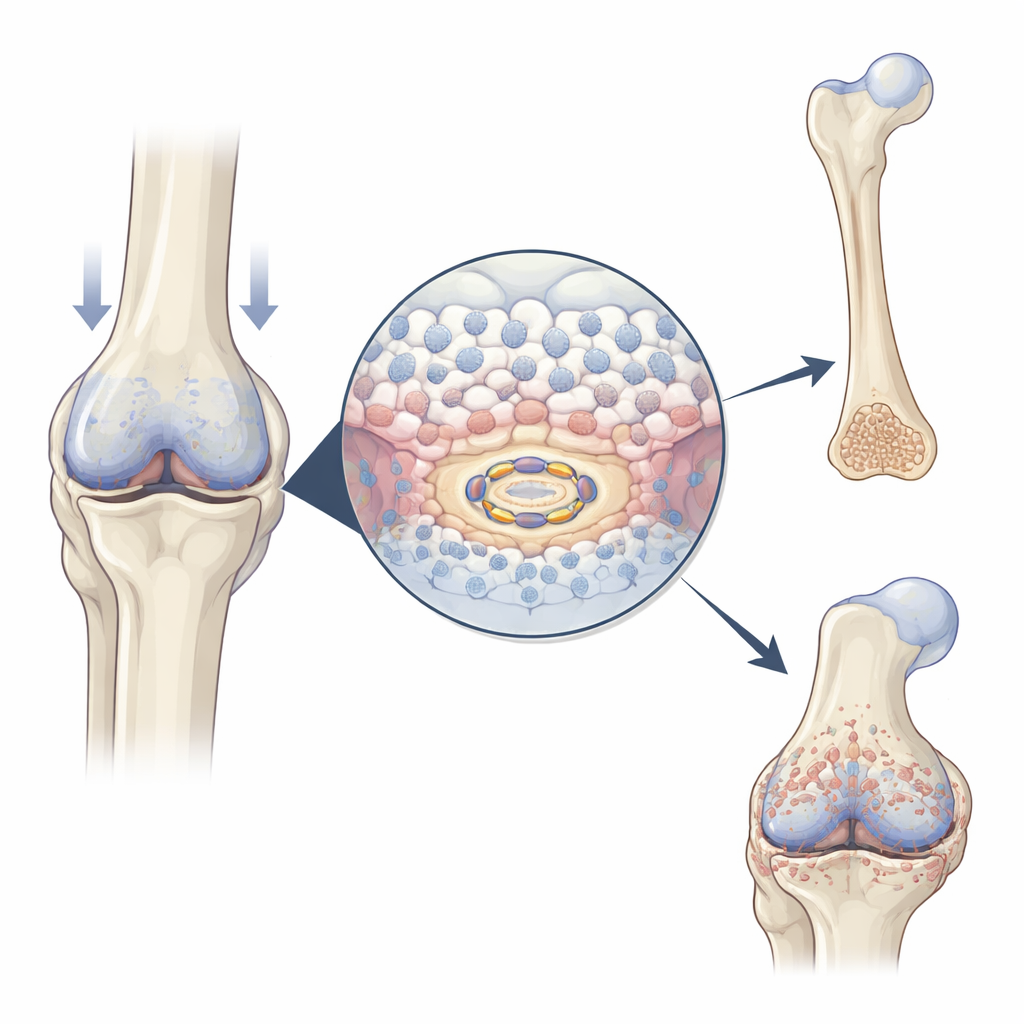
Was passiert, wenn USP26 fehlt
Um die Rolle von USP26 zu prüfen, erzeugte das Team Mäuse, bei denen dieses Protein ausschließlich in Chondrozyten entfernt wurde. Diese Tiere entwickelten kürzere Gliedmaßen und Wirbel, was auf ein verzögertes Skelettwachstum hinweist. Ihre Wachstumsfugen – die Zonen, in denen normalerweise neuer Knochen gebildet wird – zeigten weniger vergrößerte Chondrozyten, weniger mineralisierten Knorpel und eine verringerte Expression wichtiger Gene, die die Knochenbildung und das Einwachsen von Blutgefäßen steuern. Als diese Knockout-Mäuse Oberschenkelbruch erlitten, enthielten ihre Kallusse weniger Knorpel und Knochen, und Bildgebungen zeigten schwächere, weniger mineralisierte Reparaturgewebe. Gleichzeitig schützte das Entfernen von USP26 aus dem Gelenkknorpel vor experimentell induzierter Arthrose: Es bildeten sich weniger Knochenwucherungen, die Knorpeloberflächen blieben glatter und die Krankheitsbewertungen waren niedriger. Zusammengenommen zeigen die Befunde, dass USP26 eine zweischneidige Rolle hat – es ist für normales Wachstum und Reparatur notwendig, trägt aber zugleich zu schädlichem Knochenüberwuchs in erkrankten Gelenken bei.
Die Knochenbildung über zelluläre Kraftwerke ankurbeln
Die Vergrößerung der Chondrozyten und die Mineralisierung verlangen große Energiemengen. Die Forscher entdeckten, dass USP26 dazu beiträgt, diesen Bedarf zu decken, indem es gesunde Mitochondrien – die Kraftwerke der Zelle – erhält. Ohne USP26 nahmen Chondrozyten weniger Glukose auf, produzierten weniger ATP (die Energieeinheit der Zelle) und weniger Laktat. Ihre Mitochondrien waren weniger zahlreich, stärker fragmentiert und funktionierten schlecht, mit verringerter Atmungsaktivität und geringerer Expression von Genen der oxidativen Phosphorylierung. Ein Protein namens FBP2 erwies sich als entscheidende Verbindung: In Abwesenheit von USP26 stiegen die FBP2-Spiegel stark an. FBP2 ist dafür bekannt, Zellen vom Glukoseabbau wegzulenken und die mitochondriale Biogenese zu unterdrücken. Hier stellte das Blockieren von FBP2 in USP26-defizienten Chondrozyten die Glukosenutzung, die mitochondriale Masse und die Energieproduktion wieder her und belebte ihre Fähigkeit zur Vergrößerung und Mineralisierung. In Arthrosemodellen verstärkte die Hemmung von FBP2 ebenfalls die Knorpelossifikation, was die Bedeutung des USP26–FBP2-Gleichgewichts für knochenbezogene Ergebnisse unterstreicht. 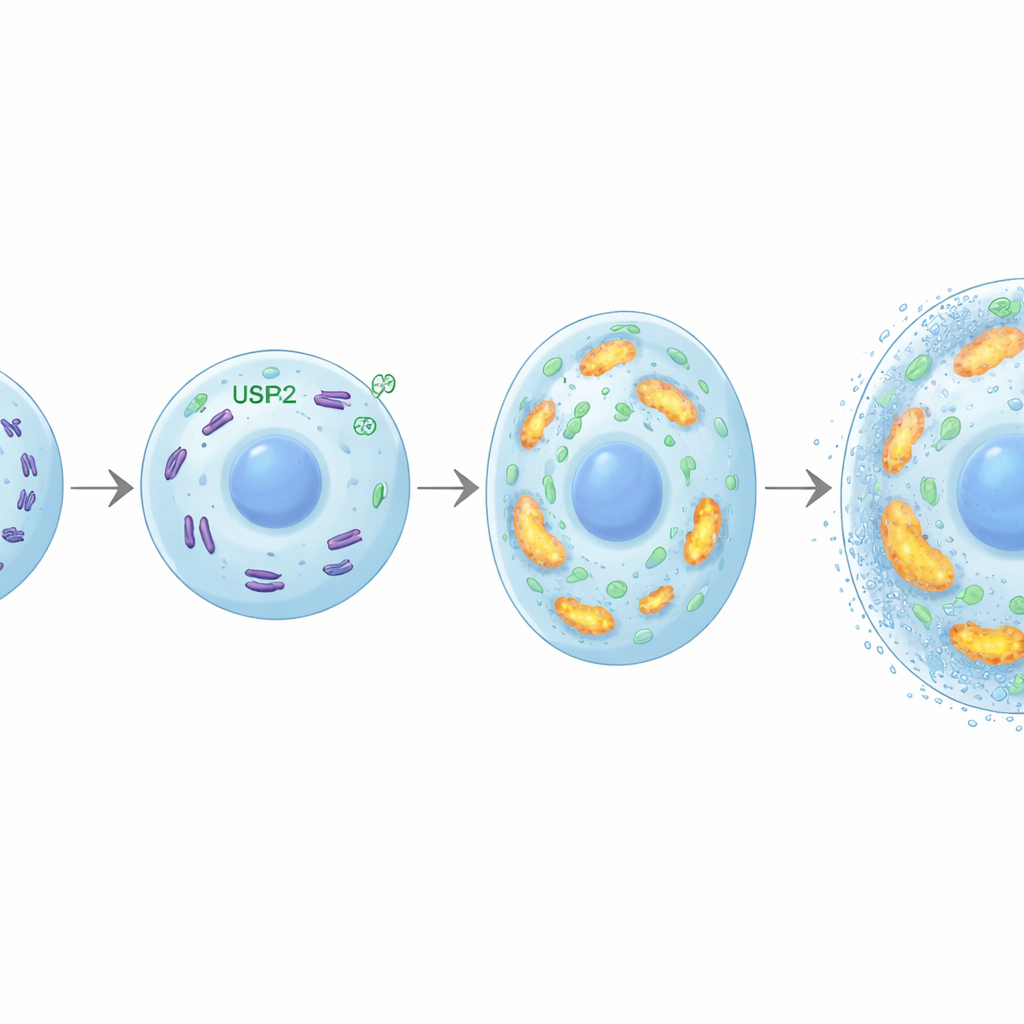
Wie mechanische Kräfte USP26 einschalten
Das Skelett nimmt mechanische Kräfte ständig wahr und passt sich ihnen an. Das Team fand heraus, dass Knorpelzonen unter starker Belastung – etwa tragende Bereiche in arthritischen Knien – höhere USP26-Spiegel aufweisen. In kultivierten Chondrozyten führte kontrollierte Kompression zu einem Anstieg von USP26 und aktiviert gleichzeitig Gene, die Hypertrophie und Mineralisierung vorantreiben. Dieses mechanische Signal wurde über den Östrogenrezeptor‑α (ER‑α) vermittelt, einen hormonabhängigen Transkriptionsfaktor. Unter Kompression wurde ER‑α durch Phosphorylierung an einer spezifischen Stelle (Serin 118) aktiviert und band sich direkt an eine kurze DNA-Sequenz in der Kontrollregion des USP26-Gens. Die Mutation entweder dieser DNA-Stelle oder der Phosphorylierungsstelle auf ER‑α schwächte den Anstieg von USP26 ab, ließ höhere FBP2-Spiegel bestehen und verringerte die metabolische und entwicklungsbiologische Umstellung in Richtung Knochenbildung. In Mäusen, die zum Laufen gezwungen wurden und so ihre Kniegelenke überlasteten, reduzierte die Deletion von USP26 in Chondrozyten erneut den Knochenüberwuchs und den Knorpelschaden, was seine Rolle als mechanischen „Sensor–Effektor“ in vivo bestätigt.
Warum das für Knochen und Gelenke wichtig ist
Kurz gesagt hilft USP26 Knorpelzellen dabei, mechanische Belastung und Energiezufuhr in knochenbildende Aktivität umzusetzen. Dies geschieht, indem FBP2 gesenkt, robuste energieproduzierende Mitochondrien erhalten und Chondrozyten in Richtung Vergrößerung und Mineralisierung gedrängt werden. Damit ist USP26 essenziell für normales Skelettwachstum und eine effektive Frakturheilung. In alternden oder verletzten Gelenken, die chronischer Überbelastung ausgesetzt sind, scheint derselbe Weg jedoch die Verhärtung und den Überwuchs von Knorpel zu fördern, die für Arthrose charakteristisch sind. Durch gezieltes Eingreifen in USP26 selbst oder seinem nachgeschalteten Partner FBP2 könnten zukünftige Therapien möglicherweise die enchondrale Ossifikation selektiv verstärken, wenn mehr Knochen benötigt wird – nach Traumata oder bei Wachstumsstörungen – und sie gleichzeitig in gefährdeten Gelenken abschwächen, um degenerativen Erkrankungen vorzubeugen.
Zitation: Li, C., Xu, Y., Zhou, L. et al. Ubiquitin-specific protease 26 facilitates endochondral ossification by driving chondrocyte hypertrophy and mineralization. Bone Res 14, 41 (2026). https://doi.org/10.1038/s41413-026-00517-5
Schlüsselwörter: enchondrale Ossifikation, Chondrozytenhypertrophie, mitochondrialer Stoffwechsel, Mechanotransduktion, Arthrose