Clear Sky Science · pt
Protease específica de ubiquitina 26 facilita a ossificação endocondral ao promover hipertrofia e mineralização de condrócitos
Como os ossos crescem e se regeneram
Nosso esqueleto está em constante transformação. Os ossos longos dos braços e das pernas se formam inicialmente como cartilagem macia, que depois se converte em osso duro através de um processo chamado ossificação endocondral. O mesmo programa auxilia a cicatrização de fraturas — mas quando é excessivamente ativado nas articulações, também pode alimentar a osteoartrite. Este estudo revela um interruptor molecular chave, uma proteína chamada USP26, que ajuda as células da cartilagem a crescer, se endurecer e responder a forças mecânicas, como o peso corporal e o movimento. Compreender esse interruptor pode abrir novas estratégias para estimular a reparação óssea e, ao mesmo tempo, retardar os danos articulares.
A jornada da cartilagem macia ao osso duro
Em embriões em crescimento e na reparação de fraturas, células cartilaginosas especializadas conhecidas como condrócitos primeiro se multiplicam, depois se tornam maiores e finalmente ajudam a depositar minerais para formar osso. Os autores observaram que USP26 se torna mais abundante precisamente quando e onde essa transição ocorre: no centro dos ossos em desenvolvimento nos membros de camundongos, no calo cartilaginoso que une uma fratura em cicatrização e em áreas de cartilagem hipertrofiada em articulações com osteoartrite. Quando os condrócitos são estimulados a maturar em cultura, os níveis de USP26 aumentam em paralelo com marcadores clássicos de hipertrofia (aumento celular) e mineralização. Esses padrões sugerem que USP26 atua como um acelerador da transição cartilagem–osso. 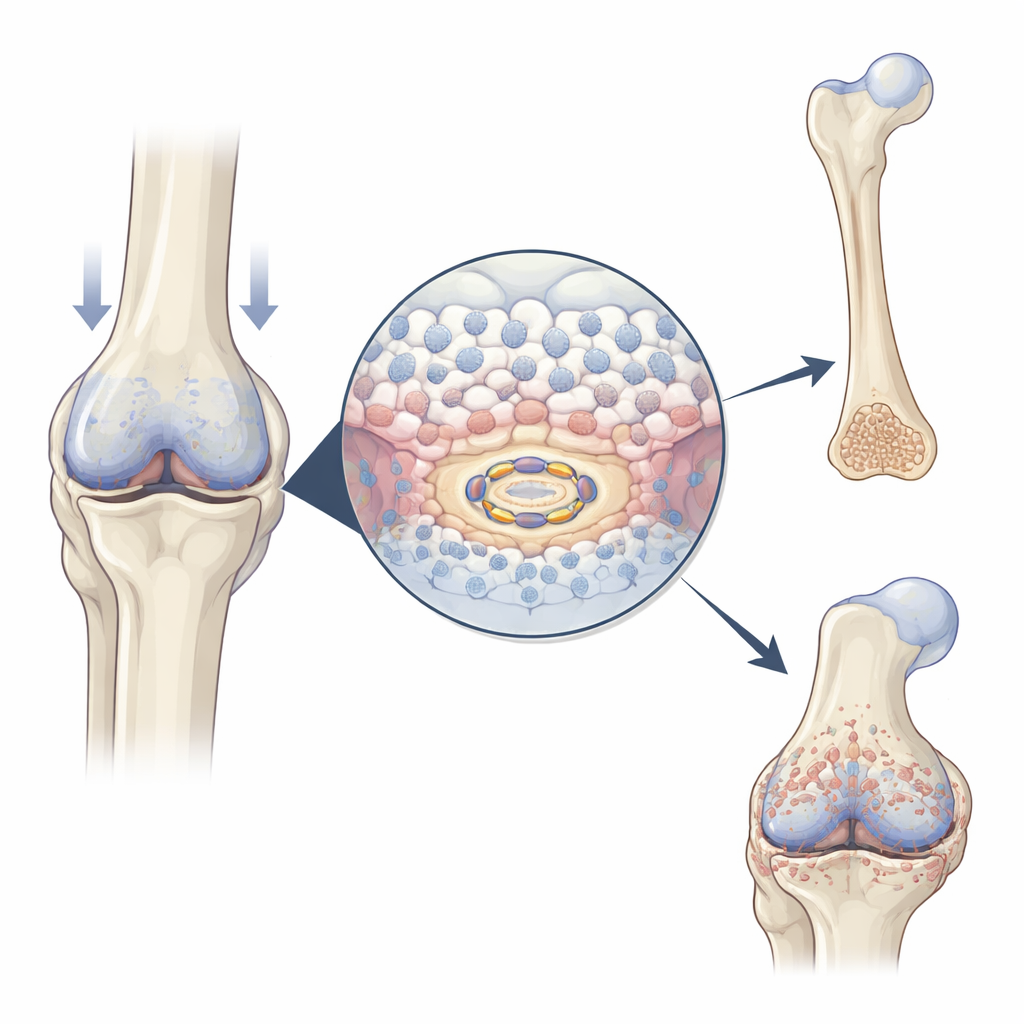
O que acontece quando USP26 está ausente
Para testar o papel de USP26, a equipe desenvolveu camundongos nos quais essa proteína foi removida apenas dos condrócitos. Esses animais apresentaram membros e vértebras mais curtos, refletindo crescimento esquelético comprometido. Suas placas de crescimento — as zonas onde o novo osso normalmente se forma — exibiram menos condrócitos aumentados, cartilagem menos mineralizada e expressão reduzida de genes-chave que impulsionam a formação óssea e a invasão vascular. Quando esses camundongos nocaute sofreram fraturas no fêmur, seus calos continham menos cartilagem e osso, e exames revelaram tecido de reparo mais fraco e menos mineralizado. Ao mesmo tempo, a remoção de USP26 da cartilagem articular protegeu contra osteoartrite induzida experimentalmente: houve menos esporões ósseos, superfícies cartilaginosas mais lisas e escores de severidade da doença menores. Em conjunto, os achados mostram que USP26 tem dois gumes — é necessário para crescimento e reparo normais, mas também contribui para o crescimento ósseo prejudicial em articulações doentes.
Alimentando a formação óssea por meio das usinas energéticas celulares
O aumento e a mineralização dos condrócitos exigem grandes quantidades de energia. Os pesquisadores descobriram que USP26 ajuda a suprir essa demanda ao manter mitocôndrias saudáveis, as usinas energéticas da célula. Na ausência de USP26, os condrócitos captaram menos glicose, produziram menos ATP (a moeda energética celular) e geraram menos lactato. Suas mitocôndrias eram em menor número, mais fragmentadas e funcionavam mal, com atividade respiratória reduzida e expressão diminuída de genes envolvidos na fosforilação oxidativa. Uma proteína chamada FBP2 emergiu como um elo crucial: na ausência de USP26, os níveis de FBP2 aumentaram fortemente. Sabe‑se que FBP2 direciona as células a consumir menos glicose e suprime a biogênese mitocondrial. Aqui, bloquear FBP2 em condrócitos deficientes em USP26 restaurou o uso de glicose, a massa mitocondrial e a produção de energia, e reativou sua capacidade de aumentar e mineralizar. Em modelos de osteoartrite, inibir FBP2 também intensificou a ossificação da cartilagem, ressaltando como o equilíbrio USP26–FBP2 molda os desfechos relacionados ao osso. 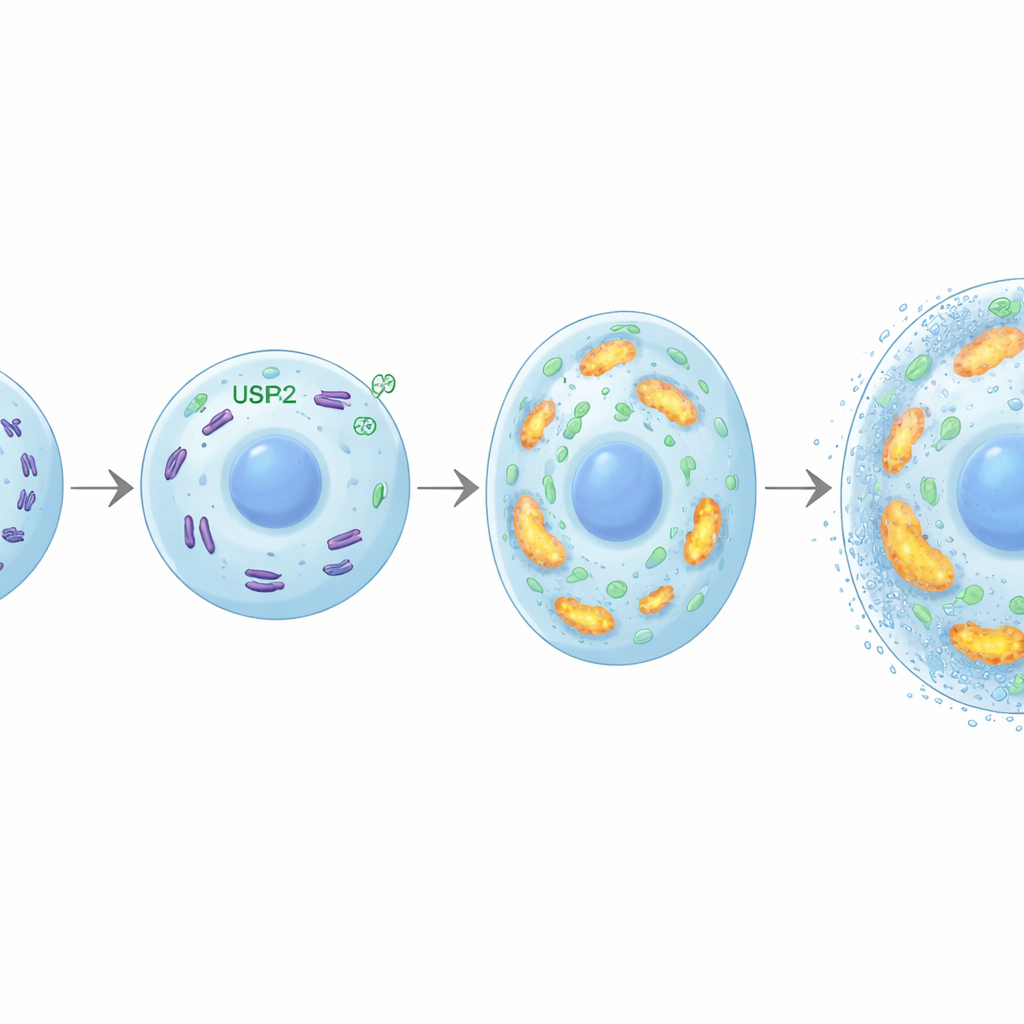
Como forças mecânicas ligam o USP26
O esqueleto está constantemente sensível e adaptando‑se às forças mecânicas. A equipe constatou que zonas de cartilagem submetidas a carga elevada — como áreas de suporte de peso em joelhos artríticos — apresentam níveis maiores de USP26. Em condrócitos em cultura, a aplicação de compressão controlada aumentou USP26 e simultaneamente ativou genes que impulsionam a hipertrofia e a mineralização. Esse sinal mecânico transitou pela receptora de estrogênio‑α (ER‑α), um fator de transcrição sensível a hormônios. Sob compressão, ER‑α foi ativada por fosforilação em um sítio específico (serina 118) e ligou‑se diretamente a uma curta sequência de DNA na região reguladora do gene USP26. Mutar esse sítio de DNA ou o sítio de fosforilação em ER‑α atenuou o aumento de USP26, preservou níveis mais altos de FBP2 e enfraqueceu a mudança metabólica e de desenvolvimento rumo à formação óssea. Em camundongos forçados a correr e sobrecarregar suas articulações do joelho, a deleção de USP26 nos condrócitos novamente reduziu o crescimento ósseo excessivo e os danos cartilaginosos, confirmando seu papel como um “sensor‑efetor” mecânico in vivo.
Por que isso importa para ossos e articulações
Em termos simples, USP26 ajuda as células da cartilagem a converter carga mecânica e suprimento de combustível em atividade construtora de osso. Faz isso reduzindo FBP2, preservando mitocôndrias robustas e produtoras de energia, e impulsionando os condrócitos em direção à hipertrofia e à mineralização. Isso torna USP26 essencial para crescimento esquelético normal e para a cicatrização eficaz de fraturas. Mas, em articulações envelhecidas ou lesionadas expostas a sobrecarga crônica, a mesma via parece promover o endurecimento e o crescimento excessivo da cartilagem característicos da osteoartrite. Ao mirar USP26 em si ou seu parceiro a jusante FBP2, terapias futuras podem algum dia amplificar seletivamente a ossificação endocondral quando precisarmos de mais osso — após trauma ou em distúrbios do crescimento — ao mesmo tempo em que a reduzem em articulações em risco de doença degenerativa.
Citação: Li, C., Xu, Y., Zhou, L. et al. Ubiquitin-specific protease 26 facilitates endochondral ossification by driving chondrocyte hypertrophy and mineralization. Bone Res 14, 41 (2026). https://doi.org/10.1038/s41413-026-00517-5
Palavras-chave: ossificação endocondral, hipertrofia de condrócitos, metabolismo mitocondrial, mecanotransdução, osteoartrite