Clear Sky Science · nl
Ubiquitine‑specifieke protease 26 bevordert endochondrale ossificatie door chondrocyt‑hypertrofie en mineralisatie te stimuleren
Hoe botten groeien en zichzelf herstellen
Ons skelet is voortdurend in verandering. Lange botten in armen en benen ontstaan eerst als zacht kraakbeen, dat later in hard bot verandert in een proces dat endochondrale ossificatie wordt genoemd. Datzelfde programma helpt ook bij het genezen van botbreuken — maar als het te sterk in gewrichten wordt geactiveerd, kan het ook bijdragen aan artrose. Deze studie onthult een belangrijke moleculaire schakelaar, een eiwit genaamd USP26, dat kraakbeencellen helpt groeien, verharden en reageren op mechanische krachten zoals lichaamsgewicht en beweging. Inzicht in deze schakelaar kan nieuwe mogelijkheden openen om botherstel te bevorderen en tegelijkertijd gewrichtsschade te vertragen.
De reis van zacht kraakbeen naar hard bot
Bij zich ontwikkelende embryo’s en bij het helen van fracturen delen gespecialiseerde kraakbeencellen, chondrocyten, zich eerst, vergroten ze vervolgens en helpen ze uiteindelijk bij het aanleggen van mineralen om bot te vormen. De auteurs vonden dat USP26 precies op het juiste moment en op de juiste plaats toeneemt: in het midden van zich ontwikkelende muisledematen, in de kraakbeenslagader (callus) die een helende breuk overbrugt, en in overgroeide kraakbeengebieden in artritische gewrichten. Wanneer chondrocyten in het laboratorium worden gestimuleerd om te rijpen, stijgt USP26 in overeenstemming met klassieke markers van hypertrofie (celvergroting) en mineralisatie. Deze patronen suggereren dat USP26 fungeert als een versneller van de overgang van kraakbeen naar bot. 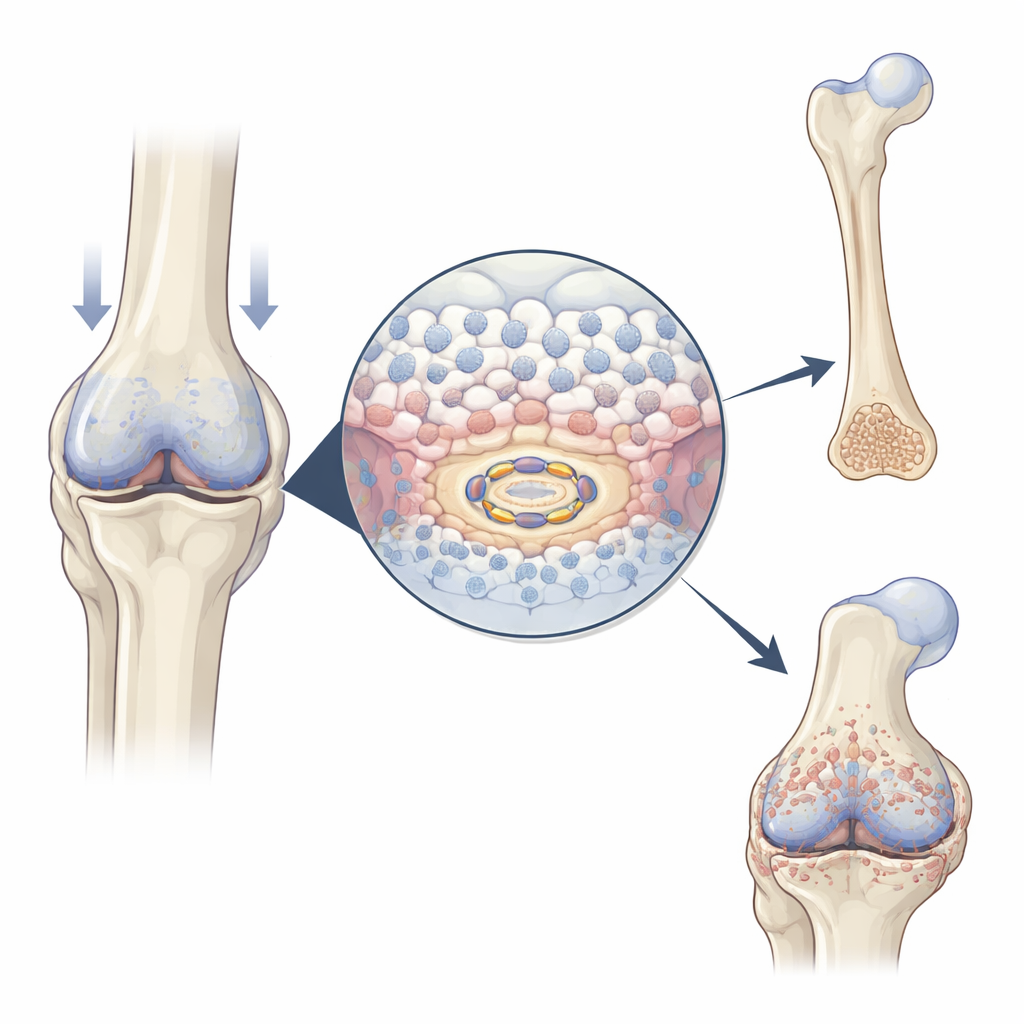
Wat er gebeurt als USP26 ontbreekt
Om de rol van USP26 te testen, maakten de onderzoekers muizen waarbij dit eiwit alleen uit chondrocyten werd verwijderd. Deze dieren ontwikkelden kortere ledematen en wervels, wat wijst op geremde skeletgroei. Hun groeischijven — de zones waar normaal nieuw bot wordt gevormd — vertoonden minder vergrote chondrocyten, minder gemineraliseerd kraakbeen en verminderde expressie van sleutelgenen die botvorming en binnendringing van bloedvaten aansturen. Wanneer deze knock‑outmuizen femurfracturen kregen, bevatte hun callus minder kraakbeen en bot, en scans toonden zwakker, minder gemineraliseerd herstelweefsel. Tegelijkertijd beschermde het verwijderen van USP26 uit gewrichtskraakbeen tegen experimenteel geïnduceerde artrose: er waren minder benige uitsteeksels, gladdere kraakbeenoppervlakken en lagere scores voor ziekte‑ernst. Gezamenlijk tonen de bevindingen dat USP26 een dubbelzijdig effect heeft — het is nodig voor normale groei en herstel, maar het draagt ook bij aan schadelijke botovergroei in zieke gewrichten.
Botvorming aansturen via cellulaire energiecentrales
Chondrocytvergroting en mineralisatie vragen om grote hoeveelheden energie. De onderzoekers ontdekten dat USP26 helpt aan die vraag te voldoen door gezonde mitochondriën te behouden, de energiecentrales van de cel. Zonder USP26 namen chondrocyten minder glucose op, maakten ze minder ATP (de energievaluta van de cel) en produceerden ze minder lactaat. Hun mitochondriën waren talrijker afgenomen, meer gefragmenteerd en functioneerden slecht, met verminderde respiratoire activiteit en lagere expressie van genen betrokken bij oxidatieve fosforylering. Een eiwit genaamd FBP2 kwam naar voren als een cruciale schakel: bij afwezigheid van USP26 stegen FBP2‑niveaus sterk. Van FBP2 is bekend dat het cellen afschuift van het verbranden van glucose en mitochondriale biogenese onderdrukt. Hierher leidde het blokkeren van FBP2 in USP26‑deficiënte chondrocyten tot herstel van glucosegebruik, mitochondriale massa en energieproductie, en herstelde het hun vermogen om te vergroten en te mineraliseren. In artrosemodellen verscherpte het remmen van FBP2 eveneens de kraakbeenossificatie, wat onderstreept hoe de balans tussen USP26 en FBP2 botgerelateerde uitkomsten bepaalt. 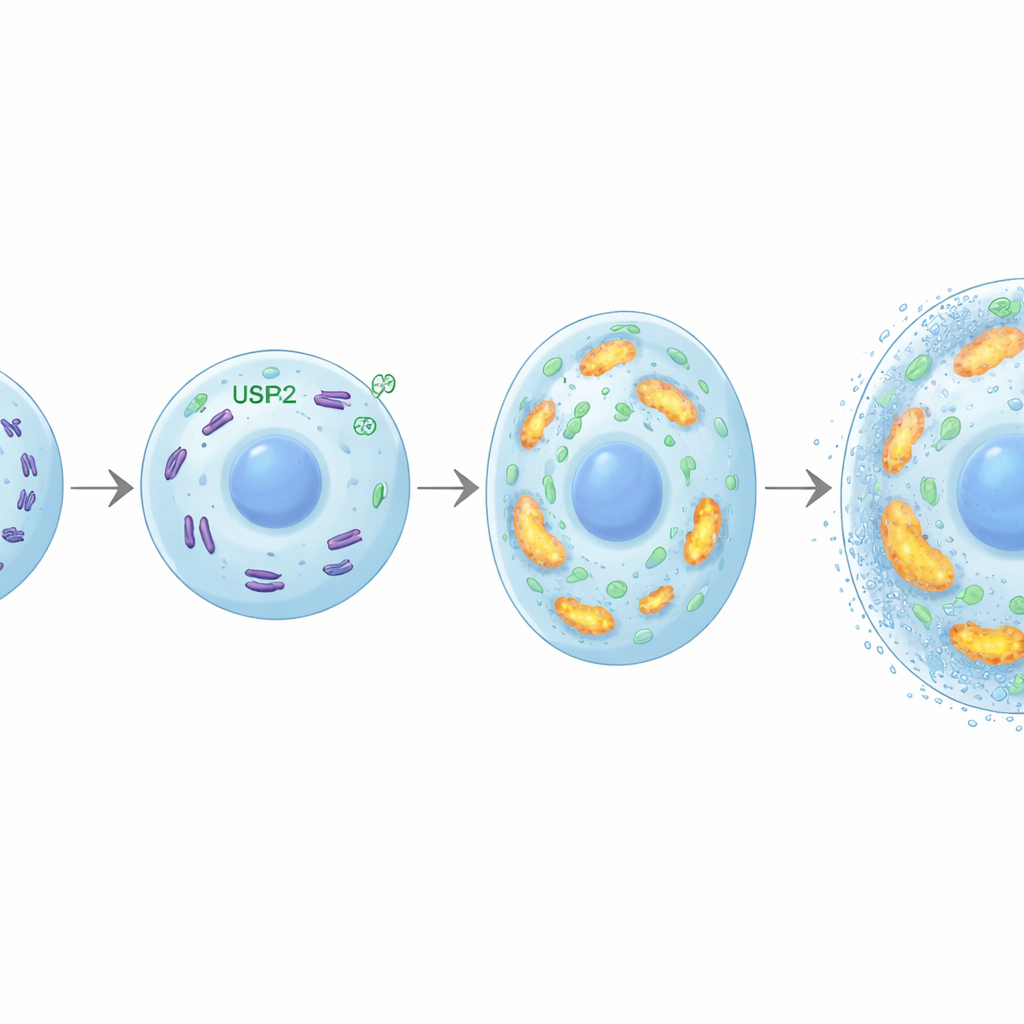
Hoe mechanische krachten USP26 inschakelen
Het skelet voelt voortdurend mechanische krachten en past zich daaraan aan. Het team vond dat zones van kraakbeen onder hoge belasting — zoals dragende gebieden in artritische knieën — hogere USP26‑niveaus vertoonden. In gekweekte chondrocyten zorgde gecontroleerde compressie voor een toename van USP26 en schakelde gelijktijdig genen in die hypertrofie en mineralisatie aansturen. Dit mechanische signaal verliep via oestrogeenreceptor‑α (ER‑α), een hormoon‑gevoelige transcriptiefactor. Onder compressie werd ER‑α geactiveerd door fosforylering op een specifieke plaats (serine 118) en bond het rechtstreeks aan een korte DNA‑sequentie in het controlegebied van het USP26‑gen. Het muteren van óf deze DNA‑plaats óf de fosforyleringsplaats op ER‑α verzwakte de stijging van USP26, hield hogere FBP2‑niveaus in stand en verzwakte de metabolische en ontwikkelingsverschuiving naar botvorming. In muizen die gedwongen werden te rennen en hun kniegewrichten te overbelasten, verminderde de verwijdering van USP26 uit chondrocyten opnieuw de benige overgroei en kraakbeenschade, waarmee de rol ervan als mechanische “sensor‑effector” in vivo werd bevestigd.
Waarom dit belangrijk is voor botten en gewrichten
Kort gezegd helpt USP26 kraakbeencellen mechanische belasting en brandstofaanbod om te zetten in botopbouwende activiteit. Het doet dit door FBP2 te verlagen, robuuste, energieproducerende mitochondriën te behouden en chondrocyten richting vergroting en mineralisatie te duwen. Dat maakt USP26 essentieel voor normale skeletgroei en effectief fractuurgenezing. Maar in verouderende of beschadigde gewrichten die chronisch overbelast zijn, lijkt hetzelfde pad de verharding en overgroei van kraakbeen te stimuleren die kenmerkend zijn voor artrose. Door USP26 zelf of zijn downstream‑partner FBP2 aan te pakken, zouden toekomstige therapieën mogelijk selectief endochondrale ossificatie kunnen versterken wanneer we meer bot nodig hebben — na trauma of bij groeistoornissen — en die tegelijkertijd kunnen afremmen in gewrichten die risico lopen op degeneratieve ziekte.
Bronvermelding: Li, C., Xu, Y., Zhou, L. et al. Ubiquitin-specific protease 26 facilitates endochondral ossification by driving chondrocyte hypertrophy and mineralization. Bone Res 14, 41 (2026). https://doi.org/10.1038/s41413-026-00517-5
Trefwoorden: endochondrale ossificatie, chondrocyt‑hypertrofie, mitochondriale stofwisseling, mechanotransductie, artrose