Clear Sky Science · es
La proteasa específica de ubiquitina 26 facilita la osificación endocondral al promover la hipertrofia y mineralización de los condrocitos
Cómo crecen y se reparan los huesos
Nuestro esqueleto está en constante cambio. Los huesos largos de brazos y piernas se forman primero como cartílago blando, que más tarde se convierte en hueso duro en un proceso llamado osificación endocondral. Ese mismo programa ayuda a sanar fracturas, pero cuando se activa en exceso en las articulaciones puede favorecer la artrosis. Este estudio descubre un interruptor molecular clave, una proteína denominada USP26, que ayuda a las células del cartílago a crecer, endurecerse y responder a fuerzas mecánicas como el peso corporal y el movimiento. Comprender este interruptor podría abrir nuevas vías para potenciar la reparación ósea al tiempo que se frena el daño articular.
El viaje del cartílago blando al hueso duro
En embriones en crecimiento y en fracturas en proceso de curación, células cartilaginosas especializadas llamadas condrocitos primero se multiplican, luego aumentan de tamaño y finalmente contribuyen a depositar mineral para formar hueso. Los autores encontraron que USP26 se vuelve más abundante exactamente cuando y donde ocurre esta transición: en el centro de los huesos en desarrollo de las extremidades de ratón, en el callo cartilaginoso que puentea una fractura en curación y en áreas de cartílago sobredesarrollado en articulaciones con artrosis. Cuando se estimula la maduración de condrocitos en el laboratorio, los niveles de USP26 aumentan en paralelo con marcadores clásicos de hipertrofia (aumento celular) y mineralización. Estos patrones sugieren que USP26 actúa como un acelerador de la transición de cartílago a hueso. 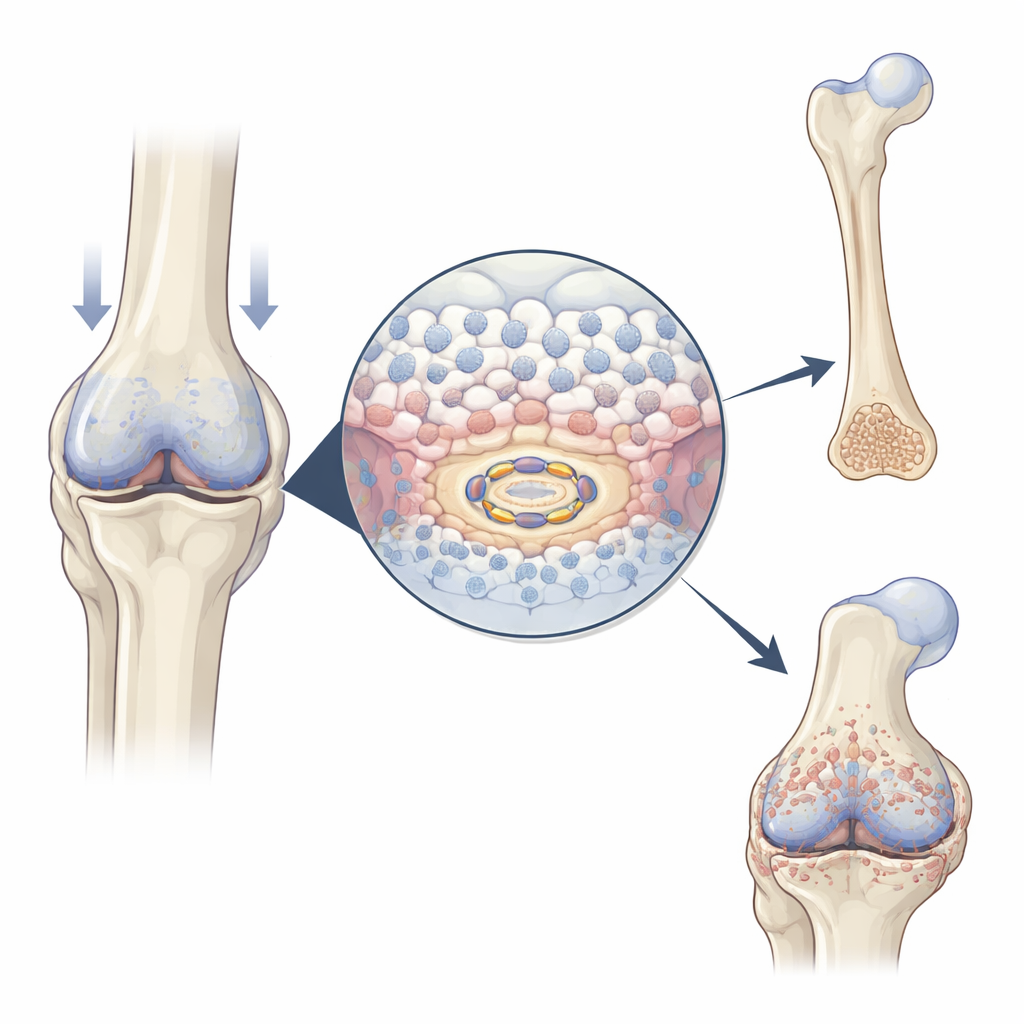
Qué ocurre cuando falta USP26
Para evaluar el papel de USP26, el equipo diseñó ratones en los que esta proteína fue eliminada únicamente de los condrocitos. Estos animales desarrollaron extremidades y vértebras más cortas, reflejando un crecimiento esquelético atrofiado. Sus placas de crecimiento —las zonas donde normalmente se genera nuevo hueso— mostraron menos condrocitos agrandados, cartílago menos mineralizado y una expresión reducida de genes clave que impulsan la formación ósea y la invasión vascular. Cuando estos ratones knock-out sufrieron fracturas de fémur, sus callos contenían menos cartílago y hueso, y las exploraciones mostraron tejido de reparación más débil y menos mineralizado. Al mismo tiempo, eliminar USP26 del cartílago articular protegió frente a artrosis experimentalmente inducida: hubo menos espolones óseos, superficies cartilaginosas más lisas y puntuaciones de gravedad de la enfermedad menores. En conjunto, los hallazgos muestran que USP26 es de doble filo: es necesario para el crecimiento y la reparación normales, pero también contribuye al crecimiento óseo perjudicial en articulaciones enfermas.
Alimentando la formación ósea a través de las centrales energéticas celulares
La ampliación y mineralización de condrocitos requieren grandes cantidades de energía. Los investigadores descubrieron que USP26 ayuda a satisfacer esta demanda manteniendo mitocondrias saludables, las centrales energéticas de la célula. Sin USP26, los condrocitos absorbían menos glucosa, producían menos ATP (la moneda energética celular) y generaban menos lactato. Sus mitocondrias eran menos numerosas, más fragmentadas y funcionaban mal, con actividad respiratoria reducida y menor expresión de genes implicados en la fosforilación oxidativa. Emergió una proteína llamada FBP2 como un vínculo crucial: en ausencia de USP26, los niveles de FBP2 aumentaron considerablemente. FBP2 es conocida por desviar a las células de la quema de glucosa y por suprimir la biogénesis mitocondrial. Aquí, bloquear FBP2 en condrocitos deficientes en USP26 restauró el uso de glucosa, la masa mitocondrial y la producción de energía, y recuperó su capacidad para agrandarse y mineralizarse. En modelos de artrosis, inhibir FBP2 también intensificó la osificación del cartílago, subrayando cómo el equilibrio USP26–FBP2 condiciona los resultados relacionados con el hueso. 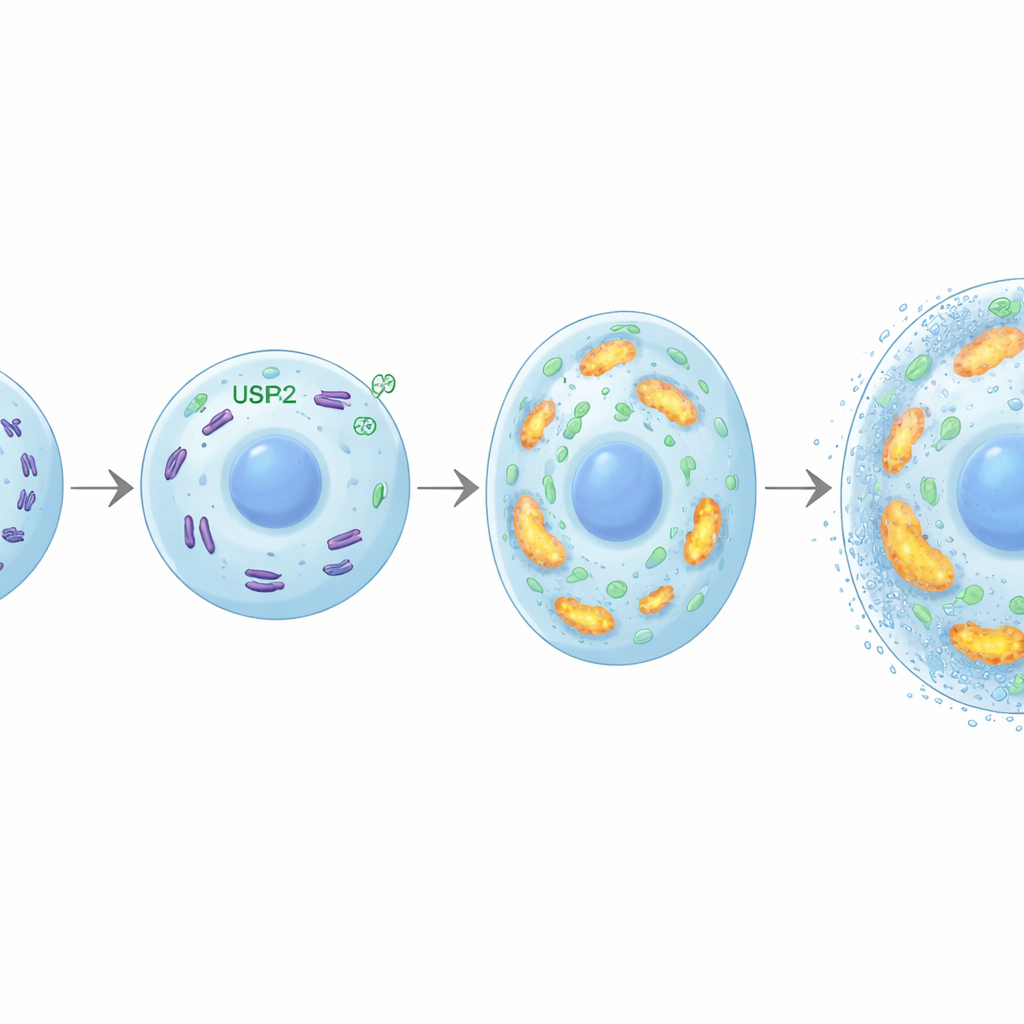
Cómo las fuerzas mecánicas activan USP26
El esqueleto detecta y se adapta continuamente a fuerzas mecánicas. El equipo encontró que zonas de cartílago sometidas a elevada carga —como áreas soportantes de peso en rodillas artríticas— muestran niveles más altos de USP26. En condrocitos cultivados, la aplicación de compresión controlada aumentó USP26 y, al mismo tiempo, activó genes que promueven la hipertrofia y la mineralización. Esta señal mecánica transitó por el receptor de estrógenos α (ER‑α), un factor de transcripción sensible a hormonas. Bajo compresión, ER‑α se activó mediante fosforilación en un sitio específico (serina 118) y se unió directamente a una corta secuencia de ADN en la región reguladora del gen USP26. Mutar ese sitio de ADN o el sitio de fosforilación en ER‑α atenuó el aumento de USP26, mantuvo niveles más altos de FBP2 y debilitó el cambio metabólico y de desarrollo hacia la formación ósea. En ratones obligados a correr y sobrecargar sus articulaciones de la rodilla, la eliminación de USP26 en condrocitos volvió a reducir el sobredesarrollo óseo y el daño cartilaginoso, confirmando su papel como un “sensor‑efector” mecánico in vivo.
Por qué esto importa para huesos y articulaciones
En pocas palabras, USP26 ayuda a las células del cartílago a convertir la carga mecánica y la disponibilidad de combustible en actividad formadora de hueso. Lo hace reduciendo FBP2, preservando mitocondrias robustas y productoras de energía y empujando a los condrocitos hacia la ampliación y la mineralización. Eso hace a USP26 esencial para el crecimiento esquelético normal y la curación eficaz de fracturas. Pero en articulaciones envejecidas o lesionadas expuestas a sobrecarga crónica, la misma vía parece impulsar el endurecimiento y el sobredesarrollo del cartílago que caracterizan la artrosis. Al dirigir terapias contra USP26 en sí o contra su socio downstream FBP2, en el futuro podría ser posible amplificar selectivamente la osificación endocondral cuando necesitemos más hueso —tras un traumatismo o en trastornos del crecimiento— mientras se modera en articulaciones en riesgo de enfermedad degenerativa.
Cita: Li, C., Xu, Y., Zhou, L. et al. Ubiquitin-specific protease 26 facilitates endochondral ossification by driving chondrocyte hypertrophy and mineralization. Bone Res 14, 41 (2026). https://doi.org/10.1038/s41413-026-00517-5
Palabras clave: osificación endocondral, hipertrofia de condrocitos, metabolismo mitocondrial, mecanotransducción, artrosis