Clear Sky Science · ar
البروتياز الخاص باليوبيكويتين 26 يسهل التنسج العظمي البطاني عن طريق دفع تضخيم الخلايا الغضروفية والتكلس
كيف تنمو العظام وتصلح نفسها
هيكلنا العظمي في حالة تغير مستمر. تتشكل العظام الطويلة في الذراعين والساقين أولاً كغضروف لين، يتحول لاحقًا إلى عظم صلب في عملية تسمى التنسج العظمي البطاني. نفس البرنامج يساعد العظام المكسورة على التعافي — لكن عندما يعمل بقوة مفرطة في المفاصل، يمكن أن يغذي أيضًا التهاب المفاصل التنكسي. تكشف هذه الدراسة عن مفتاح جزيئي رئيسي، بروتين يسمى USP26، يساعد خلايا الغضروف على النمو والتصلب والاستجابة للقوى الميكانيكية مثل وزن الجسم والحركة. قد يفتح فهم هذا المفتاح طرقًا جديدة لتعزيز إصلاح العظام مع إبطاء تلف المفاصل.
الرحلة من الغضروف اللين إلى العظم الصلب
في الأجنة النامية وعند شفاء الكسور، تتكاثر خلايا غضروفية متخصصة تُسمى الخلايا الغضروفية أولاً، ثم تتضخم، وأخيرًا تساعد على ترسيب المعدن لتشكيل العظم. وجد الباحثون أن مستوى USP26 يزداد بالضبط عندما وأين يحدث هذا الانتقال: في منتصف عظام أطراف فأر نامية، وفي الندبة الغضروفية التي تربط كسرًا شافيًا، وفي مناطق الغضروف المتضخمة في المفاصل المصابة بالتهاب المفاصل التنكسي. عندما تُحفز الخلايا الغضروفية على النضج في المختبر، ترتفع مستويات USP26 بالتزامن مع علامات التضخيم والتكلس المألوفة. تشير هذه الأنماط إلى أن USP26 يعمل كمسرع لانتقال الغضروف إلى عظم. 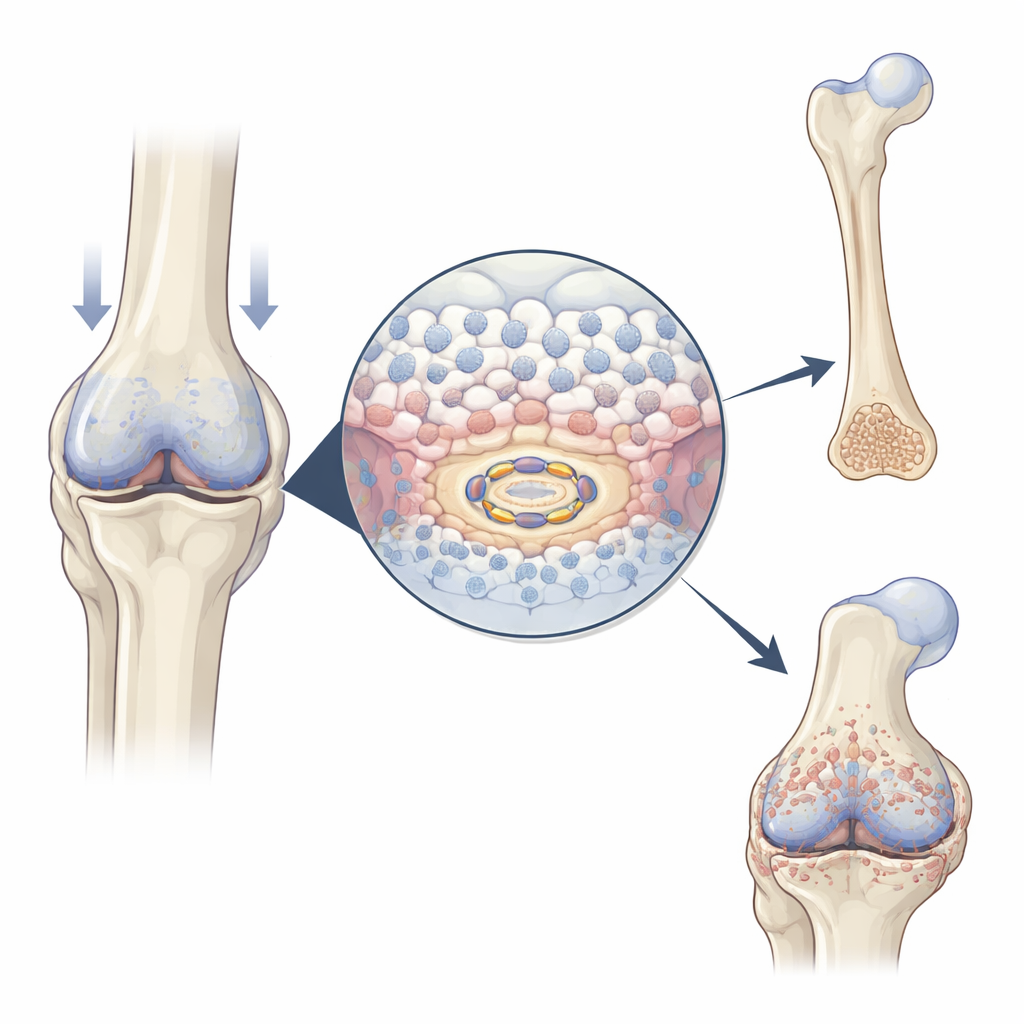
ماذا يحدث عندما يغيب USP26
لاختبار دور USP26، مهندس الفريق فئرانًا أُزيل فيها هذا البروتين من الخلايا الغضروفية فقط. طورت هذه الحيوانات أطرافًا وعمودًا فقريًا أقصر، ما يعكس تباطؤ النمو الهيكلي. أظهرت صفائح النمو — المناطق التي يتشكل فيها العظم الجديد عادة — عددًا أقل من الخلايا الغضروفية المتضخمة، وغضروفًا أقل تكلسًا، وتعبيرًا منخفضًا لجينات مفتاحية تدفع تكوين العظم وغزو الأوعية الدموية. عندما تعرضت هذه الفئران المعدلة لكسر في الفخذ، احتوت ندباتها على غضروف وعظم أقل، وكشفت الفحوصات عن نسيج إصلاح أضعف وأقل تكلسًا. في المقابل، أدت إزالة USP26 من غضروف المفصل إلى حماية ضد التهاب المفاصل المستحث تجريبيًا: كانت نتوءات عظمية أقل، وأساطح الغضروف أكثر نعومة، وتراجعت درجات شدة المرض. مجتمعة، تُظهر النتائج أن USP26 ذو حدين — إنه ضروري للنمو والإصلاح الطبيعيين، لكنه أيضًا يساهم في نمو عظمي مفرط ضار في المفاصل المريضة.
تغذية تكوين العظم عبر مصانع الطاقة الخلوية
يتطلب تضخم الخلايا الغضروفية والتكلس كميات كبيرة من الطاقة. اكتشف الباحثون أن USP26 يساعد في تلبية هذا الطلب عن طريق الحفاظ على ميتوكوندريا صحية، وهي مصانع الطاقة في الخلية. بدون USP26، امتصت الخلايا الغضروفية جلوكوزًا أقل، أنتجت ATP أقل (عملة طاقة الخلية)، وأنتجت لاكتات أقل. كانت ميتوكوندريا هذه الخلايا أقل عددًا، أكثر تجزؤًا، وتعمل بشكل سيئ، مع انخفاض في النشاط التنفسي وتعبير الجينات المشاركة في الفسفرة التأكسدية. ظهر بروتين يسمى FBP2 كرابط حاسم: في غياب USP26، ارتفعت مستويات FBP2 بشكل حاد. يُعرف عن FBP2 أنه يميل بالخلايا بعيدًا عن حرق الجلوكوز ويثبط تكوين الميتوكوندريا. هنا، أدّى حجب FBP2 في الخلايا الغضروفية الخالية من USP26 إلى استعادة استخدام الجلوكوز وكتلة الميتوكوندريا وإنتاج الطاقة، وإحياء قدرتها على التضخم والتكلس. في نماذج التهاب المفاصل، أدى تثبيط FBP2 أيضًا إلى تكثيف تآرم الغضروف، مما يؤكد كيف يشكل توازن USP26–FBP2 مآلات متعلقة بالعظم. 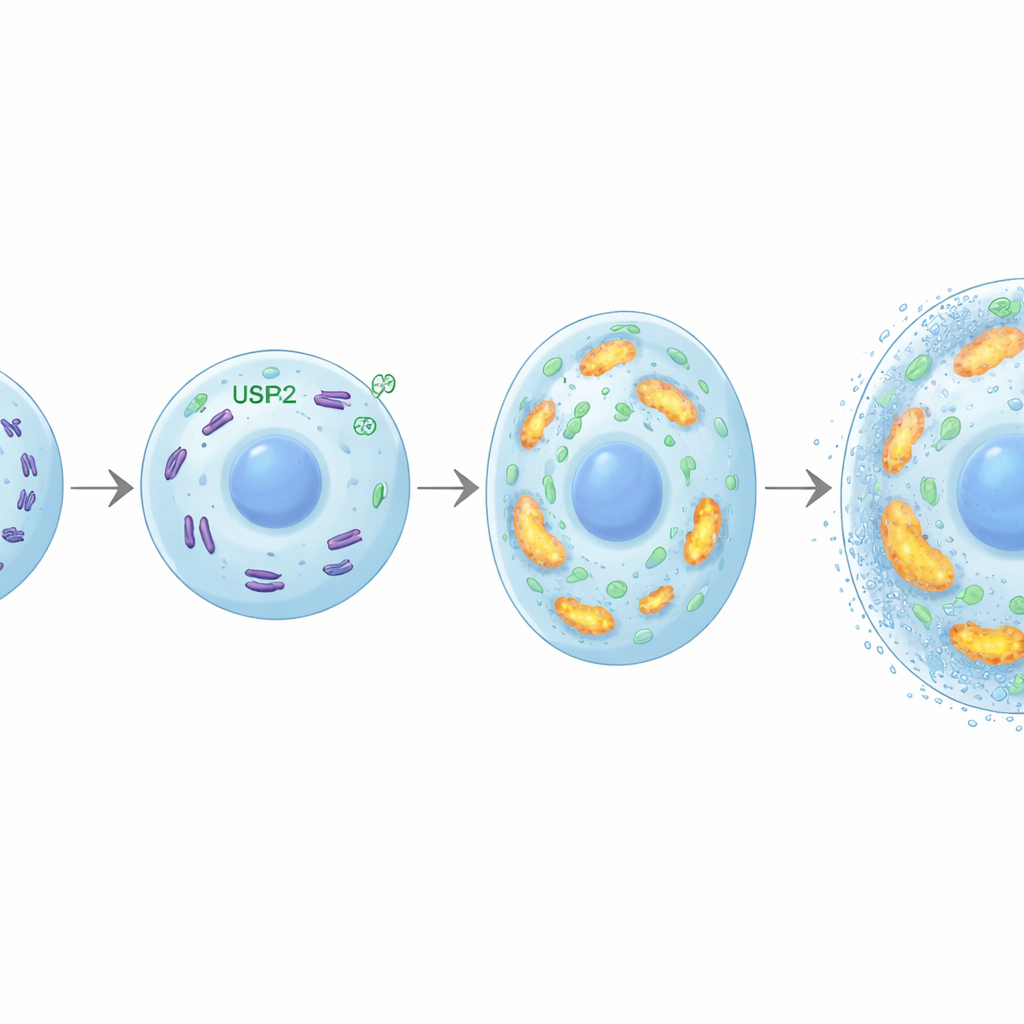
كيف تشغّل القوى الميكانيكية USP26
يشعر الهيكل العظمي باستمرار بالقوى الميكانيكية ويتأقلم معها. وجد الفريق أن مناطق الغضروف تحت حمولة ثقيلة — مثل مناطق تحمل الوزن في الركب المصابة بالتهاب المفاصل — تظهر مستويات أعلى من USP26. في الخلايا الغضروفية المزرعية، أدت الضغوط المطبقة بشكل منضبط إلى زيادة USP26 وفي الوقت نفسه إلى تشغيل جينات تدفع التضخيم والتكلس. سرت هذه الإشارة الميكانيكية عبر مستقبل الإستروجين‑α (ER‑α)، وهو عامل نسخ مستجيب للهرمونات. تحت الضغط، نُشط ER‑α عبر فوسفوريلation في موقع محدد (السيرين 118) وارتبط مباشرة بتسلسل DNA قصير في منطقة تنظيم جين USP26. تسببت طفرات إما في هذا الموقع من الـDNA أو في موقع الفوسفوريلة على ER‑α في تخفيف ارتفاع USP26، والحفاظ على مستويات FBP2 أعلى، وإضعاف التحول الأيضي والتنموي نحو تكوين العظم. في فئران أُجبرت على الجري وتحميل ركبتها زائدًا، قلّ إحداث النمو العظمي المفرط وتلف الغضروف عند حذف USP26 في الخلايا الغضروفية، مؤكدة دوره كـ"مستشعر–منفذ" ميكانيكي في الجسم الحي.
لماذا يهم هذا للعظام والمفاصل
ببساطة، يساعد USP26 خلايا الغضروف على تحويل الحمولة الميكانيكية ومخزون الوقود إلى نشاط بناء عظمي. يفعل ذلك عن طريق خفض FBP2، والحفاظ على ميتوكوندريا قوية منتجة للطاقة، ودفع الخلايا الغضروفية نحو التضخم والتكلس. يجعل هذا USP26 ضروريًا للنمو الهيكلي الطبيعي ولشَفَاء الكسور الفعال. لكن في المفاصل المتقدّم بها العمر أو المصابة والمعرضة للتحميل المزمن، يبدو أن نفس المسار يقود تصلبًا ونموًا عظميًا مفرطًا في الغضروف الذي يميّز التهاب المفاصل التنكسي. من خلال استهداف USP26 نفسه أو شريكه الطرفي FBP2، قد تتيح العلاجات المستقبلية تضخيم التنسج العظمي البطاني انتقائيًا عندما نحتاج المزيد من العظم — بعد الصدمة أو في اضطرابات النمو — مع تقليصه في المفاصل المعرضة لمرض تنكسي.
الاستشهاد: Li, C., Xu, Y., Zhou, L. et al. Ubiquitin-specific protease 26 facilitates endochondral ossification by driving chondrocyte hypertrophy and mineralization. Bone Res 14, 41 (2026). https://doi.org/10.1038/s41413-026-00517-5
الكلمات المفتاحية: التنسج العظمي البطاني, تضخيم الخلايا الغضروفية, استقلاب الميتوكوندريا, التحويل الميكانيكي للإشارات, التهاب المفاصل التنكسي