Clear Sky Science · ru
Специфичная к убиквитину протеаза 26 облегчает эндохондральное окостенение, стимулируя гипертрофию хондроцитов и минерализацию
Как кости растут и восстанавливаются
Наш скелет постоянно меняется. Длинные кости в руках и ногах сначала формируются как мягкий хрящ, который затем превращается в твёрдую кость в процессе, называемом эндохондральным окостенением. Тот же механизм помогает заживлению переломов — но если он работает слишком активно в суставах, это может усугублять остеоартрит. В этом исследовании обнаружен ключевой молекулярный переключатель — белок USP26, который помогает хрящевым клеткам расти, уплотняться и реагировать на механические силы, такие как вес тела и движение. Понимание этого переключателя может открыть новые пути для усиления восстановления костей при одновременном замедлении повреждений суставов.
Путь от мягкого хряща к твёрдой кости
У растущих эмбрионов и при заживлении переломов специализированные хрящевые клетки, известные как хондроциты, сначала размножаются, затем увеличиваются в размере и наконец участвуют в отложении минералов, формирующих кость. Авторы обнаружили, что USP26 становится более распространённым точно тогда и там, где происходит этот переход: в середине развивающихся конечностей мышей, в хрящевом каллусе, который заполняет перелом, и в разросшихся участках хряща при остеоартрите. Когда в культуре стимулируют созревание хондроцитов, уровни USP26 повышаются синхронно с классическими маркерами гипертрофии (увеличения клетки) и минерализации. Эти закономерности указывают на то, что USP26 действует как акселератор перехода от хряща к кости. 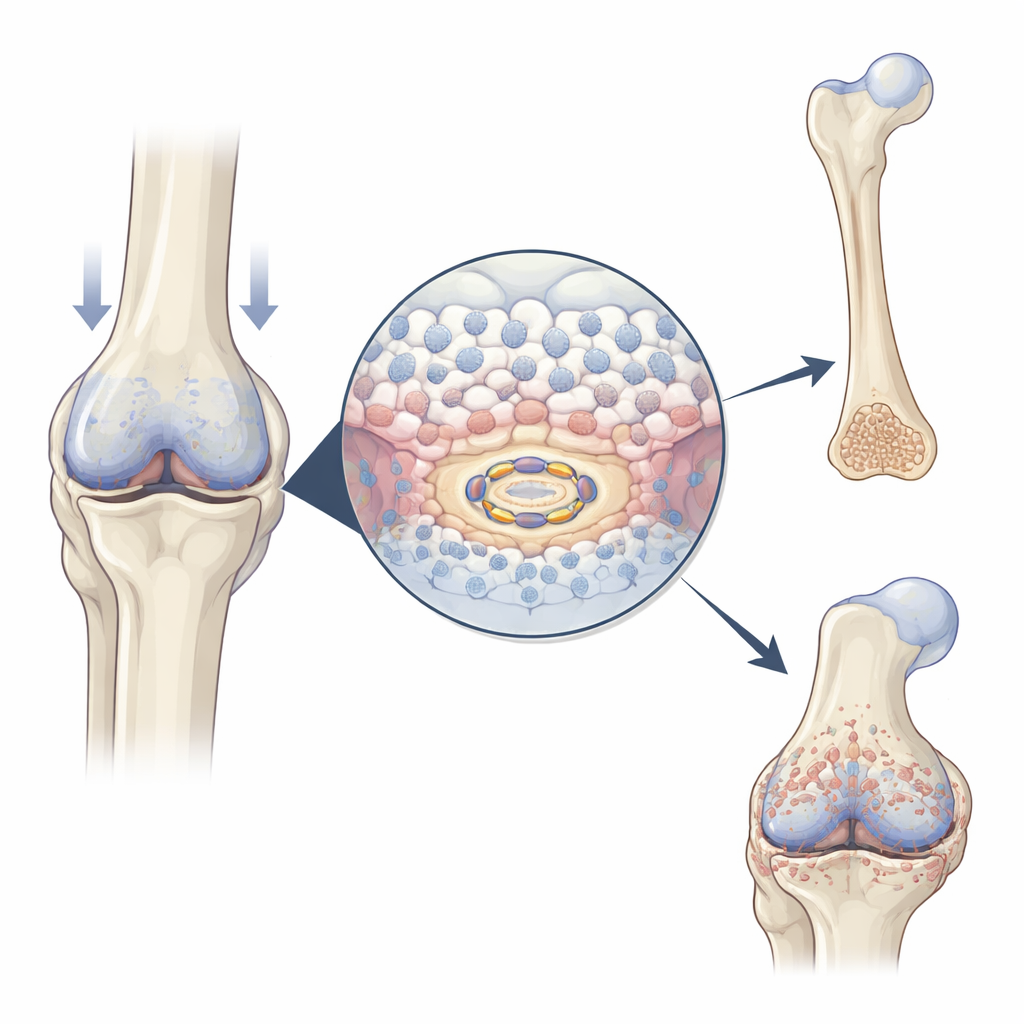
Что происходит, когда USP26 отсутствует
Чтобы проверить роль USP26, команда создала мышей, у которых этот белок был удалён только из хондроцитов. Эти животные развивались с укороченными конечностями и позвонками, что отражало замедленный рост скелета. Их зоны роста — участки, где обычно образуется новая кость — демонстрировали меньше увеличившихся хондроцитов, менее минерализованный хрящ и пониженную экспрессию ключевых генов, управляющих формированием кости и инвазией кровеносных сосудов. Когда у этих нокаутных мышей случались переломы бедренной кости, их каллусы содержали меньше хряща и кости, а сканы показывали более слабую, менее минерализованную ткань восстановления. Одновременно удаление USP26 из суставного хряща защищало от экспериментально вызванного остеоартрита: наблюдалось меньше остеофитов, более гладкие поверхности хряща и более низкие показатели тяжести болезни. В совокупности результаты показывают, что USP26 — двузначный фактор: он необходим для нормального роста и восстановления, но также способствует вредному разрастанию кости в поражённых суставах.
Питание формирования кости через клеточные энергостанции
Увеличение хондроцитов и минерализация требуют больших объёмов энергии. Исследователи обнаружили, что USP26 помогает удовлетворить эту потребность, поддерживая здоровье митохондрий — клеточных энергостанций. Без USP26 хондроциты поглощали меньше глюкозы, вырабатывали меньше АТФ (энергетической валюты клетки) и давали меньше лактата. Их митохондрий было меньше, они были более фрагментированы и работали хуже, с пониженной дыхательной активностью и экспрессией генов, вовлечённых в окислительное фосфорилирование. Белок FBP2 выявился как ключевое звено: при отсутствии USP26 уровни FBP2 резко повышались. Известно, что FBP2 смещает метаболизм клетки от использования глюкозы и подавляет биогенез митохондрий. В этом исследовании блокирование FBP2 в хондроцитах, лишённых USP26, восстановило потребление глюкозы, массу митохондрий и выработку энергии и возродило их способность увеличиваться и минерализоваться. В моделях остеоартрита ингибирование FBP2 также усиливало окостенение хряща, подчёркивая, как баланс USP26–FBP2 формирует исходы, связанные с образованием кости. 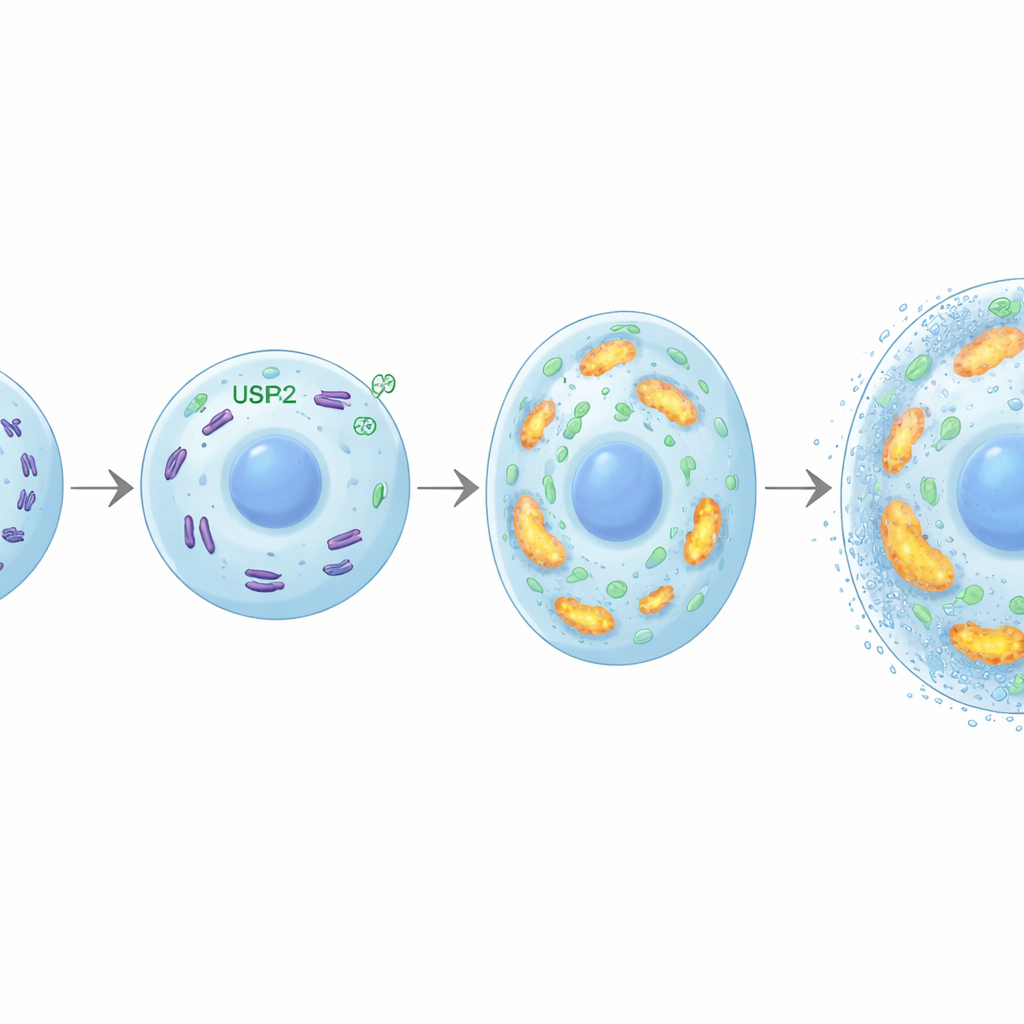
Как механические силы включают USP26
Скелет постоянно ощущает и адаптируется к механическим нагрузкам. Команда обнаружила, что участки хряща, испытывающие сильную нагрузку — например, опорные зоны в артритических коленях — демонстрируют более высокие уровни USP26. В культивируемых хондроцитах применение контролируемой компрессии повышало USP26 и одновременно включало гены, стимулирующие гипертрофию и минерализацию. Этот механический сигнал проходил через эстрогеновый рецептор‑α (ER‑α), гормонозависимый транскрипционный фактор. При компрессии ER‑α активировался фосфорилированием в определённой позиции (серин 118) и прямо связывался с короткой последовательностью ДНК в регуляторной области гена USP26. Мутация либо этой ДНК‑мишени, либо фосфорилируемого сайта на ER‑α ослабляла рост USP26, сохраняла повышенные уровни FBP2 и уменьшала метаболический и дифференцировочный сдвиг в сторону образования кости. У мышей, вынужденных бегать и перегружать свои коленные суставы, удаление USP26 в хондроцитах снова снижало костное разрастание и повреждение хряща, подтверждая его роль как механического «сенсора‑эффектора» in vivo.
Почему это важно для костей и суставов
Проще говоря, USP26 помогает хрящевым клеткам преобразовывать механическую нагрузку и доступность топлива в активность по построению кости. Он действует, снижая FBP2, поддерживая мощные, энергообразующие митохондрии и направляя хондроциты к увеличению и минерализации. Это делает USP26 незаменимым для нормального скелетного роста и эффективного заживления переломов. Но у стареющих или повреждённых суставов, подвергающихся хронической перегрузке, та же схема, по-видимому, приводит к уплотнению и разрастанию хряща — признакам остеоартрита. Нацеленность на USP26 или на его мишень FBP2 может в будущем позволить избирательно усиливать эндохондральное окостенение там, где нужно больше кости — после травмы или при нарушениях роста, — и одновременно ослаблять его в суставах, подверженных дегенеративным изменениям.
Цитирование: Li, C., Xu, Y., Zhou, L. et al. Ubiquitin-specific protease 26 facilitates endochondral ossification by driving chondrocyte hypertrophy and mineralization. Bone Res 14, 41 (2026). https://doi.org/10.1038/s41413-026-00517-5
Ключевые слова: эндохондральное окостенение, гипертрофия хондроцитов, митохондриальный метаболизм, механотрансдукция, остеоартрит