Clear Sky Science · it
La proteasi specifica per ubiquitina 26 facilita l’ossificazione endocondrale promuovendo l’ipertrofia e la mineralizzazione dei condrociti
Come le ossa crescono e si riparano
Il nostro scheletro è in continuo cambiamento. Le ossa lunghe di braccia e gambe si formano inizialmente come cartilagine morbida, che poi si trasforma in osso duro in un processo chiamato ossificazione endocondrale. Lo stesso programma favorisce la guarigione delle fratture—ma se si attiva eccessivamente nelle articolazioni, può alimentare l’artrosi. Questo studio mette in luce un interruttore molecolare chiave, una proteina chiamata USP26, che aiuta le cellule cartilaginee a crescere, indurirsi e rispondere a forze meccaniche come il peso corporeo e il movimento. Comprendere questo interruttore potrebbe aprire nuove strade per migliorare la riparazione ossea rallentando al contempo il danno articolare.
Il viaggio dalla cartilagine morbida all’osso duro
Negli embrioni in crescita e nelle fratture in guarigione, particolari cellule cartilaginee note come condrociti prima si moltiplicano, poi aumentano di volume e infine contribuiscono a depositare minerali per formare l’osso. Gli autori hanno osservato che USP26 aumenta precisamente quando e dove avviene questa transizione: al centro delle ossa degli arti in sviluppo nei topi, nel callo cartilagineo che unisce una frattura in guarigione e nelle aree di cartilagine ipertrofica presenti nelle articolazioni artrosiche. Quando in coltura si induce la maturazione dei condrociti, i livelli di USP26 crescono in parallelo ai marcatori classici di ipertrofia (ingrandimento cellulare) e mineralizzazione. Questi schemi suggeriscono che USP26 funzioni come un acceleratore della transizione cartilagine-osso. 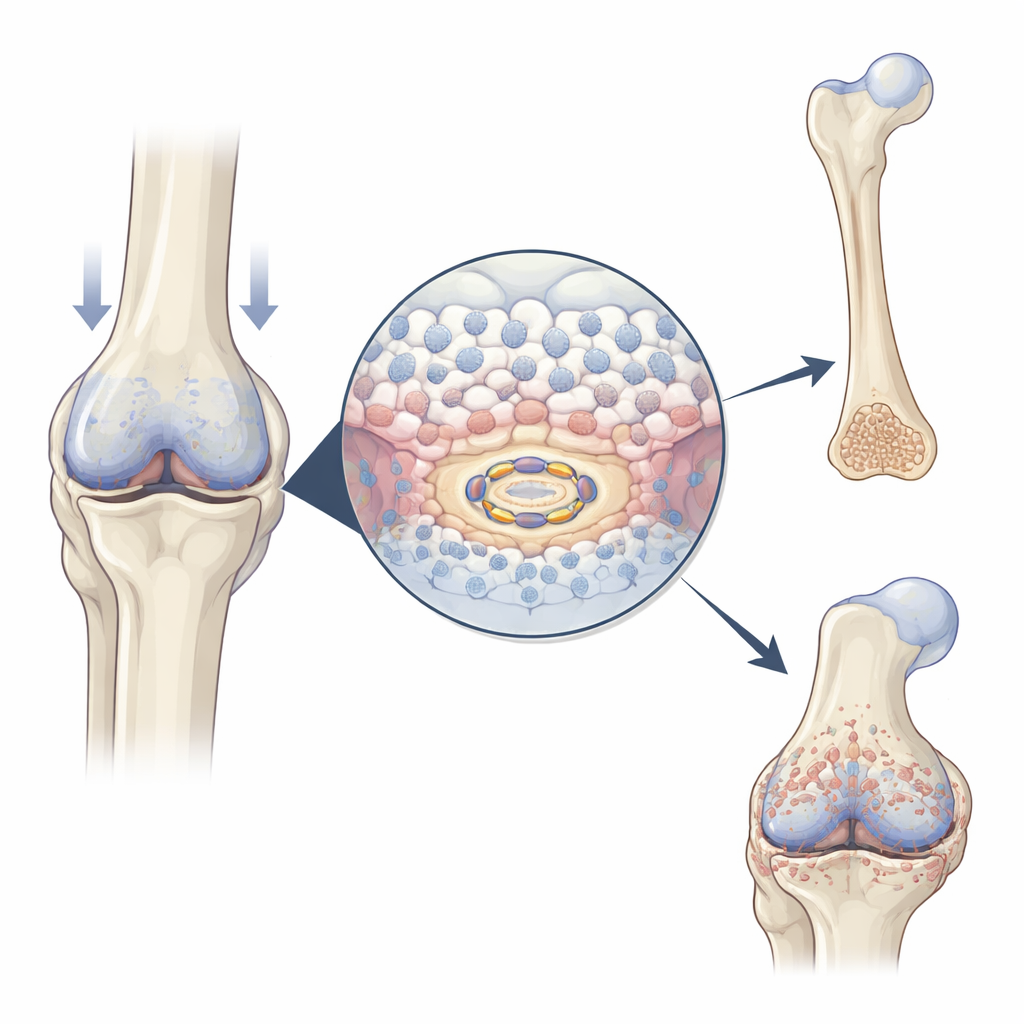
Cosa succede quando manca USP26
Per testare il ruolo di USP26, il gruppo ha ingegnerizzato topi in cui questa proteina è stata rimossa solo dai condrociti. Questi animali hanno sviluppato arti e vertebre più corti, riflettendo una crescita scheletrica ridotta. Le loro placche di crescita—le zone dove normalmente si forma nuovo osso—mostravano meno condrociti ingranditi, cartilagine meno mineralizzata e una minore espressione di geni chiave che guidano la formazione ossea e l’invasione vascolare. Quando questi topi knockout subirono fratture del femore, i loro calli contenevano meno cartilagine e osso e le scansioni rivelarono tessuto di riparazione più debole e meno mineralizzato. Allo stesso tempo, la rimozione di USP26 nella cartilagine articolare proteggeva dall’artrosi indotta sperimentalmente: si osservavano meno speroni ossei, superfici cartilaginee più lisce e punteggi di gravità della malattia più bassi. Complessivamente, i risultati dimostrano che USP26 ha un effetto a doppio taglio—è necessario per la crescita e la riparazione normali, ma contribuisce anche a un eccesso di crescita ossea nelle articolazioni malate.
Alimentare la formazione ossea attraverso le centrali energetiche cellulari
L’ingrandimento e la mineralizzazione dei condrociti richiedono grandi quantità di energia. I ricercatori hanno scoperto che USP26 aiuta a soddisfare questa domanda mantenendo mitocondri sani, le centrali energetiche della cellula. Senza USP26, i condrociti assorbivano meno glucosio, producevano meno ATP (la valuta energetica cellulare) e generavano meno lattato. I loro mitocondri erano in numero ridotto, più frammentati e funzionavano male, con attività respiratoria ridotta ed espressione inferiore di geni coinvolti nella fosforilazione ossidativa. Una proteina chiamata FBP2 è emersa come anello critico: in assenza di USP26, i livelli di FBP2 aumentavano nettamente. FBP2 è nota per deviare le cellule dal consumo di glucosio e per sopprimere la biogenesi mitocondriale. In questo contesto, bloccare FBP2 nei condrociti privi di USP26 ha ripristinato l’uso del glucosio, la massa mitocondriale e la produzione di energia, e ha riattivato la loro capacità di ingrandirsi e mineralizzarsi. Nei modelli di artrosi, l’inibizione di FBP2 ha inoltre intensificato l’ossificazione della cartilagine, sottolineando come l’equilibrio USP26–FBP2 modelli gli esiti legati all’osso. 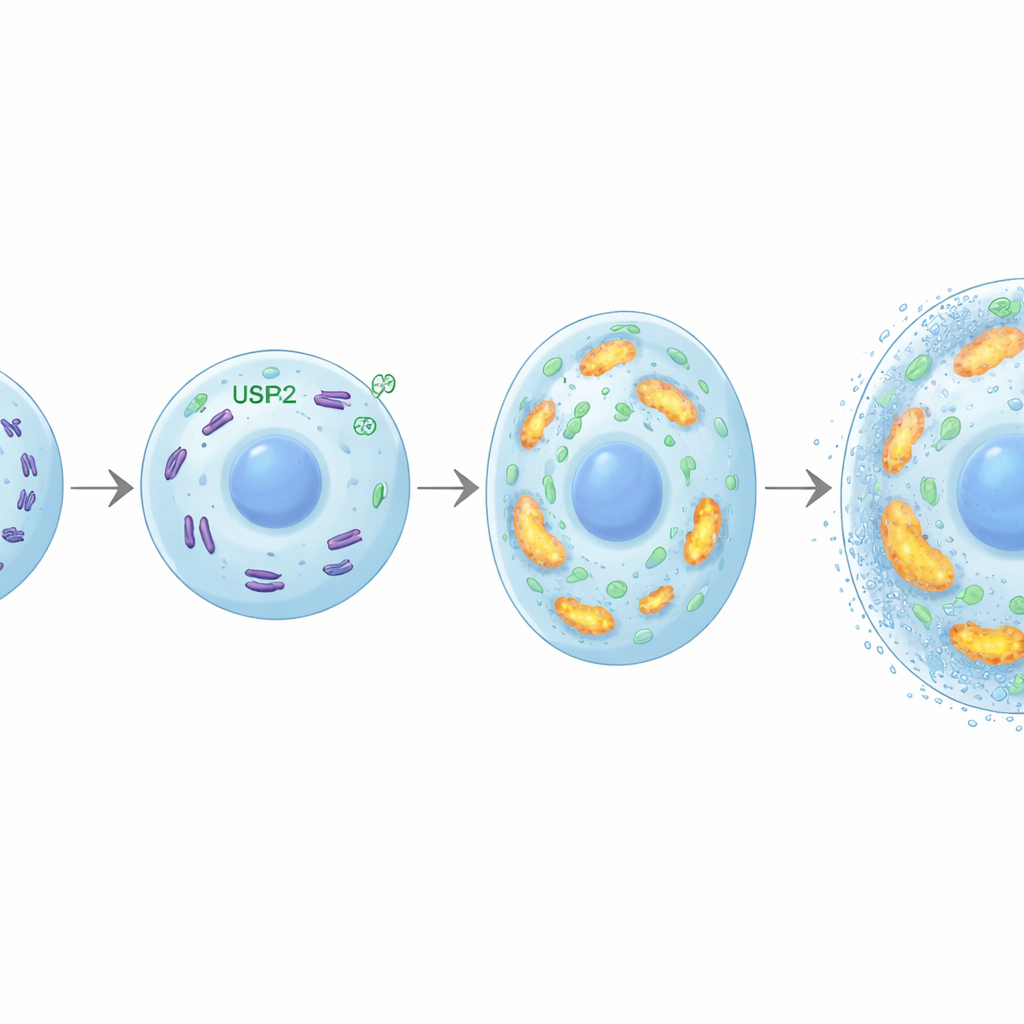
Come le forze meccaniche attivano USP26
Lo scheletro percepisce e si adatta costantemente alle forze meccaniche. Il gruppo ha scoperto che le zone di cartilagine soggette a carico intenso—come le aree portanti nelle ginocchia artrosiche—mostrano livelli più alti di USP26. Nei condrociti in coltura, l’applicazione di compressione controllata ha aumentato USP26 e, simultaneamente, ha attivato geni che promuovono ipertrofia e mineralizzazione. Questo segnale meccanico transitava attraverso il recettore degli estrogeni‑α (ER‑α), un fattore di trascrizione sensibile agli ormoni. Sotto compressione, ER‑α veniva attivato per fosforilazione in un sito specifico (serina 118) e si legava direttamente a una breve sequenza di DNA nella regione di controllo del gene USP26. Mutare sia questo sito del DNA sia il sito di fosforilazione su ER‑α attenuava l’aumento di USP26, manteneva livelli più alti di FBP2 e indeboliva lo spostamento metabolico e di sviluppo verso la formazione ossea. In topi costretti a correre e sovraccaricare le articolazioni del ginocchio, la delezione di USP26 nei condrociti riduceva di nuovo l’ipercrescita ossea e il danno cartilagineo, confermandone il ruolo come “sensore‑effettore” meccanico in vivo.
Perché questo è importante per ossa e articolazioni
In termini semplici, USP26 aiuta le cellule cartilaginee a convertire il carico meccanico e le risorse energetiche in attività di costruzione ossea. Lo fa abbassando FBP2, preservando mitocondri robusti e produttivi e spingendo i condrociti verso l’ingrandimento e la mineralizzazione. Ciò rende USP26 essenziale per la crescita scheletrica normale e per la guarigione efficace delle fratture. Ma in articolazioni invecchiate o danneggiate esposte a sovraccarico cronico, lo stesso percorso sembra guidare l’indurimento e l’ipercrescita della cartilagine che caratterizzano l’artrosi. Mirare a USP26 stesso, o al suo partner a valle FBP2, potrebbe in futuro permettere terapie in grado di amplificare selettivamente l’ossificazione endocondrale quando serve più osso—dopo traumi o in patologie della crescita—mentre la riducono nelle articolazioni a rischio di degenerazione.
Citazione: Li, C., Xu, Y., Zhou, L. et al. Ubiquitin-specific protease 26 facilitates endochondral ossification by driving chondrocyte hypertrophy and mineralization. Bone Res 14, 41 (2026). https://doi.org/10.1038/s41413-026-00517-5
Parole chiave: ossificazione endocondrale, ipertrofia dei condrociti, metabolismo mitocondriale, meccanotrasduzione, artrosi